配合物在许多尖端领域如激光材料、超导材料、抗癌药物、催化剂、自组装超分子等方面有广泛的应用。回答下列问题:
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为___________ 。CO的结构式为C≡O,则Ni(CO)4分子中σ键与π键个数之比为___________ 。
(2)胆矾溶于水后可得蓝色的水合铜离子,其中 的配位数是
的配位数是___________ 。胆矾晶体的结构如下图所示,其存在的化学键有___________ (填字母)。

A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。
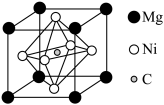
①该物质的化学式为___________ 。
②每个Mg原子距离最近的Ni原子的个数是___________ 。
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为___________ nm3(用含ρ、NA的代数式表示)。
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为
(2)胆矾溶于水后可得蓝色的水合铜离子,其中
 的配位数是
的配位数是
A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。

①该物质的化学式为
②每个Mg原子距离最近的Ni原子的个数是
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为
更新时间:2023-07-05 18:19:54
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
【推荐1】回答下列问题
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是_______ (填元素符号,下同);
②B、C、D、E的第一电离能由小到大的顺序是_______ ;
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是_______ 。
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
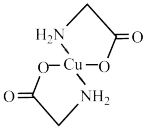
①硅原子电子占据的最高能级电子云形状为_______ ;
②Fe3+的价电子排布图为_______ ;
③铜位于周期表中_______ 区,铜原子的电子排布式为_______ 。试从核外电子排布角度比较,高温下Cu2O和CuO的稳定性更高的原因是_______ 。
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是
②B、C、D、E的第一电离能由小到大的顺序是
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:

①硅原子电子占据的最高能级电子云形状为
②Fe3+的价电子排布图为
③铜位于周期表中
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为___________ ;Y的简化电子排布式为___________ ;Z的电子排布式为____________ ;YX2的化学式是________ ,电子式是________ ;ZX2的化学式是________ 。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】硫酸亚铁铵晶体[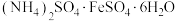 ]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:

回答下列问题:
(1)步骤①需要的玻璃仪器有烧杯、___________ 、___________ (填仪器名称)。
(2)制备硫酸亚铁过程加入炭黑的目的为___________ 。
(3)步骤②的具体操作为___________ 、___________ 、___________ 。
(4)“洗涤”包含水洗、醇洗,其中用乙醇洗涤的目的是___________ 。
(5)写出基态Fe原子的核外电子排布式:___________ 。
(6)称取16.0g制得的粗产品于100mL烧杯中,加入2mL3
 ,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
 ,再用0.1
,再用0.1
 标准溶液滴定。平行滴定三次,平均消耗12.00mL
标准溶液滴定。平行滴定三次,平均消耗12.00mL 标准溶液,产品纯度为
标准溶液,产品纯度为___________ 。(写出计算过程,已知M[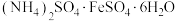 ]为392g/mol)
]为392g/mol)
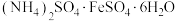 ]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
回答下列问题:
(1)步骤①需要的玻璃仪器有烧杯、
(2)制备硫酸亚铁过程加入炭黑的目的为
(3)步骤②的具体操作为
(4)“洗涤”包含水洗、醇洗,其中用乙醇洗涤的目的是
(5)写出基态Fe原子的核外电子排布式:
(6)称取16.0g制得的粗产品于100mL烧杯中,加入2mL3

 ,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
 ,再用0.1
,再用0.1
 标准溶液滴定。平行滴定三次,平均消耗12.00mL
标准溶液滴定。平行滴定三次,平均消耗12.00mL 标准溶液,产品纯度为
标准溶液,产品纯度为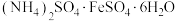 ]为392g/mol)
]为392g/mol)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期数相同;其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族。请回答下列问题:
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是___________ (任写一种)。
(2)C的简单氢化物的电子式为___________ 。
(3)B的氢化物中空间结构为正四面体形的是___________ (填名称),键角为___________ ,中心原子的杂化方式为___________ 杂化。
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为___________ 。
(5)基态原子第一电离能:C___________ (填“>”“<”或“=”)E.
(6)离子CD3-的中心原子的价层电子对数为___________ 。
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是
(2)C的简单氢化物的电子式为
(3)B的氢化物中空间结构为正四面体形的是
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为
(5)基态原子第一电离能:C
(6)离子CD3-的中心原子的价层电子对数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】已知A、B、C、D四种分子所含原子的数目依次为1、3、6、2,且都含有18个电子,B、C由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D元素的氢化物能刻蚀玻璃。
(1)A的分子式是______ ,写出A原子的最后两个能级的电子排布式:________ 。
(2)B分子的中心原子的杂化类型是_______ ,分子的空间结构是______ ,该分子属于_______ 分子(填“极性”或“非极性”)。
(3)C的化学式是______ ,分子中含有的化学键类型是_______ (根据键的极性)。
(4)D元素氢化物的沸点比HCl的沸点高,其主要原因是______ 。
(1)A的分子式是
(2)B分子的中心原子的杂化类型是
(3)C的化学式是
(4)D元素氢化物的沸点比HCl的沸点高,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中基态A原子的电子分布在3个能级,且每个能级所含的电子数相同;C的原子核外最外层有 6 个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物的水化物酸性最强;基态F原子核外最外层只有一个电子,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)下列物质的性质与氢键有关的是_______ 。
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为_______ 。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为_______ 。
(3)F原子的外围电子排布式为_______ 。
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为_______ 。
(5)通常情况下,D单质的熔沸点比G单质高,原因是_______ 。
(6)已知 DE 晶体的晶胞如图所示:
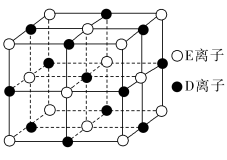
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有_______ 个 A 原子,该晶体的密度是_______ g·cm-3(列式表示)。
(1)下列物质的性质与氢键有关的是
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为
(3)F原子的外围电子排布式为
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
(5)通常情况下,D单质的熔沸点比G单质高,原因是
(6)已知 DE 晶体的晶胞如图所示:

若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有
您最近一年使用:0次
【推荐1】布洛芬(D)是解热类镇痛药,目前醇羰基化BHC法是以异丁苯为原料制取布洛芬最先进的工艺,其流程如下图:
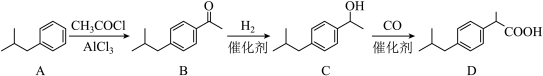
(1) 的反应方程式为
的反应方程式为___________ 。
(2) 的反应类型为
的反应类型为___________ 。
(3)布洛芬(D)的分子式为___________ ,其一卤代物有___________ 种。
(4)CO做配体时,碳原子的配位能力___________ 氧原子(填“大于”“小于”或“等于”),其原因是___________ 。
(5)A的同分异构体中核磁共振氢谱峰面积之比为6:3:2:2:1的所有分子的结构简式为___________ 。

(1)
 的反应方程式为
的反应方程式为(2)
 的反应类型为
的反应类型为(3)布洛芬(D)的分子式为
(4)CO做配体时,碳原子的配位能力
(5)A的同分异构体中核磁共振氢谱峰面积之比为6:3:2:2:1的所有分子的结构简式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】铁和硫及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
(1)基态 的价电子排布图为
的价电子排布图为______ 。
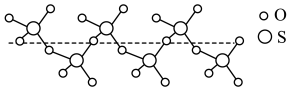
(2)某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图所示,从该结构片段分析可知该物质的化学式为______ ,两种原子的第一电离能大小关系是______ 。
(3)有机铁肥三硝酸六尿素合铁(Ⅲ)的化学式为 。尿素分子中C原子的杂化方式是
。尿素分子中C原子的杂化方式是______ , 中“
中“ ”与
”与 (Ⅲ)之间的作用力是
(Ⅲ)之间的作用力是______ ,根据价层电子对互斥理论推测 的空间构型为
的空间构型为____________ 。
(4) 可用
可用 检验,
检验, 对应的酸有两种,分别为硫氰酸
对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸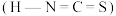 ,这两种酸中沸点较高的是
,这两种酸中沸点较高的是______ ,原因是_________________________________________ 。
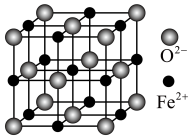
(5)立方 晶体的晶胞结构如图所示,其晶胞边长为
晶体的晶胞结构如图所示,其晶胞边长为 ,列式表示
,列式表示 晶体的密度:
晶体的密度:______  (用含
(用含 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
(1)基态
 的价电子排布图为
的价电子排布图为(2)某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图所示,从该结构片段分析可知该物质的化学式为

(3)有机铁肥三硝酸六尿素合铁(Ⅲ)的化学式为
 。尿素分子中C原子的杂化方式是
。尿素分子中C原子的杂化方式是 中“
中“ ”与
”与 (Ⅲ)之间的作用力是
(Ⅲ)之间的作用力是 的空间构型为
的空间构型为(4)
 可用
可用 检验,
检验, 对应的酸有两种,分别为硫氰酸
对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸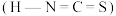 ,这两种酸中沸点较高的是
,这两种酸中沸点较高的是(5)立方
 晶体的晶胞结构如图所示,其晶胞边长为
晶体的晶胞结构如图所示,其晶胞边长为 ,列式表示
,列式表示 晶体的密度:
晶体的密度: (用含
(用含 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】回答下列问题
(1)铁元素在元素周期表中的位置为___________ ,其形成的离子常见的有 和
和 ,基态
,基态 的价电子的排布式为
的价电子的排布式为___________ ,相同条件下, 比
比 稳定,原因是
稳定,原因是___________ 。
(2)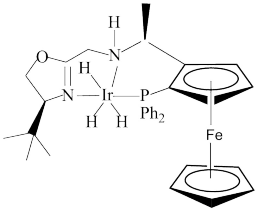 一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中
一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中 为苯基,
为苯基, 为铱元素。该结构中电负性最大的元素为
为铱元素。该结构中电负性最大的元素为___________ (填元素符号,下同),分子中第二周期元素的第一电离能由大到小的顺序为___________ ,分子中不含有的化学键类型是___________ (填标号)。
A.离子键B.配位键C.极性共价键D.非极性共价键E. 键、
键、 键
键
(3) 与
与 位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是___________
(1)铁元素在元素周期表中的位置为
 和
和 ,基态
,基态 的价电子的排布式为
的价电子的排布式为 比
比 稳定,原因是
稳定,原因是(2)
 一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中
一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中 为苯基,
为苯基, 为铱元素。该结构中电负性最大的元素为
为铱元素。该结构中电负性最大的元素为A.离子键B.配位键C.极性共价键D.非极性共价键E.
 键、
键、 键
键(3)
 与
与 位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
您最近一年使用:0次
【推荐1】Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,Cl元素的原子核外有___ 种不同运动状态的电子;有___ 种不同能级的电子,基态Fe3+的电子排布式为___ 。
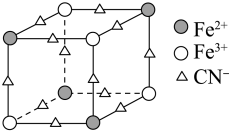
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是___ ;K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为___ 。
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图: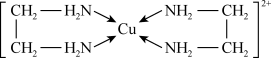 ,该配离子中含有的化学键类型有
,该配离子中含有的化学键类型有___ (填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有___ 个σ键,C原子的杂化方式为___ 。
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。则铜原子的直径约为___ pm。
(1)FeCl3是一种常用的净水剂,Cl元素的原子核外有
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是
 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
 ,该配离子中含有的化学键类型有
,该配离子中含有的化学键类型有a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。则铜原子的直径约为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具一般。叠氨化物和块经合成抗真菌药物三唑是点击化学的重要应用,反应示例如下:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2)C、N、Cu的电负性由大到小的顺序为_______ 。
(3)分子乙中存在5中心6电子的大 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是_______ (填对应原子的序号)。
(4)分子中碳碳三键的活泼性:甲_______ 丙(填“>”“=”“<”),理由是_______ (从分子的结构角度分析)。
(5)丁形成的晶体中不存在的微粒间作用力有_______ 。
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中, 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。 的配位数为
的配位数为_______ 。
②由 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为_______ 。
 +CH3CH2N3
+CH3CH2N3

 +CH3CH2N3→
+CH3CH2N3→
(1)
 的核外电子排布式为
的核外电子排布式为(2)C、N、Cu的电负性由大到小的顺序为
(3)分子乙中存在5中心6电子的大
 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是(4)分子中碳碳三键的活泼性:甲
(5)丁形成的晶体中不存在的微粒间作用力有
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中,
 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。
 的配位数为
的配位数为②由
 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某小组利用如图甲所示装置制备并收集 (夹持装置略去)。
(夹持装置略去)。

已知:Ⅰ.高温时能与 反应,极易水解,能溶于
反应,极易水解,能溶于 ;
;
Ⅱ.物质的熔沸点如表:
(1)加热管式炉前需先通入 的目的是
的目的是___________ ,管式炉加热至900℃时,瓷舟中会生成 、
、 和一种有毒的气态氧化物,并发生副反应生成少量
和一种有毒的气态氧化物,并发生副反应生成少量 ,写出主反应生成
,写出主反应生成 的化学方程式
的化学方程式___________ 。
(2)为除去 中的
中的 应调节控温箱的温度范围为
应调节控温箱的温度范围为___________ ℃。
(3)碱石灰的作用是___________ ,该装置的缺陷是___________ 。
(4)已知 在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原
在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原 制取
制取 :
: 。
。
①基态Ti原子的电子排布式为___________ 。
②反应中涉及的元素第一电离能最大的是___________ , 中化学键类型为
中化学键类型为___________ 。
③ 是一种优良的颜料,其晶胞结构如图。
是一种优良的颜料,其晶胞结构如图。

则黑球代表___________ (填“Ti”或“O”)。该晶体的密度为___________  (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 (夹持装置略去)。
(夹持装置略去)。
已知:Ⅰ.高温时能与
 反应,极易水解,能溶于
反应,极易水解,能溶于 ;
;Ⅱ.物质的熔沸点如表:
| 物质 |  |  |  |
| 熔点℃ | -23.2 | 306 | -23 |
| 沸点℃ | 136.4 | 315 | 76.8 |
(1)加热管式炉前需先通入
 的目的是
的目的是 、
、 和一种有毒的气态氧化物,并发生副反应生成少量
和一种有毒的气态氧化物,并发生副反应生成少量 ,写出主反应生成
,写出主反应生成 的化学方程式
的化学方程式(2)为除去
 中的
中的 应调节控温箱的温度范围为
应调节控温箱的温度范围为(3)碱石灰的作用是
(4)已知
 在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原
在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原 制取
制取 :
: 。
。①基态Ti原子的电子排布式为
②反应中涉及的元素第一电离能最大的是
 中化学键类型为
中化学键类型为③
 是一种优良的颜料,其晶胞结构如图。
是一种优良的颜料,其晶胞结构如图。
则黑球代表
 (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次



