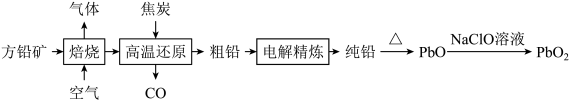
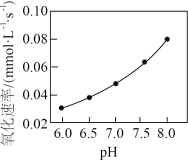
实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表示为
,其实验过程可表示为
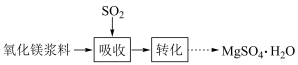
(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成
气体,生成 ,反应为
,反应为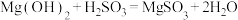 ,其平衡常数K与
,其平衡常数K与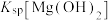 、
、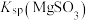 、
、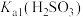 、
、 、
、 的代数关系式为
的代数关系式为
__________ 。
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收 效率,说明原因
效率,说明原因__________ 。
②写出一种能提高氧化镁浆料吸收 效率的操作
效率的操作__________ 。
(3)在负载钴的分子筛催化剂作用下 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为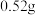 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以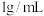 计。
计。
①计算19℃时,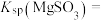
__________ 。
②写出 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为__________ 。
③金属钴在周期表中的位置是__________ 。钴原子价电子排布式为__________ 。
(4)在其他条件相同时,浆料中 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在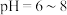 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是__________ 。
 ,其实验过程可表示为
,其实验过程可表示为
(1)在搅拌下向氧化镁浆料中匀速缓慢通入
 气体,生成
气体,生成 ,反应为
,反应为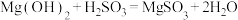 ,其平衡常数K与
,其平衡常数K与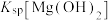 、
、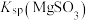 、
、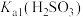 、
、 、
、 的代数关系式为
的代数关系式为
(2)①水浴加热氧化镁浆料,不一定能提高氧化镁浆料吸收
 效率,说明原因
效率,说明原因②写出一种能提高氧化镁浆料吸收
 效率的操作
效率的操作(3)在负载钴的分子筛催化剂作用下
 被
被 氧化为
氧化为 。已知
。已知 的溶解度为
的溶解度为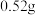 (19℃),若
(19℃),若 饱和溶液的密度以
饱和溶液的密度以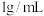 计。
计。①计算19℃时,
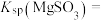
②写出
 氧化溶液中
氧化溶液中 的离子方程式为
的离子方程式为③金属钴在周期表中的位置是
(4)在其他条件相同时,浆料中
 被
被 氧化的速率随pH的变化如图所示。在
氧化的速率随pH的变化如图所示。在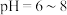 范围内,pH增大,浆料中
范围内,pH增大,浆料中 的氧化速率增大,其主要原因是
的氧化速率增大,其主要原因是
更新时间:2024-02-26 16:09:53
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】铈(Ce)的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
(1) 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有_______ (填序号)。
a. b.
b. c.
c. d.
d.
(2) 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为_______ 。
(3)“氧化焙烧”后, 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:_______ 。
(4)实验室进行操作①所需的玻璃仪器有_______ 。
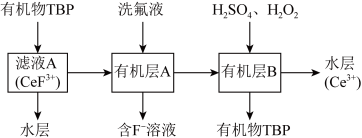
(5)“系列操作”包含下图几个过程: 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应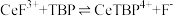 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是_______ 。
(6)已知25℃时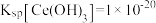 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于_______ 。
(7) 立方晶胞结构如图所示。
立方晶胞结构如图所示。_______ 。
 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图: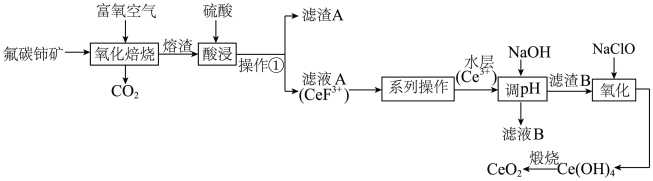
(1)
 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有a.
 b.
b. c.
c. d.
d.
(2)
 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为(3)“氧化焙烧”后,
 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:(4)实验室进行操作①所需的玻璃仪器有
(5)“系列操作”包含下图几个过程:
 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应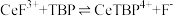 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是(6)已知25℃时
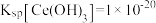 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于(7)
 立方晶胞结构如图所示。
立方晶胞结构如图所示。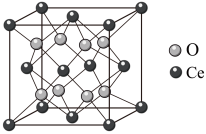
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】一种利用废镍催化剂(含金属Ni、Al、Fe及其氧化物,还含有少量的油脂)制备NiSO4•6H2O的工艺流程如下:
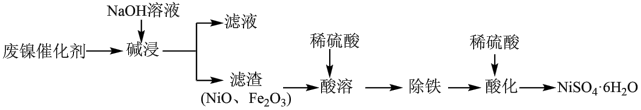
已知:常温下,Ksp[Fe(OH)3]=1.0×10-38、Ksp[Ni(OH)2]=2.0×10-15。
回答下列问题:
(1)“碱浸”的目的是_______ ;为提高“碱浸”效率,可采取的措施有_______ (任写两点)。
(2)“碱浸”时有气体生成,则该气体为_______ (填化学式),写出生成此气体的化学方程式:_______ 。
(3)“酸溶”时需要用到2mol/L的稀硫酸,实验室利用浓硫酸配制实验用的稀硫酸需要用到的玻璃仪器除了容量瓶、量筒、烧杯外,还有_______ 。
(4)常温下,若“酸溶”后溶液中c(Ni2+)=0.2mol/L,则“调节溶液的pH”时应控制的pH范围是_______ 。[c(Fe3+)=1.0×10-5mol/L时,Fe3+沉淀完全]
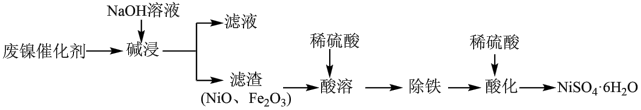
已知:常温下,Ksp[Fe(OH)3]=1.0×10-38、Ksp[Ni(OH)2]=2.0×10-15。
回答下列问题:
(1)“碱浸”的目的是
(2)“碱浸”时有气体生成,则该气体为
(3)“酸溶”时需要用到2mol/L的稀硫酸,实验室利用浓硫酸配制实验用的稀硫酸需要用到的玻璃仪器除了容量瓶、量筒、烧杯外,还有
(4)常温下,若“酸溶”后溶液中c(Ni2+)=0.2mol/L,则“调节溶液的pH”时应控制的pH范围是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】铜及其化合物在工业上有许多用途。回答下列问题:
(1)某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:

①“浸取”反应中氧化剂的化学式为___________ ;若“浸取”反应中得到一种单质,则滤渣Ⅰ的成分为 MnO2和___________ (写化学式)。
②“除铁”这一步反应在25℃进行,加入的试剂 A 为___________ ,若加A后溶液的pH调为4,溶液中 Fe3+浓度为___________ mol∙L−1。{已知 Ksp[Fe(OH)3]=4.0×10−38}
③写出“沉锰”(除 Mn2+)过程中反应的离子方程式:___________ 。
④滤液Ⅱ经蒸发结晶得到的盐主要是___________ (写化学式)。
(2)如图(a)为某实验小组设计的原电池装置,盐桥内装载的是足量用饱和氯化钾溶液浸泡的琼脂,反应前两电极质量相等,一段时间后,两电极质量相差 25.8 g,则导线中通过了___________ mol 电子。
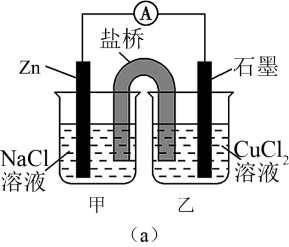
(1)某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:

①“浸取”反应中氧化剂的化学式为
②“除铁”这一步反应在25℃进行,加入的试剂 A 为
③写出“沉锰”(除 Mn2+)过程中反应的离子方程式:
④滤液Ⅱ经蒸发结晶得到的盐主要是
(2)如图(a)为某实验小组设计的原电池装置,盐桥内装载的是足量用饱和氯化钾溶液浸泡的琼脂,反应前两电极质量相等,一段时间后,两电极质量相差 25.8 g,则导线中通过了

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】废物再利用是一种环保行为,可以有效降低环境污染,同时又能达到资源的再利用。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如图:

已知:ⅰ.酸浸液中的金属阳离子有 、
、 、
、 、
、 、
、 等
等
ⅱ. 在水中的溶解度随温度升高而增大
在水中的溶解度随温度升高而增大
回答下列问题:
(1)提高“酸浸”速率的方法有___________ 。(任写一条)
(2)基态Fe原子价层电子的轨道表示式___________ 。Fe的晶胞结构如图所示,已知 表示阿伏加德罗常数的值,若晶胞参数为anm,则Fe晶胞的密度为
表示阿伏加德罗常数的值,若晶胞参数为anm,则Fe晶胞的密度为___________  (用含
(用含 和a的代数式表示)。
和a的代数式表示)。

(3)黄钠铁矾的化学式为 ,“除铁”的离子方程式为
,“除铁”的离子方程式为___________ 。
(4)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是___________ (结合平衡理论解释)。
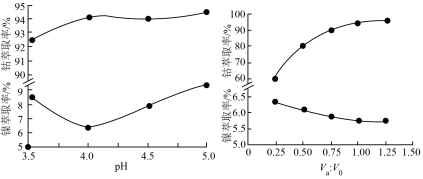
(5)镍、钴萃取率与料液pH、萃取剂体积与料液体积比 的关系曲线如图所示,则“萃取”时应选择的pH和
的关系曲线如图所示,则“萃取”时应选择的pH和 分别为
分别为___________ 、___________ 。
(6)获得 的“一系列操作”是
的“一系列操作”是___________ ,工艺流程中,可循环利用的物质是___________ 。

已知:ⅰ.酸浸液中的金属阳离子有
 、
、 、
、 、
、 、
、 等
等ⅱ.
 在水中的溶解度随温度升高而增大
在水中的溶解度随温度升高而增大回答下列问题:
(1)提高“酸浸”速率的方法有
(2)基态Fe原子价层电子的轨道表示式
 表示阿伏加德罗常数的值,若晶胞参数为anm,则Fe晶胞的密度为
表示阿伏加德罗常数的值,若晶胞参数为anm,则Fe晶胞的密度为 (用含
(用含 和a的代数式表示)。
和a的代数式表示)。
(3)黄钠铁矾的化学式为
 ,“除铁”的离子方程式为
,“除铁”的离子方程式为(4)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(5)镍、钴萃取率与料液pH、萃取剂体积与料液体积比
 的关系曲线如图所示,则“萃取”时应选择的pH和
的关系曲线如图所示,则“萃取”时应选择的pH和 分别为
分别为
(6)获得
 的“一系列操作”是
的“一系列操作”是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】锰的单质及其化合物的用途非常广泛 回答下列问题:
回答下列问题:
⑴基态锰原子的外围电子排布式为______________________ ,其d轨道中未成对电子数为__________ 。
⑵MnO的熔点(1650℃)比MnS的熔点(1610℃)高原因是_____________________________________ 。
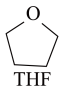
⑶锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
①THF中的元素的电负性从大到小的顺序是__________________ 。
②与Mn2+形成配位键的原子为______ (填元素符号)。
③BH4-的空间构型为_______ ,其中B原子的杂化轨道类型为________ 。
④写出两种与BH4-互为等电子体的分子或离子___________ 。
⑷一种磁性材料的单晶胞结构如图所示。
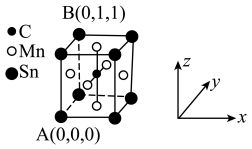
①该晶胞中碳原子的原子坐标为________ 。
②Mn在晶体中的堆积方式为_______ (填“简单立方”“体心立方”或“面心立方最密”)堆积。
③若该晶胞的边长为a pm,NA表示阿伏加 德罗常数的数值,则该晶体密度的表达式为ρ =___________________ g∙cm-3。
 回答下列问题:
回答下列问题:
⑴基态锰原子的外围电子排布式为
⑵MnO的熔点(1650℃)比MnS的熔点(1610℃)高原因是
⑶锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
①THF中的元素的电负性从大到小的顺序是
②与Mn2+形成配位键的原子为
③BH4-的空间构型为
④写出两种与BH4-互为等电子体的分子或离子
⑷一种磁性材料的单晶胞结构如图所示。

①该晶胞中碳原子的原子坐标为
②Mn在晶体中的堆积方式为
③若该晶胞的边长为a pm,NA表示阿伏加 德罗常数的数值,则该晶体密度的表达式为ρ =
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子。
请回答下列问题:
(1)写出下列元素的元素符号:A____ 、C_____ 、E_____ 、F_____ 。
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式____ ,甲为_____ (填“极性”或“非极性”)分子。
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙_______________ ;常温下甲为液态,乙为气态,试解释原因__________________________ 。
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:_________________ 。
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是__________ 。
(6)写出元素F的外围电子排布式_______________________ 。
请回答下列问题:
(1)写出下列元素的元素符号:A
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是
(6)写出元素F的外围电子排布式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】三氯化硼 是一种重要的化工原料。实验室制备
是一种重要的化工原料。实验室制备 的原理为
的原理为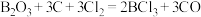 ,某实验小组利用干燥的氯气和下列装置(装置可重复使用,略去夹持装置)制备
,某实验小组利用干燥的氯气和下列装置(装置可重复使用,略去夹持装置)制备 并验证反应中有
并验证反应中有 生成。已知:
生成。已知: 的熔点为
的熔点为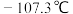 ,沸点为
,沸点为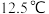 ,遇水水解生成
,遇水水解生成 和
和 ,请回答下列问题:
,请回答下列问题:
实验:制备 并验证产物
并验证产物
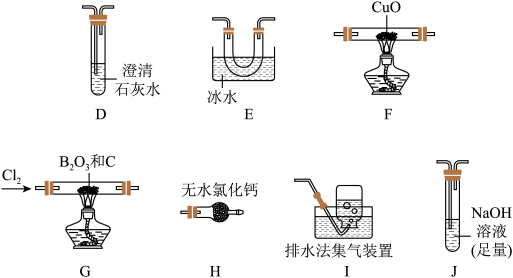
(1)该实验装置中合理的连接顺序为G→_______ →F→D→I。其中装置E的作用是_______ 。
(2)装置J中发生反应的化学方程式为_______ 。
 是一种重要的化工原料。实验室制备
是一种重要的化工原料。实验室制备 的原理为
的原理为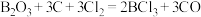 ,某实验小组利用干燥的氯气和下列装置(装置可重复使用,略去夹持装置)制备
,某实验小组利用干燥的氯气和下列装置(装置可重复使用,略去夹持装置)制备 并验证反应中有
并验证反应中有 生成。已知:
生成。已知: 的熔点为
的熔点为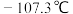 ,沸点为
,沸点为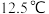 ,遇水水解生成
,遇水水解生成 和
和 ,请回答下列问题:
,请回答下列问题:实验:制备
 并验证产物
并验证产物

(1)该实验装置中合理的连接顺序为G→
(2)装置J中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某小组利用如图所示装置制备少量NCl3。已知:NCl3可由Cl2与NH4Cl溶液在适宜温度下反应生成。常温下,NCl3为黄色油状液体,熔点为-40℃,沸点为71℃;极易爆炸,自然爆炸点为95℃。
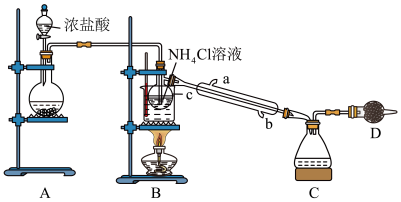
回答下列问题:
(1)装置A中圆底烧瓶内所盛放的固体是___ (填化学式)。
(2)装置B中仪器C的名称是___ ,实验过程中该仪器内发生反应的化学方程式为___ 。
(3)装置B的烧杯中应控制水浴加热的温度范围为____ 。
(4)装置D中所盛放的试剂不能为下列选项中的___ (填字母)。
a.生石灰 b.NaOH固体 C.碱石灰 d.无水CaCl2
(5)查阅资料可知,电解pH<5的NH4Cl溶液也可制得NCl3,则电解池中产生NCl3的电极为___ (填“阴极’’或“阳极’’),该电极的电极反应式为___ 。

回答下列问题:
(1)装置A中圆底烧瓶内所盛放的固体是
(2)装置B中仪器C的名称是
(3)装置B的烧杯中应控制水浴加热的温度范围为
(4)装置D中所盛放的试剂不能为下列选项中的
a.生石灰 b.NaOH固体 C.碱石灰 d.无水CaCl2
(5)查阅资料可知,电解pH<5的NH4Cl溶液也可制得NCl3,则电解池中产生NCl3的电极为
您最近一年使用:0次