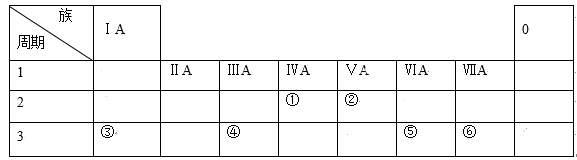
如图是现行元素周期表的一部分,请回答:
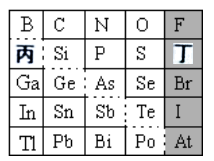
(1)元素Se在周期表中的位置为___________ 。
(2)下列说法正确的是___________ 。
A.丙位于周期表中从左到右数第13列
B.Bi的最高价氧化物的化学式为Bi2O5
C.丁所形成的含氧酸是强酸
D.C、N、O三种元素的最高正价等于其所在族的族序数
(3)①阴影部分元素所形成的氢化物中热稳定性最高的是___________ (填化学式)。请从原子结构的角度解释其原因:___________ 。
②可在图中分界线(虚线部分)附近寻找___________ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.新品种农药
(4)Pb能形成多种氧化物,如碱性氧化物PbO,酸性氧化物PbO2,还有类似于Fe3O4中铁元素价态特征(有两种价态)的Pb3O4,Pb3O4能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出该反应的化学方程式___________ 。

(1)元素Se在周期表中的位置为
(2)下列说法正确的是
A.丙位于周期表中从左到右数第13列
B.Bi的最高价氧化物的化学式为Bi2O5
C.丁所形成的含氧酸是强酸
D.C、N、O三种元素的最高正价等于其所在族的族序数
(3)①阴影部分元素所形成的氢化物中热稳定性最高的是
②可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.新品种农药
(4)Pb能形成多种氧化物,如碱性氧化物PbO,酸性氧化物PbO2,还有类似于Fe3O4中铁元素价态特征(有两种价态)的Pb3O4,Pb3O4能与硝酸发生非氧化还原反应生成一种盐和一种铅的氧化物,写出该反应的化学方程式
20-21高一上·浙江台州·期末 查看更多[7]
(已下线)人教必修第一册第4章第2节第2课时元素周期表和元素周期律的应用(课后)浙江省瑞安中学2020-2021学年高一下学期期初考试化学试题(已下线)【浙江新东方】在线化学51高一上(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)浙江省台州市2020-2021学年高一上学期期末考试化学试题浙江省台州市2020-2021学年高一上学期期末质量评估化学试题
更新时间:2021-01-26 22:41:46
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。
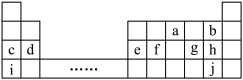
(1)元素a、b、c对应原子半径由大到小的顺序是_______ (用对应元素符号表示,下同)。
元素a、b、c对应简单离子中,半径最小的是_______ (用对应离子符号)。
(2)写出由上述元素形成的最高价氧化物对应水化物酸性最强的酸和最高价氧化物对应水化物碱性最强的碱反应的化学方程式:_______ 。
(3)上述元素中最高正化合价与最低负化合价绝对值相等的元素是_______ 。
(4)g的简单氢化物的电子式为_______ 。
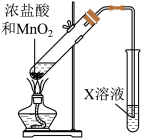
(5)用如图所示装置可以比较h和j的单质氧化性强弱,则X可以是_______ (填化学式)。

(1)元素a、b、c对应原子半径由大到小的顺序是
元素a、b、c对应简单离子中,半径最小的是
(2)写出由上述元素形成的最高价氧化物对应水化物酸性最强的酸和最高价氧化物对应水化物碱性最强的碱反应的化学方程式:
(3)上述元素中最高正化合价与最低负化合价绝对值相等的元素是
(4)g的简单氢化物的电子式为
(5)用如图所示装置可以比较h和j的单质氧化性强弱,则X可以是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】153年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。下图为现代元素周期表的一部分,请回答下列问题:(以下问题均用相应的化学符号表达)
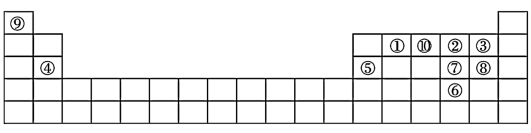
(1)在这10种元素中,非金属性最强的元素对应的单质与水反应的化学方程式:_______ ;③④⑦⑧的简单离子半径由大到小依次为_______ 。
(2)元素①的简单气态氢化物的电子式为_______ ;用电子式表示②与⑨形成 化合物的过程
化合物的过程_______ 。
(3)HSCN是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓HSCN溶液和软锰矿在加热条件下的离子方程式:_______ ;反应中断裂的化学键类型有:_______ 、_______ 。
(4)比较元素⑦⑧形成的气态氢化物的稳定性:_______ >_______ (用化学式表示)。
(5)在含有⑨、④、⑤简单阳离子的100 mL溶液中,逐滴滴加 的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:_______ 。
②a点的数值为:_______ mL。

(1)在这10种元素中,非金属性最强的元素对应的单质与水反应的化学方程式:
(2)元素①的简单气态氢化物的电子式为
 化合物的过程
化合物的过程(3)HSCN是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓HSCN溶液和软锰矿在加热条件下的离子方程式:
(4)比较元素⑦⑧形成的气态氢化物的稳定性:
(5)在含有⑨、④、⑤简单阳离子的100 mL溶液中,逐滴滴加
 的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如图所示是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:(问题中所写的均为字母,回答时涉及字母的均用元素符号作答)
(1)J的元素符号为___________ ,M在周期表中位于___________ 区。
(2)写出基态A原子核外电子的轨道表示式:___________ 。
(3)写出I元素基态原子的价层电子排布式:___________ 。
(4)N元素在周期表中的位置是___________ 。
(5)A、B、G、H的原子半径由大到小的顺序是___________ ;A、B、C、D的第一电离能由大到小的顺序是___________ 。
| A | B | C | D | E | |||||||||||||
| F | G | H | |||||||||||||||
| L | I | J | M | K | N | ||||||||||||
| O |
(1)J的元素符号为
(2)写出基态A原子核外电子的轨道表示式:
(3)写出I元素基态原子的价层电子排布式:
(4)N元素在周期表中的位置是
(5)A、B、G、H的原子半径由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】三位科学家“发现和合成量子点”获得2023年诺贝尔化学奖。量子点又称为半导体荧光纳米晶,主要是由ⅡA-ⅥA族元素(如CdS、CdSe、ZnSe等)和ⅢA-ⅤA族元素(如GaN、InP、InAs等)组成的纳米颗粒,元素周期表从此有了第三个维度。元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。下表列出了a~h8种元素在周期表的位置,请回答下列问题:
(1)某量子点含有e元素。e原子结构示意图为:___________ 。
(2)GaN量子点中的Ga与d同族。Ga与d两种元素最高价氧化物对应的水化物碱性较强的是___________ (填化学式)。
(3)CdSe量子点中的Se是34号元素,在周期表中的位置是___________ ;Se与f的简单氢化物稳定性较弱的是___________ (填化学式)。
(4)单质c在单质b中燃烧火焰呈___________ 色,所得产物的电子式为___________ ,该产物与a的最高价氧化物反应的化学方程式为___________ 。
(5)写出一条能证明h的金属性强于c的实验事实___________ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | |||
| 4 | h | |||||||
(2)GaN量子点中的Ga与d同族。Ga与d两种元素最高价氧化物对应的水化物碱性较强的是
(3)CdSe量子点中的Se是34号元素,在周期表中的位置是
(4)单质c在单质b中燃烧火焰呈
(5)写出一条能证明h的金属性强于c的实验事实
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表是元素周期律的具体表现,是学习和研究化学的重要工具.下图是元素周期表的一部分:
请完成下列填空:
(1)元素①的简单气态氢化物的空间构型是_____________ 。
(2)元素②、③、④的简单离子半径由大到小的顺序为_____________ (用离子符号表示)。
(3) 元素在周期表中的位置是
元素在周期表中的位置是____ ,最后一行元素的基态原子中只有1个未成对电子的是_____ (填元素名称)。
(4)元素④、⑤非金属性更强的是________ (填元素符号),请从原子结构的角度解释:_________ 。并写出一个证明它们非金属性强弱的化学反应方程式________________________ 。
(5)表中第一电离能最大的元素是_____________ ,理由是__________________________ 。
| ① | ② | ||||
| ③ | ④ | ⑤ | ⑥ | ||
 |  |  |  |  |
(1)元素①的简单气态氢化物的空间构型是
(2)元素②、③、④的简单离子半径由大到小的顺序为
(3)
 元素在周期表中的位置是
元素在周期表中的位置是(4)元素④、⑤非金属性更强的是
(5)表中第一电离能最大的元素是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表在学习、研究和生产实践中有很重要的作用。下表显示了元素周期表中的短周期,①~⑤代表5种元素。
(1)②在元素周期表中的位置是___________ 。
(2)①分别与④、⑤形成的化合物中,稳定性强的是___________ (用化学式表示)。
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是___________ 。
(4)用原子结构解释④和⑤非金属性强弱的原因:___________ 。
(5)元素硒(Se)的原子结构示意图为 。下列推断正确的是___________(填字母)。
。下列推断正确的是___________(填字母)。
| ① | ||||||||
| ② | ||||||||
| ③ | ④ | ⑤ | ||||||
(2)①分别与④、⑤形成的化合物中,稳定性强的是
(3)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是
(4)用原子结构解释④和⑤非金属性强弱的原因:
(5)元素硒(Se)的原子结构示意图为
 。下列推断正确的是___________(填字母)。
。下列推断正确的是___________(填字母)。| A.Se位于第4周期、与④同主族 | B.Se的最低负化合价为 |
C. 具有还原性 具有还原性 | D. 的酸性强于 的酸性强于 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请回答有关问题:
(1)画出①的原子结构示意图:_______ , ⑩的元素名称:_______ 。
(2)③④⑤原子半径由大到小的顺序是_______ (填元素符号)
(3)表中最活泼的金属是_______ ,非金属性最强的元素是_______ ;(填写元素符号)
(4)表中能形成两性氢氧化物的元素是_______ ,写出该元素的氢氧化物与⑨的最高价氧化物对应水化物反应的离子方程式:_______ 。
(5)用电子式表示③与⑥的化合物的形成过程:_______ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ⑥ | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)③④⑤原子半径由大到小的顺序是
(3)表中最活泼的金属是
(4)表中能形成两性氢氧化物的元素是
(5)用电子式表示③与⑥的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表一部分,针对表中的①~⑧种元素,请按要求填写下列空白:
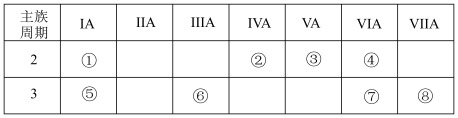
(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:_______ 。
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序_______ (用离子符号表示)。
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式_______ 。
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式_____ 。
(5)用电子式来表示⑤与⑦组成化合物的形成过程_______ 。

(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式
(5)用电子式来表示⑤与⑦组成化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题.
(1)可作半导体材料的元素是 ______ (填元素符号);气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐的元素是 _____ (填名称);
(2)第三周期中离子半径最小的是___________ (填离子符号);
(3)①~⑨的最高价氧化物的水化物中:酸性最强的是__________ (填化学式);碱性最强的是________ (填化学式)。
(4)比较③、⑧最简单氢化物的稳定性:____________________ (用化学式表示)。
(5)写出②形成单质电子式________ 。
(6)⑤和⑨形成的化合物中所含化学键类型为________ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期中离子半径最小的是
(3)①~⑨的最高价氧化物的水化物中:酸性最强的是
(4)比较③、⑧最简单氢化物的稳定性:
(5)写出②形成单质电子式
(6)⑤和⑨形成的化合物中所含化学键类型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
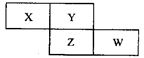
I.若Y元素原子的最外层电子数是电子层数的3倍
(1) W的原子结构示意图为___________________ 。
(2)Z在周期表中的位置____________________ 。
(3)一定条件下,X的最低价氢化物与X的某种氧化物按2:3物质的量比混合恰好反应生成X 单质和水,该氧化物的化学式为_____________ 。
(4)写出铜片置于Z的最高价氧化物水化物稀溶液,没有明显变化。加热,依然如故。再通入空气,溶液就逐渐变蓝,使溶液变蓝的反应的离子方程式:_______ 。
Ⅱ.若Y和Z的核外电子数之和为20。
(5)相对分子质量为16的Y的氢化物电子式为_______________________ 。
(6)写出单质Y和浓硝酸反应的化学方程式:________________________ 。
(7)写出工业制备Z的过程中发生的第一个反应的化学方程式__________ 。

I.若Y元素原子的最外层电子数是电子层数的3倍
(1) W的原子结构示意图为
(2)Z在周期表中的位置
(3)一定条件下,X的最低价氢化物与X的某种氧化物按2:3物质的量比混合恰好反应生成X 单质和水,该氧化物的化学式为
(4)写出铜片置于Z的最高价氧化物水化物稀溶液,没有明显变化。加热,依然如故。再通入空气,溶液就逐渐变蓝,使溶液变蓝的反应的离子方程式:
Ⅱ.若Y和Z的核外电子数之和为20。
(5)相对分子质量为16的Y的氢化物电子式为
(6)写出单质Y和浓硝酸反应的化学方程式:
(7)写出工业制备Z的过程中发生的第一个反应的化学方程式
您最近一年使用:0次