如图所示是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:(问题中所写的均为字母,回答时涉及字母的均用元素符号作答)
(1)J的元素符号为___________ ,M在周期表中位于___________ 区。
(2)写出基态A原子核外电子的轨道表示式:___________ 。
(3)写出I元素基态原子的价层电子排布式:___________ 。
(4)N元素在周期表中的位置是___________ 。
(5)A、B、G、H的原子半径由大到小的顺序是___________ ;A、B、C、D的第一电离能由大到小的顺序是___________ 。
| A | B | C | D | E | |||||||||||||
| F | G | H | |||||||||||||||
| L | I | J | M | K | N | ||||||||||||
| O |
(1)J的元素符号为
(2)写出基态A原子核外电子的轨道表示式:
(3)写出I元素基态原子的价层电子排布式:
(4)N元素在周期表中的位置是
(5)A、B、G、H的原子半径由大到小的顺序是
更新时间:2023-05-07 08:13:02
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分。根据表中元素,用化学用语填空:
(1)上表编号的元素中,属于金属元素的是_______ ,最高价含氧酸酸性最强的元素是______ ,非金属性最强的元素是_______ ,原子半径最小的元素是______ ,单质可制作芯片的元素是______ ,元素⑦的原子结构示意图是_______ 。
(2)元素②的单质的电子式为_______ ;元素③的最简单氢化物的结构式为______ 。
(3)元素③和元素⑦的最简单氢化物的沸点由高到低的顺序是______ ;
(4)写出一个化学反应方程式,证明③和④的单质非金属性强弱____________________ ;
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上表编号的元素中,属于金属元素的是
(2)元素②的单质的电子式为
(3)元素③和元素⑦的最简单氢化物的沸点由高到低的顺序是
(4)写出一个化学反应方程式,证明③和④的单质非金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】如图是元素周期表的一部分,其中每个字母代表对应的一种元素。
请按要求回答下列问题:
(1)写出D与E按 的原子个数比形成的化合物与水反应的离子方程式:
的原子个数比形成的化合物与水反应的离子方程式:___________ ,F的原子结构示意图为___________ 。
(2)B在周期表中的位置为___________ ,A、C、F三种元素形成的化合物CA4F中阳离子的检验方法为:取少量待测液,___________ 。
(3)化合物甲由A、B、D、E四种元素组成,俗称小苏打,乙由A、D、E三种元素组成,则甲、乙反应的离子方程式为___________ 。
(4)C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)。
(5)B的非金属性___________ 于C(填“强”或“弱”),并用化学方程式证明上述结论___________ 。
| A | |||||||||||||
| B | C | D | |||||||||||
| E | F |
(1)写出D与E按
 的原子个数比形成的化合物与水反应的离子方程式:
的原子个数比形成的化合物与水反应的离子方程式:(2)B在周期表中的位置为
(3)化合物甲由A、B、D、E四种元素组成,俗称小苏打,乙由A、D、E三种元素组成,则甲、乙反应的离子方程式为
(4)C、D、E的原子半径由大到小的顺序是
(5)B的非金属性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
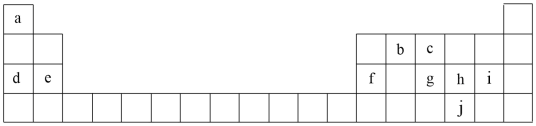
(1)元素c代表的元素是(写元素符号)___________ 请写出元素e在元素周期表中所在的位置___________
(2)请画出元素f的简单离子结构示意图___________ 。请写出单质f与d的最高价氧化物对应水化物的离子反应方程式___________ 。
(3)元素a和b能构成最简单的有机化合物(用结构式表示)___________ ,其分子的空间结构为___________ 。
(4)元素h的最高价氧化物对应的水化物呈___________ (酸性、中性或碱性);请写出元素h的最高价氧化物对应的水化物与单质b发生的氧化还原反应方程式___________ 。

(1)元素c代表的元素是(写元素符号)
(2)请画出元素f的简单离子结构示意图
(3)元素a和b能构成最简单的有机化合物(用结构式表示)
(4)元素h的最高价氧化物对应的水化物呈
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】根据下图短周期主族元素的原子序数和化合价的关系推断元素种类,用化学符号回答下列问题:
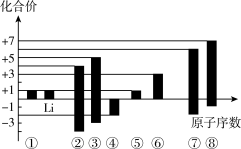
(1)写出元素③的原子结构示意图_______ ;元素⑤在周期表中的位置是_______ 。
(2)④、⑥、⑦、⑧四种元素的简单离子的半径最大的是_______ 。
(3)元素②、⑦、⑧的最高价氧化物对应的水化物中酸性最强的是_______ ;元素⑦、⑧对应的简单氢化物中,稳定性较强的是_______ ,原因是_______ 。
(4)元素④、⑦的简单氢化物中沸点较高的是_______ (写结构式)。
(5)由①和④两种元素组成原子个数比为1:1的化合物的电子式为_______ ;请用电子式表示由④和⑤两种元素组成原子个数比为1:2的化合物的形成过程:_______ 。
(6)元素⑤和⑥的最高价氧化物对应的水化物能相互反应,请写出该反应的离子方程式:_______ ;元素②的一种链状气态氢化物为18电子分子,请写出其结构简式:_______ 。

(1)写出元素③的原子结构示意图
(2)④、⑥、⑦、⑧四种元素的简单离子的半径最大的是
(3)元素②、⑦、⑧的最高价氧化物对应的水化物中酸性最强的是
(4)元素④、⑦的简单氢化物中沸点较高的是
(5)由①和④两种元素组成原子个数比为1:1的化合物的电子式为
(6)元素⑤和⑥的最高价氧化物对应的水化物能相互反应,请写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分。
请回答下列问题:
(1)写出④的元素符号:_______ 。
(2)①~⑥六种元素的单质相比较,金属性最强的是_______ (填元素符号)。
(3)元素①的最高价氧化物对应的水化物的化学式是_______ 。
(4)两种元素的原子半径大小:③_______ ⑥(填“>”或“<”)。
(5)硫的原子结构示意图:_______ 。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | ① | ② | Ne | |||||
| 3 | ③ | ④ | ⑤ | ⑥ | Ar |
(1)写出④的元素符号:
(2)①~⑥六种元素的单质相比较,金属性最强的是
(3)元素①的最高价氧化物对应的水化物的化学式是
(4)两种元素的原子半径大小:③
(5)硫的原子结构示意图:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】学习了元素周期律可以把元素化合物知识系统地归纳起来,可以从物质的类别和元素的化合价两个方面在二维空间构造知识体系。例如:如图为S元素的价类二维图。回答下列问题:___________ ;图中所给出的物质属于含有共价键的离子化合物的是___________ (填化学式)。
(2)为验证 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
(3)Y与氢氧化钠溶液反应的离子方程式为___________ 。
(4) 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为___________ 。
(5)木炭与浓硫酸反应的化学方程式为___________ ,验证该反应的气体产物所需溶液依次为___________ 。
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液

(2)为验证
 的相关性质,将
的相关性质,将 通入
通入 溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。
溶液中无明显现象,若将其取出分成三份,分别滴加下列溶液后,都出现了沉淀,填写表中沉淀的化学式。| 滴加的溶液 | 氯水 | 氨水 |  溶液 溶液 |
| 沉淀的化学式 |
(3)Y与氢氧化钠溶液反应的离子方程式为
(4)
 中各元素原子半径由大到小的顺序为
中各元素原子半径由大到小的顺序为(5)木炭与浓硫酸反应的化学方程式为
A.品红溶液、酸性高锰酸钾、澄清石灰水
B.澄清石灰水、澄清石灰水、品红溶液
C.澄清石灰水、氢氧化钠溶液、品红溶液
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)第一电离能比较Mg_______ Al,并解释原因 _______ 。
(2)基态V原子价电子排布图_______ 。
(3)C、N、O元素的性质由大到小的顺序为:电负性_______ ;第一电离能_______ 。
(4)键角比较:CH 、CH
、CH
_______ ;CO2、SO2、H2O _______
(5)水结冰后,水分子之间最大程度的形成氢键,该氢键可表示为_______ ,冰分子和氢键的物质的量之比为_______ ,当温度有0℃升高到4℃时,水的密度逐渐 _______ (填“增大”、“减小”)。
(6)比较下列物质的熔沸点,按由大到小的顺序写:H2O、SO2、NaCl、SiO2_______ 。
(7)某元素基态原子是第四周期未成对电子最多的,该元素符号是_______ 。
(8)根据等电子体原理判断N 立体构型为
立体构型为_______ 。
(9)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,ClO 中心原子的杂化形式为
中心原子的杂化形式为_______ 。
(1)第一电离能比较Mg
(2)基态V原子价电子排布图
(3)C、N、O元素的性质由大到小的顺序为:电负性
(4)键角比较:CH
 、CH
、CH
(5)水结冰后,水分子之间最大程度的形成氢键,该氢键可表示为
(6)比较下列物质的熔沸点,按由大到小的顺序写:H2O、SO2、NaCl、SiO2
(7)某元素基态原子是第四周期未成对电子最多的,该元素符号是
(8)根据等电子体原理判断N
 立体构型为
立体构型为(9)氯气与熟石灰反应制漂白粉时会生成副产物Ca(ClO3)2,ClO
 中心原子的杂化形式为
中心原子的杂化形式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】如图所示是s能级和p能级的原子轨道图:
(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(2)元素X的基态原子最外层电子排布式为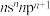 ,其p电子云在空间有3个互相
,其p电子云在空间有3个互相___________ (填“垂直”或“平行”)的伸展方向;元素X的名称是___________ ,它的最低价氢化物的电子式是___________ 。
(3)元素Y的基态原子最外层电子排布式为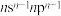 ,那么Y的元素符号应为
,那么Y的元素符号应为___________ ,其基态原子的轨道表示式为___________ 。

(1)s电子的原子轨道呈
(2)元素X的基态原子最外层电子排布式为
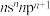 ,其p电子云在空间有3个互相
,其p电子云在空间有3个互相(3)元素Y的基态原子最外层电子排布式为
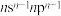 ,那么Y的元素符号应为
,那么Y的元素符号应为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】短周期主族元素X、Y、Z、W、M、N的原子序数依次增大, 核外电子只有1种运动状态,
核外电子只有1种运动状态, 的
的 轨道均含有2个未成对电子,
轨道均含有2个未成对电子, 均是与
均是与 不同主族的金属元素。回答下列问题:
不同主族的金属元素。回答下列问题:
(1)基态 原子有
原子有___________ 种不同空间运动状态的电子,价层电子排布式为___________ 。
(2)基态 原子中,核外电子占据的最高能层的符号是
原子中,核外电子占据的最高能层的符号是___________ ,该金属单质与 溶液反应的离子方程式为
溶液反应的离子方程式为______________________ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的Z原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的Z原子,其价层电子自旋磁量子数的代数和为___________ 。
(4) 的氢化物沸点
的氢化物沸点___________ (填“一定”或“不一定”)低于 的氢化物的沸点。
的氢化物的沸点。
(5)由X、Y、Z、W共同组成的一种无机含氧酸盐的化学式为___________ ,其阳离子中心原子的价层电子对数为___________ 。
 核外电子只有1种运动状态,
核外电子只有1种运动状态, 的
的 轨道均含有2个未成对电子,
轨道均含有2个未成对电子, 均是与
均是与 不同主族的金属元素。回答下列问题:
不同主族的金属元素。回答下列问题:(1)基态
 原子有
原子有(2)基态
 原子中,核外电子占据的最高能层的符号是
原子中,核外电子占据的最高能层的符号是 溶液反应的离子方程式为
溶液反应的离子方程式为(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的Z原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的Z原子,其价层电子自旋磁量子数的代数和为(4)
 的氢化物沸点
的氢化物沸点 的氢化物的沸点。
的氢化物的沸点。(5)由X、Y、Z、W共同组成的一种无机含氧酸盐的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
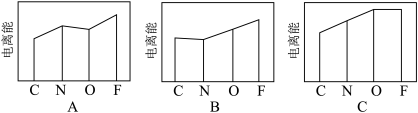
(1)图A、B、C分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同),第一电离能I1的变化图是_______ 。
(2)NE是微电子工业中一种优良的等离子蚀刻气体,NF3分子空间构型为_______ ,NH3的键角约为107°,推测NF3的键角______ 107°(填“>”,“<”或“=”)。
(3)X射线衍射测定等发现,I3AsF6中存在I 离子。I
离子。I 中心原子的杂化方式为
中心原子的杂化方式为_________ 。
(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示。若该立方晶胞参数为apm,NA为阿伏加德罗常数:计算品体的密度为_______ g•cm-3(列出表达式)。[注:1皮米(pm)=1.0×10-12米(m)]

(1)图A、B、C分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同),第一电离能I1的变化图是

(2)NE是微电子工业中一种优良的等离子蚀刻气体,NF3分子空间构型为
(3)X射线衍射测定等发现,I3AsF6中存在I
 离子。I
离子。I 中心原子的杂化方式为
中心原子的杂化方式为(4)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构如图所示。若该立方晶胞参数为apm,NA为阿伏加德罗常数:计算品体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是____ .
A.CO2 B.H3O+ C.CH4 D.[Ag(NH3)2]+
(2)向硫酸铜溶液中滴加过量氨水,观察到的现象是:首先生成蓝色沉淀。继续加氨水,沉淀溶解,得到深蓝色透明溶液。
①请写出上述过程沉淀溶解的离子方程式________________________________ 。再向深蓝色透明溶液中加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为_____________ 。
②根据以上实验,判断NH3和H2O与Cu2+的配位能力:NH3____ H2O(填“>”、“=”或“<”)。
③请写出铜原子的核外电子排布式_________________ 。单质铜及镍都是由________ 键形成的晶体;元素铜与镍的第二电离能分别为ICu=1 958 kJ·mol-1、INi=1 753 kJ·mol-1,ICu>INi的原因是_________________________________ ;
(3)配位化学创始人维尔纳发现,将各为1mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol。已知上述配合物中配离子的配位数均为6。请根据实验事实用配合物的形式写出它们的化学式。
①CoCl3·5NH3________________ ;②CoCl3·4NH3(紫色)__________________ 。
(1)下列粒子中可能存在配位键的是
A.CO2 B.H3O+ C.CH4 D.[Ag(NH3)2]+
(2)向硫酸铜溶液中滴加过量氨水,观察到的现象是:首先生成蓝色沉淀。继续加氨水,沉淀溶解,得到深蓝色透明溶液。
①请写出上述过程沉淀溶解的离子方程式
②根据以上实验,判断NH3和H2O与Cu2+的配位能力:NH3
③请写出铜原子的核外电子排布式
(3)配位化学创始人维尔纳发现,将各为1mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol。已知上述配合物中配离子的配位数均为6。请根据实验事实用配合物的形式写出它们的化学式。
①CoCl3·5NH3
您最近一年使用:0次
【推荐3】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级的电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出下列元素的名称:
C___________ ;D_______ ;E_______ 。
(2)基态C原子的电子排布图为_____ 。
(3)当n=2时,B的最简单气态氢化物的电子式为_____ ,BC2分子的结构式为_____ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_________ 。
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)E元素在元素周期表中的位置是______ ,其最高价氧化物的化学式是_____ 。
(1)写出下列元素的名称:
C
(2)基态C原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是
(5)E元素在元素周期表中的位置是
您最近一年使用:0次



