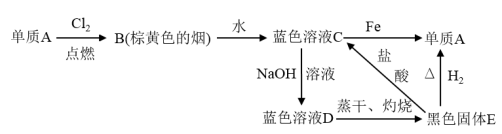
由四种常见元素组成的化合物X,按如下流程进行实验。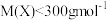 。
。
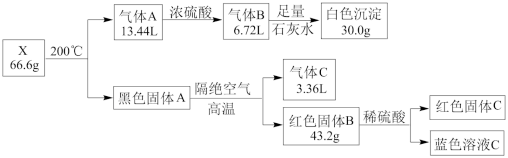
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是___________ (填元素符号)。
(2)化合物X在空气中加热发生反应的化学方程式___________ 。
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:___________ 。
(4)写出红色固体B与稀硫酸反应的离子方程式:___________ 。
(5)某兴趣小组用气体 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:___________ 。
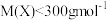 。
。
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是
(2)化合物X在空气中加热发生反应的化学方程式
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:
(4)写出红色固体B与稀硫酸反应的离子方程式:
(5)某兴趣小组用气体
 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
20-21高二下·浙江·期末 查看更多[3]
江西省吉安市永丰县永丰中学2022-2023学年高一上学期期末考试化学(B班)试题(已下线)单科化学-2021年秋季高三开学摸底考试卷03(课标全国专用)浙江省”共美联盟“2020-2021学年高二下学期期末模拟化学试题
更新时间:2021-07-07 22:02:59
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C为3种单质(其中A为固体,B、C为气体),D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E。它们之间的转化关系如下图:
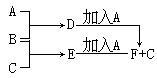
填写下列空白:
(1)物质A是________ ,B是_________ ,B的离子结构示意图为___________ 。
(2)写出化合物E的电子式:_____________ ,D的饱和溶液滴入沸水中溶液呈红褐色的原因是(用离子方程式表示):____________ 。D溶液可以用来止血,请简单说明其止血原理是:_____________ 。
(3)工业上把B单质与石灰乳反应可制得漂白粉,漂白粉的有效成分是__________ ,漂白粉常用于自来水的杀菌消毒,原因是(写出反应的化学方程式,并加以适当的文字
说明):______________ 。
(4)F中加入NaOH溶液,并在空气中放置由白色变为灰绿色最后变成红褐色沉淀的化学方程式是_____________ 。

填写下列空白:
(1)物质A是
(2)写出化合物E的电子式:
(3)工业上把B单质与石灰乳反应可制得漂白粉,漂白粉的有效成分是
说明):
(4)F中加入NaOH溶液,并在空气中放置由白色变为灰绿色最后变成红褐色沉淀的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知有如图所示物质间的相互转化,已知A是一种金属单质。
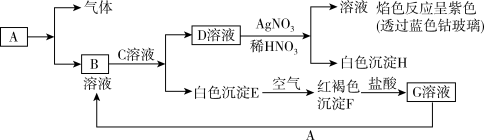
试回答:
(1)按要求作答:B物质的化学式:___________ ,C物质的电子式___________ 。
(2)写出由E转变成F的化学方程式:___________ 。
(3)写出下列反应的离子方程式:D溶液与AgNO3反应:___________ ;向G溶液中加入A:___________ 。
(4)焰色试验是___________ 变化。填(“物理”或“化学”)

试回答:
(1)按要求作答:B物质的化学式:
(2)写出由E转变成F的化学方程式:
(3)写出下列反应的离子方程式:D溶液与AgNO3反应:
(4)焰色试验是
您最近一年使用:0次
【推荐3】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_________________ ;
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则
①C的化学式为________ ;
②反应B+A→C的离子方程式为_______________________________________________ ;
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D的化学式为__________ ;
②若图c符合事实,则其pH变化的原因是_______________________ (用离子方程式表示);
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式_________________________________________ ;

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则
①C的化学式为
②反应B+A→C的离子方程式为
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D的化学式为
②若图c符合事实,则其pH变化的原因是
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】CuCl难溶于水、乙醇和稀硫酸,具有较强的还原性,潮湿环境下会发生水解。某小组设计实验以CuO为原料制备氯化亚铜,装置如图所示(夹持装置已省略)。
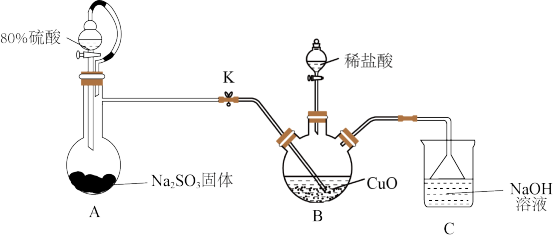
实验步骤:
第1步:连接装置并检查气密性;
第2步:按图示装置装入药品;
第3步:关闭止水夹K,向三颈烧瓶中加盐酸。当氧化铜完全溶解时关闭B中分液漏斗的活塞;
第4步:打开止水夹K,向圆底烧瓶中缓慢加入80%硫酸,当_______时(答实验现象),制备CuCl结束,然后_______(答实验操作);
第5步:对B中混合物进行过滤、洗涤、干燥。
请回答下列问题:
(1)A中_______ (“能”或“不能”)用98%硫酸替代80%硫酸,理由为_______ 。
(2)第4步的化学方程式为_______ 。
(3)装置C的作用为_______ 。
(4)将第4步补充完整:当_______ 时(答实验现象),制备CuCl结束,然后_______ 。(答实验操作)。
(5)洗涤产品时最好先用_______ 洗涤后用_______ 洗涤(填字母)。原因是_______ 。
A.水 B.SO2水溶液 C.NaOH水溶液 D.75%乙醇溶液
(6)实验时若用碱式碳酸铜代替氧化铜,可提高产品的纯度和产率,理由是_______ 。

实验步骤:
第1步:连接装置并检查气密性;
第2步:按图示装置装入药品;
第3步:关闭止水夹K,向三颈烧瓶中加盐酸。当氧化铜完全溶解时关闭B中分液漏斗的活塞;
第4步:打开止水夹K,向圆底烧瓶中缓慢加入80%硫酸,当_______时(答实验现象),制备CuCl结束,然后_______(答实验操作);
第5步:对B中混合物进行过滤、洗涤、干燥。
请回答下列问题:
(1)A中
(2)第4步的化学方程式为
(3)装置C的作用为
(4)将第4步补充完整:当
(5)洗涤产品时最好先用
A.水 B.SO2水溶液 C.NaOH水溶液 D.75%乙醇溶液
(6)实验时若用碱式碳酸铜代替氧化铜,可提高产品的纯度和产率,理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】胆矾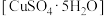 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
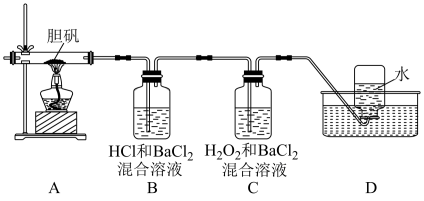
(1)B装置中 的作用是
的作用是___________ 。
(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有___________ 气体产生,写出B中发生反应的离子方程式___________ 。
(3)推测D中收集到的气体是___________ ,其检验方法为___________ 。
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: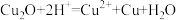 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。
(5)结合上述实验现象,写出胆矾在 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式____ 。
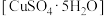 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中
 的作用是
的作用是(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有
(3)推测D中收集到的气体是
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为
 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: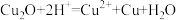 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。| 实验步骤 | 实验预期 | 实验结论 |
准确称取 红色固体,加入足量 红色固体,加入足量 | 固体残留物仅为 |
 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】现有某铁碳合金(可看作铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中碳的质量分数,设计了如图所示的实验装置(夹持仪器已省略)。
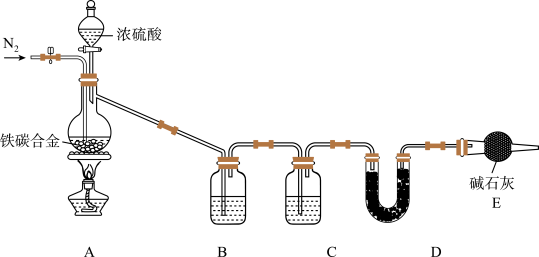
(1)装置A中发生的反应除外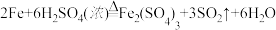 ,还有
,还有________________ 。
(2)请完成下列表格:
(3)若铁碳合金的质量为5.00g,充分反应后称得D装置增重0.66g,则合金中碳的质量分数为_______ ,若缺少E装置,则所测碳的质量分数_________ (填“偏高”“偏低”或“无影响”)。

(1)装置A中发生的反应除外
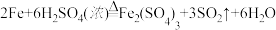 ,还有
,还有(2)请完成下列表格:
| 装置代号 | B | C | D |
| 所盛试剂 | 酸性 溶液 溶液 | ① | ② |
| 装置作用 | ③ | 干燥气体 | ④ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定有机物物分子式的常用装置.

现准确称取0.72g某烃样品,经燃烧后A管增重2.2g,B管增重1.08g。请回答:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺是:__________ ;
(2)A、B管内均盛有固态试剂,A管的作用是__________ 。
(3)燃烧管中CuO的作用是_________ ;如果把CuO网去掉,A管重量将_________ ;(填“增大”、“减小”、或“不变”);
(4)请改进这套装置的一个不足之处_________ 。
(5)若该有机物分子中含有4个甲基,则该有机物的结构简式为_________ ;该有机物的二氯代物有_______ 种。

现准确称取0.72g某烃样品,经燃烧后A管增重2.2g,B管增重1.08g。请回答:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺是:
(2)A、B管内均盛有固态试剂,A管的作用是
(3)燃烧管中CuO的作用是
(4)请改进这套装置的一个不足之处
(5)若该有机物分子中含有4个甲基,则该有机物的结构简式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】固体化合物 在太阳能电池领域有重要用途。为探究
在太阳能电池领域有重要用途。为探究 的组成(仅含两种元素,摩尔质量小于
的组成(仅含两种元素,摩尔质量小于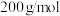 ),某研究性小组设计并完成如下实验:
),某研究性小组设计并完成如下实验:
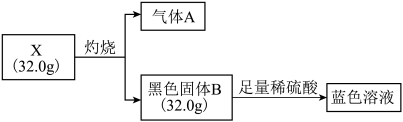
已知:气体 ,固体
,固体 均为常见氧化物,且气体
均为常见氧化物,且气体 能使品红溶液褪色。请回答:
能使品红溶液褪色。请回答:
(1) 的组成元素为
的组成元素为_____________ (用元素符号表示)。
(2)写出固体 与足量稀硫酸反应的离子方程式
与足量稀硫酸反应的离子方程式____________________________________ 。
(3)写出 在空气中灼烧的化学方程式
在空气中灼烧的化学方程式____________________________________________ 。
 在太阳能电池领域有重要用途。为探究
在太阳能电池领域有重要用途。为探究 的组成(仅含两种元素,摩尔质量小于
的组成(仅含两种元素,摩尔质量小于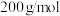 ),某研究性小组设计并完成如下实验:
),某研究性小组设计并完成如下实验:
已知:气体
 ,固体
,固体 均为常见氧化物,且气体
均为常见氧化物,且气体 能使品红溶液褪色。请回答:
能使品红溶液褪色。请回答:(1)
 的组成元素为
的组成元素为(2)写出固体
 与足量稀硫酸反应的离子方程式
与足量稀硫酸反应的离子方程式(3)写出
 在空气中灼烧的化学方程式
在空气中灼烧的化学方程式
您最近一年使用:0次