固体化合物 在太阳能电池领域有重要用途。为探究
在太阳能电池领域有重要用途。为探究 的组成(仅含两种元素,摩尔质量小于
的组成(仅含两种元素,摩尔质量小于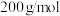 ),某研究性小组设计并完成如下实验:
),某研究性小组设计并完成如下实验:
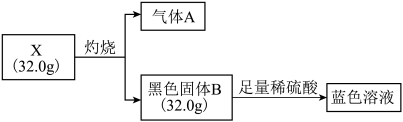
已知:气体 ,固体
,固体 均为常见氧化物,且气体
均为常见氧化物,且气体 能使品红溶液褪色。请回答:
能使品红溶液褪色。请回答:
(1) 的组成元素为
的组成元素为_____________ (用元素符号表示)。
(2)写出固体 与足量稀硫酸反应的离子方程式
与足量稀硫酸反应的离子方程式____________________________________ 。
(3)写出 在空气中灼烧的化学方程式
在空气中灼烧的化学方程式____________________________________________ 。
 在太阳能电池领域有重要用途。为探究
在太阳能电池领域有重要用途。为探究 的组成(仅含两种元素,摩尔质量小于
的组成(仅含两种元素,摩尔质量小于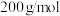 ),某研究性小组设计并完成如下实验:
),某研究性小组设计并完成如下实验:
已知:气体
 ,固体
,固体 均为常见氧化物,且气体
均为常见氧化物,且气体 能使品红溶液褪色。请回答:
能使品红溶液褪色。请回答:(1)
 的组成元素为
的组成元素为(2)写出固体
 与足量稀硫酸反应的离子方程式
与足量稀硫酸反应的离子方程式(3)写出
 在空气中灼烧的化学方程式
在空气中灼烧的化学方程式
19-20高二·浙江·期末 查看更多[3]
更新时间:2020-02-27 21:53:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】为探究某橙色含结晶水的盐的组成和性质,设计并完成如下实验:
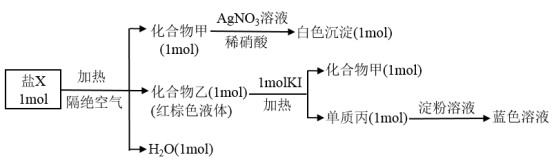
请回答:
(1)化合物甲所含阴离子的离子结构示意图为________________ 。
(2)X的化学式为________________ 。
(3)若分离化合物甲和单质丙组成的固体混合物,最简单的方法是________________ 。
(4)乙与KI反应的化学方程式为________________________________ 。
(5)乙的化学性质与其组成元素的单质相似,下列物质能与乙发生反应的是________ 。
A. B. Mg C.
B. Mg C. D. NaOH
D. NaOH
(6)下列关于卤族物质应用的说法不正确的是________ .
A.实验室常用电解饱和食盐水的方法制取氯气
B.氯气和二氧化氯均可用于自来水消毒,但二氧化氯更高效安全
C.工业上常用氢气与氯气充分混合再点燃的方法制取氯化氢,氯化氢溶于水后可得盐酸
D.可用于生产多种药剂,如熏蒸剂、杀虫剂、抗爆剂等
E.海带可用于治疗碘缺乏病
F.碘化银可用于人工降雨,也是胶片中必不可少的成分

请回答:
(1)化合物甲所含阴离子的离子结构示意图为
(2)X的化学式为
(3)若分离化合物甲和单质丙组成的固体混合物,最简单的方法是
(4)乙与KI反应的化学方程式为
(5)乙的化学性质与其组成元素的单质相似,下列物质能与乙发生反应的是
A.
 B. Mg C.
B. Mg C. D. NaOH
D. NaOH(6)下列关于卤族物质应用的说法不正确的是
A.实验室常用电解饱和食盐水的方法制取氯气
B.氯气和二氧化氯均可用于自来水消毒,但二氧化氯更高效安全
C.工业上常用氢气与氯气充分混合再点燃的方法制取氯化氢,氯化氢溶于水后可得盐酸
D.可用于生产多种药剂,如熏蒸剂、杀虫剂、抗爆剂等
E.海带可用于治疗碘缺乏病
F.碘化银可用于人工降雨,也是胶片中必不可少的成分
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。

(1)物质D的化学式为________ 。
(2)A和水反应生成B和C的离子方程式为____________________ ,列出A的一种重要用途_________________ 。
(3)H在潮湿空气中变成M的实验现象是______________________ 。
(4)反应①的离子方程式为_______________________________________ 。

(1)物质D的化学式为
(2)A和水反应生成B和C的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)反应①的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图是实验室制取 并验证
并验证 某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:

(1)①中发生反应的离子方程式为_______ 。
(2)③的实验现象证明 有
有_______ 性。
(3)④中 做
做_______ 剂。
(4)⑤中反应生成两种强酸,该反应的离子方程式是_______ 。
(5)⑥的作用是_______ 。
 并验证
并验证 某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
(1)①中发生反应的离子方程式为
(2)③的实验现象证明
 有
有(3)④中
 做
做(4)⑤中反应生成两种强酸,该反应的离子方程式是
(5)⑥的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组同学利用如图所示装置完成碳与浓硫酸反应的实验,并验证所得气体产物。请完成下列空白。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:____ 。
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂____ 和作用是____ 。
B中加入的试剂____ 和作用是____ 。
D中加入的试剂____ 和作用是____ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(2)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂
B中加入的试剂
D中加入的试剂
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫元素广泛存在于自然界中,是动植物不可缺少的元素。 的生成及性质检验装置如图所示。
的生成及性质检验装置如图所示。 的化学方程式为
的化学方程式为___________ 。
(2)试管 中盛的试剂为品红溶液,可验证
中盛的试剂为品红溶液,可验证 的
的___________ 。
(3)试管B中盛的试剂为___________ ,可验证 的水溶液呈酸性。
的水溶液呈酸性。
(4)设计实验,探究试管C溶液中的+4价硫元素是否被完全氧化。
可选用的试剂:酸性 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、淀粉溶液、
溶液、淀粉溶液、 溶液、
溶液、 溶液、
溶液、 溶液、铁粉、稀硫酸、稀盐酸
溶液、铁粉、稀硫酸、稀盐酸
 的生成及性质检验装置如图所示。
的生成及性质检验装置如图所示。
 的化学方程式为
的化学方程式为(2)试管
 中盛的试剂为品红溶液,可验证
中盛的试剂为品红溶液,可验证 的
的(3)试管B中盛的试剂为
 的水溶液呈酸性。
的水溶液呈酸性。(4)设计实验,探究试管C溶液中的+4价硫元素是否被完全氧化。
可选用的试剂:酸性
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、淀粉溶液、
溶液、淀粉溶液、 溶液、
溶液、 溶液、
溶液、 溶液、铁粉、稀硫酸、稀盐酸
溶液、铁粉、稀硫酸、稀盐酸| 序号 | 步骤 | 现象 | 结论 |
| ① | 取少量试管C中溶液,向其中滴加 | 溶液中存在+4价硫元素 | |
| ② | 取少量试管C中溶液,加入稀盐酸酸化,向其中滴加 | 溶液中存在 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组设计了图示实验装置(省略了夹持仪器)来测定某铁碳合金中铁的质量分数。

(1)称取w g铁碳合金,加入足量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②______________ 。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式__________ 。
(3)B中的现象是:____________ ;C的作用是:____________ 。
(4)如果利用球形干燥管反应前后质量的变化来测定铁的质量分数,甲同学认为结果可能偏大,理由是_________ ;也可能偏小,理由是____________ 。
(5)乙同学认为可以用烧瓶里反应后的溶液经过一系列操作来测定铁的质量分数:加入足量的NaOH溶液、_________ 、洗涤、在空气中_________ 、称重。洗涤应该在过滤装置中进行;检查是否洗净,需要用到的试剂是___________ 。一系列操作后所得固体为a g,则合金中铁的质量分数为___________ %。
(6)丙同学认为可以用中和滴定的方法来测定铁的质量分数:将反应后烧瓶里的溶液转移至锥形瓶中,加入0.1000 mol/L氢氧化钠溶液30.00 mL,反应完全后,加2滴甲基橙溶液,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.10mL。
①把标准盐酸注入润洗过的红色手柄滴定管后,应该打开活塞,使________ ,并使液面位于零刻度或零刻度以下位置,记录读数。
②从物质性质的角度分析,该方法即使操作规范,也有很大的误差,其实属于“方法错误”,理由是___________ 。

(1)称取w g铁碳合金,加入足量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式
(3)B中的现象是:
(4)如果利用球形干燥管反应前后质量的变化来测定铁的质量分数,甲同学认为结果可能偏大,理由是
(5)乙同学认为可以用烧瓶里反应后的溶液经过一系列操作来测定铁的质量分数:加入足量的NaOH溶液、
(6)丙同学认为可以用中和滴定的方法来测定铁的质量分数:将反应后烧瓶里的溶液转移至锥形瓶中,加入0.1000 mol/L氢氧化钠溶液30.00 mL,反应完全后,加2滴甲基橙溶液,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.10mL。
①把标准盐酸注入润洗过的红色手柄滴定管后,应该打开活塞,使
②从物质性质的角度分析,该方法即使操作规范,也有很大的误差,其实属于“方法错误”,理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】铁触媒(铁的氧化物)是硫酸工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。
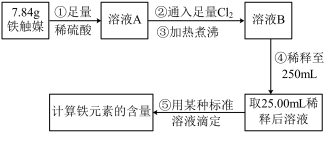
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________ 。
(2)若通入Cl2不足量,溶液B中还含有____________ ,会影响测定结果。
(3)若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。限选试剂:0.1 mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红溶液、淀粉-KI溶液、0.1 mol·L-1 KSCN溶液。
方案二:用下列装置测定铁触媒的含铁量,确定其组成。
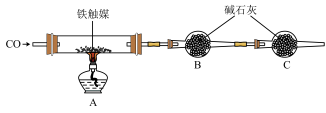
(4)干燥管C的作用是________________________ 。
(5)称取15.2 g铁触媒进行上述实验。充分反应后,测得干燥管B增重11.0 g,则该铁触媒的化学式可表示为________________________ 。
方案一:用下列流程测定铁触媒的含铁量,确定其组成。

(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和
(2)若通入Cl2不足量,溶液B中还含有
(3)若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。限选试剂:0.1 mol·L-1酸性KMnO4溶液、紫色石蕊试液、品红溶液、淀粉-KI溶液、0.1 mol·L-1 KSCN溶液。
| 实验操作 | 预期现象与结论 |
方案二:用下列装置测定铁触媒的含铁量,确定其组成。
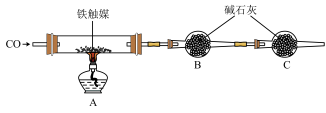
(4)干燥管C的作用是
(5)称取15.2 g铁触媒进行上述实验。充分反应后,测得干燥管B增重11.0 g,则该铁触媒的化学式可表示为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)硫酸是重要的化工原料,研究小组同学对硫酸的工业制备和性质进行探究。查阅资料,工业制硫酸的过程如下图所示:
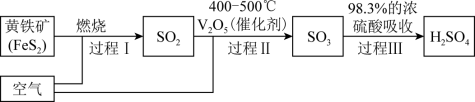
上述工业制硫酸过程中,没有发生氧化还原反应的过程是_______ (填“I”“II”或“III”),过程Ⅰ的化学方程式是:_______ 。
(2)煤燃烧产生的废气中含有 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为 )来吸收,还可以得到亚硫酸钠(Na2SO3)粗品。其流程如图:
)来吸收,还可以得到亚硫酸钠(Na2SO3)粗品。其流程如图:
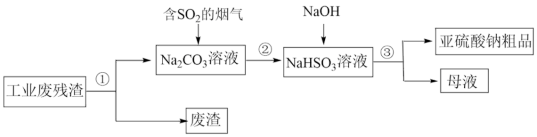
①上述流程中,流程③在NaHSO3溶液中加入NaOH后,发生反应的离子方程式为_______ 。
②亚硫酸钠粗品中可能含有少量 ,请设计实验证明亚硫酸钠粗品含有少量
,请设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
③已知有VL(已换算成标准状况)废气,通入足量 溶液吸收,再加足量
溶液吸收,再加足量 溶液充分反应后(不考虑废气中其他成分的反应),经过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑废气中其他成分的反应),经过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是_______ ;尾气中 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是_______ 。
(3)某工厂以硫酸厂排放的含 废气和硝酸厂排放的含硝酸和氮的氧化物废气为原料生产亚硝酸钠,并对亚硝酸钠进行多角度探究。其工艺流程如下:
废气和硝酸厂排放的含硝酸和氮的氧化物废气为原料生产亚硝酸钠,并对亚硝酸钠进行多角度探究。其工艺流程如下:
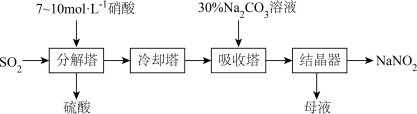
已知: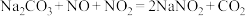 ;
;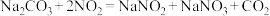
①在分解塔中通入的SO2和硝酸废气中的硝酸反应,若反应后生成的NO与NO2物质的量之比恰好 ,则分解塔中发生反应的化学方程式为
,则分解塔中发生反应的化学方程式为_______ 。
②设计实验验证酸性条件下NaNO2具有氧化性,请补充实验方案。(供选择的试剂:NaNO2溶液、KI溶液、稀硫酸、淀粉溶液)
取一定量KI溶液,_______ 。
(1)硫酸是重要的化工原料,研究小组同学对硫酸的工业制备和性质进行探究。查阅资料,工业制硫酸的过程如下图所示:

上述工业制硫酸过程中,没有发生氧化还原反应的过程是
(2)煤燃烧产生的废气中含有
 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为 )来吸收,还可以得到亚硫酸钠(Na2SO3)粗品。其流程如图:
)来吸收,还可以得到亚硫酸钠(Na2SO3)粗品。其流程如图:
①上述流程中,流程③在NaHSO3溶液中加入NaOH后,发生反应的离子方程式为
②亚硫酸钠粗品中可能含有少量
 ,请设计实验证明亚硫酸钠粗品含有少量
,请设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。③已知有VL(已换算成标准状况)废气,通入足量
 溶液吸收,再加足量
溶液吸收,再加足量 溶液充分反应后(不考虑废气中其他成分的反应),经过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑废气中其他成分的反应),经过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是(3)某工厂以硫酸厂排放的含
 废气和硝酸厂排放的含硝酸和氮的氧化物废气为原料生产亚硝酸钠,并对亚硝酸钠进行多角度探究。其工艺流程如下:
废气和硝酸厂排放的含硝酸和氮的氧化物废气为原料生产亚硝酸钠,并对亚硝酸钠进行多角度探究。其工艺流程如下:
已知:
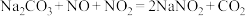 ;
;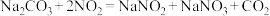
①在分解塔中通入的SO2和硝酸废气中的硝酸反应,若反应后生成的NO与NO2物质的量之比恰好
 ,则分解塔中发生反应的化学方程式为
,则分解塔中发生反应的化学方程式为②设计实验验证酸性条件下NaNO2具有氧化性,请补充实验方案。(供选择的试剂:NaNO2溶液、KI溶液、稀硫酸、淀粉溶液)
取一定量KI溶液,
您最近一年使用:0次




