1967年,C.J.Pedersen发表了关于冠醚合成和选择性配位碱金属离子的论文,开创了超分子化学新领域。超分子主要是指分子通过非共价键完成自我识别与自我组装过程形成的具有特定结构的分子聚集体。在超分子层次上,化学与生命环境、材料、信息等等学科相互交叉,形成超分子科学。目前,超分子科学在分子器件基因结构、纳米材料等方面取得了巨大进展,已成为21世纪一个十分活跃的前沿领域。近期化学家合成了一种结构非常特殊的超分子,其设计思路是,利用分子自我识别与自我组装的能力,将3个环状化合物套入Y型分子的骨架上,再通过化学反应将3个环状化合物的侧链进行关环形成第4个环。图示如下:
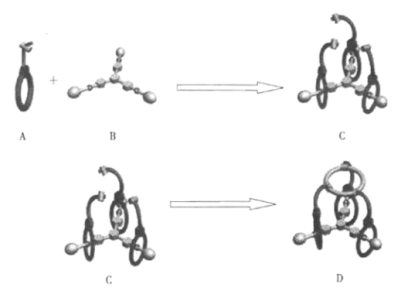
(1)已知化合物A.、B的结构分别如下图所示,试问:它们通过什么作用进行自我识别与自我组装__ ?

(2)在用邻苯二酚和1,8-二氯-3,6-二氧杂辛烷进行[2+2]环化合成化合物A中的大环冠醚部分时,需用到2种方法以提高成环产率,即高度稀释和加入金属离子(模板离子)。试说明为什么加入模板离子会提高产率____ ?对Na+、K+、Rb+、Cs+而言哪种离子作模板产率最高______ ?为什么________ ?
(3)将超分子C转变为D时使用的化学反应通常称之为烯烃复分解反应,生成D的同时,还生成另一种化合物E。已知D中的第4个环为三十三元环,试向化合物E是________ 。反应过程中每生成一个D同时生成_________ 个E。
(4)K是合成化合物A的原料之一,以E为主要原料合成K的路线如下,请写出F、G、H、I、J、K所代表的化合物或反应条件:F____ 、G____ 、H____ 、I___ 、J___ 、K___ 。
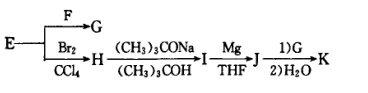
(5)K也可以用如下所示的路线合成,写出L、M、N、O所代表的化合物:L_____ 、M_____ 、N_____ 、O_____ 。


(1)已知化合物A.、B的结构分别如下图所示,试问:它们通过什么作用进行自我识别与自我组装

(2)在用邻苯二酚和1,8-二氯-3,6-二氧杂辛烷进行[2+2]环化合成化合物A中的大环冠醚部分时,需用到2种方法以提高成环产率,即高度稀释和加入金属离子(模板离子)。试说明为什么加入模板离子会提高产率
(3)将超分子C转变为D时使用的化学反应通常称之为烯烃复分解反应,生成D的同时,还生成另一种化合物E。已知D中的第4个环为三十三元环,试向化合物E是
(4)K是合成化合物A的原料之一,以E为主要原料合成K的路线如下,请写出F、G、H、I、J、K所代表的化合物或反应条件:F
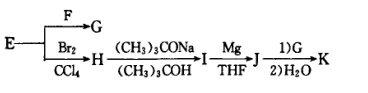
(5)K也可以用如下所示的路线合成,写出L、M、N、O所代表的化合物:L

更新时间:2021-07-08 14:37:24
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】甲醇(CH3OH)是一种用途广泛的基础有机原料和优质燃料。
(1)甲醇通过一系列反应可生成某有机物,结构简式如图。此有机物分子中有个_______ 手性碳原子。

(2)甲醇的同系物乙醇,在一定条件下可发生消去反应生成乙烯,乙烯分子中H-C-H键角_______ 120º(填 “大于”或“小于” )。
(3)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,沸点57.1℃)。
①乙酸甲酯中σ键和π键的个数之比为_______ 。
②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,工业上用蒸馏的方法分离二者时常先加适量水,理由为_______ 。
(4)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T-碳,T-碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,晶胞结构及俯视图如图所示。

①T-碳与金刚石互称为_______ 。一个T-碳晶胞中含有_______ 个碳原子。
②T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比_______ 。
(1)甲醇通过一系列反应可生成某有机物,结构简式如图。此有机物分子中有个

(2)甲醇的同系物乙醇,在一定条件下可发生消去反应生成乙烯,乙烯分子中H-C-H键角
(3)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,沸点57.1℃)。
①乙酸甲酯中σ键和π键的个数之比为
②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,工业上用蒸馏的方法分离二者时常先加适量水,理由为
(4)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T-碳,T-碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,晶胞结构及俯视图如图所示。

①T-碳与金刚石互称为
②T-碳的密度约为金刚石的一半。则T-碳晶胞的边长和金刚石晶胞的边长之比
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙二套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b-铜丝;c-无水硫酸铜;d-银氨溶液。

(1)简述两套方案各自的优点:
甲___________________________________________
乙_________________________________________
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为_______________ (例如甲①,乙②)
(3)若要保证此实验有较高的效率,还需补充的仪器有________ 。理由________ 。
(4)写出d中的化学方程式_______________ ,该反应类型为_____________ 。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式_________ 。

(1)简述两套方案各自的优点:
甲
乙
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为
(3)若要保证此实验有较高的效率,还需补充的仪器有
(4)写出d中的化学方程式
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式
您最近一年使用:0次
【推荐2】实验题
Ⅰ.下列实验操作不正确的是_________ 。(填写序号)
(1)在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
(2)将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,反复多次,完成乙醇氧化为乙醛的实验
(3)乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
(4)向试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制取乙酸乙酯
(5)实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流
(6)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液
Ⅱ.利用右图装置还可以验证醋酸、苯酚、碳酸的酸性强弱。

(1)A中固体试剂是____ ;B中所盛溶液溶质是_____ ;C中所盛溶液溶质是______ (选填字母)。
a.醋酸钠b.碳酸氢钠c.苯酚钠d.碳酸钠
(2)写出C中反应的离子方程式是:_______________ ;
(3)有同学认为没有B装置,也可以验证酸性的强弱,这种认为_____ (是或不)合理的,原因是__________________________ 。
Ⅰ.下列实验操作不正确的是
(1)在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
(2)将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,反复多次,完成乙醇氧化为乙醛的实验
(3)乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
(4)向试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制取乙酸乙酯
(5)实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流
(6)验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液
Ⅱ.利用右图装置还可以验证醋酸、苯酚、碳酸的酸性强弱。

(1)A中固体试剂是
a.醋酸钠b.碳酸氢钠c.苯酚钠d.碳酸钠
(2)写出C中反应的离子方程式是:
(3)有同学认为没有B装置,也可以验证酸性的强弱,这种认为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】兔耳草醛H是一种重要的香料,主要用于食品、化妆品等工业中。用有机物A为原料可以合成兔耳草醛H,其合成路线如图所示,其中有机物A的核磁共振氢谱只有一组峰:

中间产物D是一种精细化工产品,可用作香料,能发生如下反应:

已知:I.醛与二元醇(如乙二醇)可发生以下反应: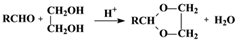
Ⅱ.
请回答:
(1)D的结构简式为________ ,E中含有的官能团名称为_________ 。
(2)A与反应物a在AlCl3催化下得到B,该反应源于工业制乙苯,则反应物a为__________ (写出结构简式),该反应的反应类型为________________________
(3)由C到D需要两步反应,请依次写出反应条件_____________________________
(4)F→G的反应类型___________ , G→H的化学方程式为____________________________ 。
(5)兔耳草醛H中的含氧官能团易被氧化,生成化合物W,G与W可发生酯化反应,写出G与W反应的化学方程式_____________________________________________ 。
(6)写出与W互为同分异构体且符合下列条件所有同分异构体的结构简式________
a.属于芳香族化合物且苯环上有三个取代基
b.1 mol该物质最多可消耗2molNaOH
c.能发生银镜反应
d.核磁共振氢谱有5组峰(面积为12:2:1:2:1)

中间产物D是一种精细化工产品,可用作香料,能发生如下反应:

已知:I.醛与二元醇(如乙二醇)可发生以下反应:
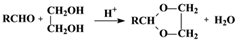
Ⅱ.

请回答:
(1)D的结构简式为
(2)A与反应物a在AlCl3催化下得到B,该反应源于工业制乙苯,则反应物a为
(3)由C到D需要两步反应,请依次写出反应条件
(4)F→G的反应类型
(5)兔耳草醛H中的含氧官能团易被氧化,生成化合物W,G与W可发生酯化反应,写出G与W反应的化学方程式
(6)写出与W互为同分异构体且符合下列条件所有同分异构体的结构简式
a.属于芳香族化合物且苯环上有三个取代基
b.1 mol该物质最多可消耗2molNaOH
c.能发生银镜反应
d.核磁共振氢谱有5组峰(面积为12:2:1:2:1)
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】吉非替尼(I)是一种抗癌药物,其合成路线如图:
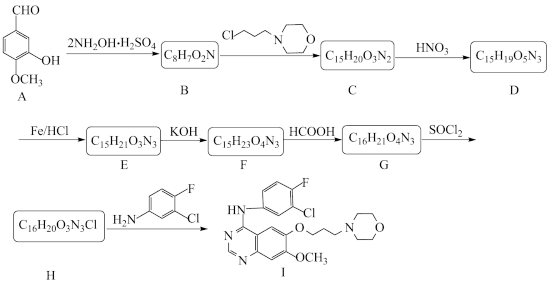
已知:
I.R—CHO R—CN
R—CN
II.R—CN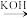

 R—CH2—NH2
R—CH2—NH2
III.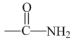 +HO—R
+HO—R

(1)下列说法正确的是___ 。
(2)已知G中含有“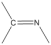 ”,请写出G的结构简式:
”,请写出G的结构简式:___ 。
(3)请写出B生成C的反应方程式:___ 。
(4)写出有机物A满足下列条件的同分异构体:___ 。
①可以使FeCl3显色;②不能发生银镜反应:③核磁共振氢谱中有5个峰;④仅有苯环一个环状结构,且苯环,上的一氯代物有两种。
(5)以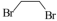 和
和 为原料合成原料
为原料合成原料 ,无机试剂以及已知信息中作为反应条件的试剂任选,请写出合成路线
,无机试剂以及已知信息中作为反应条件的试剂任选,请写出合成路线___ 。

已知:
I.R—CHO
 R—CN
R—CNII.R—CN
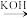

 R—CH2—NH2
R—CH2—NH2III.
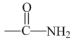 +HO—R
+HO—R

(1)下列说法正确的是
| A.1mol A可以和3mol H2加成 | B.D生成E的反应属于还原反应 |
| C.1mol F生成G的过程中有2mol H2O生成 | D.H中含有手性碳原子 |
 ”,请写出G的结构简式:
”,请写出G的结构简式:(3)请写出B生成C的反应方程式:
(4)写出有机物A满足下列条件的同分异构体:
①可以使FeCl3显色;②不能发生银镜反应:③核磁共振氢谱中有5个峰;④仅有苯环一个环状结构,且苯环,上的一氯代物有两种。
(5)以
 和
和 为原料合成原料
为原料合成原料 ,无机试剂以及已知信息中作为反应条件的试剂任选,请写出合成路线
,无机试剂以及已知信息中作为反应条件的试剂任选,请写出合成路线
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】阿比朵尔是一种抗病毒药物,主要用于流行性感冒的治疗。F是合成阿比朵尔的中间体,可由下列路线合成:
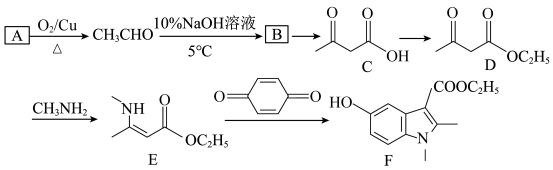
已知:RCHO+CH3CHO RCH(OH)CH2CHO
RCH(OH)CH2CHO
回答下列问题:
(1)A的名称为___________ ,B的结构简式为___________ 。
(2)E的分子式是___________ ,F的含氧官能团名称为___________ 。
(3)由乙醛生成B的反应类型为___________ 。
(4)C D的化学方程式为
D的化学方程式为___________ 。
(5)D有多种同分异构体,其中既能与NaHCO3反应,又能发生银镜反应有___________ 种。其中核磁共振氢谱有4组峰,峰面积之比为6∶1∶1∶2的结构简式为___________ 。
(6)写出用苯甲醇和乙醛为原料制备 的合成路线(其他试剂任选):
的合成路线(其他试剂任选):__________ 。

已知:RCHO+CH3CHO
 RCH(OH)CH2CHO
RCH(OH)CH2CHO回答下列问题:
(1)A的名称为
(2)E的分子式是
(3)由乙醛生成B的反应类型为
(4)C
 D的化学方程式为
D的化学方程式为(5)D有多种同分异构体,其中既能与NaHCO3反应,又能发生银镜反应有
(6)写出用苯甲醇和乙醛为原料制备
 的合成路线(其他试剂任选):
的合成路线(其他试剂任选):
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
【推荐3】氰基丙烯酸酯在碱性条件下能快速聚合为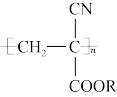 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
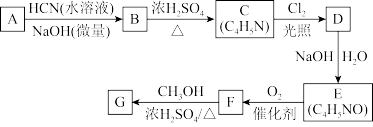
已知:
①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰


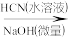
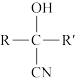
回答下列问题:
(1)A的化学名称为_______ 。
(2)B的结构简式为______ ,其核磁共振氢谱显示为______ 组峰,峰面积比为______ 。
(3)由C生成D的反应类型为________ 。
(4)由D生成E的化学方程式为___________ 。
(5)G中的官能团有___ 、 ____ 、_____ 。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____ 种。(不含立体异构)
 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
已知:
①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰


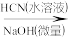

回答下列问题:
(1)A的化学名称为
(2)B的结构简式为
(3)由C生成D的反应类型为
(4)由D生成E的化学方程式为
(5)G中的官能团有
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)⇌H2NCOONH4(氨基甲酸铵)(l) ΔH1<0
第二步:H2NCOONH4(l)⇌H2O(l)+H2NCONH2(l) ΔH2>0
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L的密闭容器中投入4 mol 氨和1 mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如图所示:

(1)已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_______ 步反应决定。
(2)反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的的速率v(CO2)=_______ 。
(3)尿素在强碱性条件下用次氯酸钠氧化可以制得联氨(N2H4),该反应的离子方程式为:_______ 。联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图所示。

①在图示的转化中,化合价不变的元素是_______ (填元素名称)。
②在转化过程中通入氧气发生反应后,溶液的pH将_______ (填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为_______ 。
③加入NaClO时发生的反应为:Cu(NH3) +2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O,该反应需在需在8℃以上进行,其目的除了加快反应速率外,还有
+2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O,该反应需在需在8℃以上进行,其目的除了加快反应速率外,还有_______ 。
第一步:2NH3(l)+CO2(g)⇌H2NCOONH4(氨基甲酸铵)(l) ΔH1<0
第二步:H2NCOONH4(l)⇌H2O(l)+H2NCONH2(l) ΔH2>0
某实验小组模拟工业上合成尿素的条件,在一体积为0.5L的密闭容器中投入4 mol 氨和1 mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如图所示:

(1)已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
(2)反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的的速率v(CO2)=
(3)尿素在强碱性条件下用次氯酸钠氧化可以制得联氨(N2H4),该反应的离子方程式为:

①在图示的转化中,化合价不变的元素是
②在转化过程中通入氧气发生反应后,溶液的pH将
③加入NaClO时发生的反应为:Cu(NH3)
 +2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O,该反应需在需在8℃以上进行,其目的除了加快反应速率外,还有
+2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O,该反应需在需在8℃以上进行,其目的除了加快反应速率外,还有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】化学反应一般是由若干基元反应构成的,所以原则上可由反应机理建立反应的速率方程。在科学研究工作中,往往根据实践经验先假设反应机理,然后再用各种实验方法和手段,检验所设反应机理的正确性。硝酰胺在水溶液中的分解反应为:NO2NH2→N2O(g)+H2O。实验测得其速率方程为: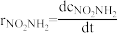 =k
=k
(1)有研究者提出下列3种反应机理,你认为何者是合理的_______ ?并写出k的表达式_______ 。
①NO2NH2 N2O(g)+H2O
N2O(g)+H2O
②NO2NH2+H3O+ NO2NH
NO2NH +H2(瞬间达到平衡)
+H2(瞬间达到平衡)
NO2NH
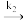 N2O(g)+H3O+(缓慢反应)
N2O(g)+H3O+(缓慢反应)
③NO2NH2+H2O NO2NH-+H3O+(瞬间达到平衡)
NO2NH-+H3O+(瞬间达到平衡)
NO2NH-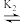 N2O(g)+OH-(缓慢反应)
N2O(g)+OH-(缓慢反应)
H3O++OH-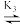 2H2O(快速反应)
2H2O(快速反应)
(2)在实验温度和pH恒定的缓冲介质中,将反应在密闭的容器中进行,测得N2O气体的压力p随时间的变化数据如下表
求NO2NH2分解反应的半衰期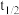
_______ ,并证明lg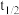 与缓冲介质的pH呈线性关系
与缓冲介质的pH呈线性关系_______ 。
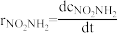 =k
=k
(1)有研究者提出下列3种反应机理,你认为何者是合理的
①NO2NH2
 N2O(g)+H2O
N2O(g)+H2O②NO2NH2+H3O+
 NO2NH
NO2NH +H2(瞬间达到平衡)
+H2(瞬间达到平衡)NO2NH

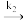 N2O(g)+H3O+(缓慢反应)
N2O(g)+H3O+(缓慢反应)③NO2NH2+H2O
 NO2NH-+H3O+(瞬间达到平衡)
NO2NH-+H3O+(瞬间达到平衡)NO2NH-
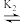 N2O(g)+OH-(缓慢反应)
N2O(g)+OH-(缓慢反应)H3O++OH-
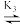 2H2O(快速反应)
2H2O(快速反应)(2)在实验温度和pH恒定的缓冲介质中,将反应在密闭的容器中进行,测得N2O气体的压力p随时间的变化数据如下表
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | ∞ |
| p/kPa | 0 | 6.80 | 12.40 | 17.20 | 20.80 | 24.00 | 40.00 |
求NO2NH2分解反应的半衰期
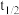
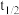 与缓冲介质的pH呈线性关系
与缓冲介质的pH呈线性关系
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(1)三种消毒剂在不同浸泡时间对芽孢杆菌的消毒效果(阳性次数/试验次数)如下表:
下列说法不正确的是_______ 。
A.84消毒液的有效成分为NaClO
B.过氧乙酸的结构简式为
C.质量分数相同时,上述消毒剂消毒效果最好的是季铵盐
D.使用消毒剂浸泡消毒时,要选择合适的浓度和适当的浸泡时间
(2)14C是碳的放射性同位素,半衰期为5730年,常用来估算动植物生存的年代,其原理为:动植物的生命活动需要不断与大气进行碳交换,因此活体内的14C丰度与大气中的14C丰度接近;没有生命体征之后,体内的14C因放射性衰变导致丰度降低,依据衰变量可估计其生存年代。2021年3月,考古学家对三星堆遗址4号坑的碳屑样品进行了分析,测得14C的丰度约为大气中的67.9%,试推测三星堆4号坑距今约_______ 。
A.1400年 B.3200年 C.4100年 D.9400年
(3)测定海水中溶解无机碳(主要为HCO )的总含量。取zmL海水样品酸化,用N2将生成的CO2全部吹出并用NaOH吸收(装置如下图)。充分反应后,将两瓶NaOH吸收液倒入锥形瓶中混合,滴加酚酞,用cmol·L-1盐酸标准溶液滴定至红色恰好褪去(pH=8.0),消耗v1mL标准溶液。再向锥形瓶内滴加溴甲酚绿-甲基红,继续滴定至溶液恰好变红(pH=5.0),又消耗v2mL盐酸标准溶液(v1>v2)。下列说法错误的是
)的总含量。取zmL海水样品酸化,用N2将生成的CO2全部吹出并用NaOH吸收(装置如下图)。充分反应后,将两瓶NaOH吸收液倒入锥形瓶中混合,滴加酚酞,用cmol·L-1盐酸标准溶液滴定至红色恰好褪去(pH=8.0),消耗v1mL标准溶液。再向锥形瓶内滴加溴甲酚绿-甲基红,继续滴定至溶液恰好变红(pH=5.0),又消耗v2mL盐酸标准溶液(v1>v2)。下列说法错误的是_______ 。

A.用两瓶NaOH吸收溶液的目的是保证CO2全部被吸收
B.v1>v2说明吸收液中NaOH过量
C.海水样品中溶解无机碳的物质的量浓度为 mol·L-1
mol·L-1
D.若将硫酸改为盐酸,会因HCl挥发进入吸收瓶而影响无机碳的测定结果
(4)麦角新碱属于吲哚类衍生物,其结构简式如图所示,分子结构中存在3个手性碳原子,它们的绝对构型从1到3依次为_______

A.R,S,S B.R,R,S C.S,R,R D.S,S,R
(5)氮气在常温常压下转化成氨气具有重要意义。近期报道的我国学者研究成果,使用MoSe2负载氮化碳(C3N4)为光电催化剂,利用光电化学方法实现常温常压合成氨。其可能的催化原理和能量变化如下图所示(图b中“*”表示催化剂的活性位点)。

下列说法不正确的是_______ 。
A.NH3在阴极生成
B.8步历程中有3步需要吸收能量
C.仅④涉及氮氮之间共价键的断裂
D.催化剂中的Mo具有空轨道,有利于“吸附”N2并催化反应
(6)某小组研究在25℃的水溶液中,HClO4催化丙酮与Br2的反应: +Br2
+Br2
 +HBr
+HBr
其机理为:

通过分光光度法测出Br2单质的浓度随时间的变化,数据如下图所示。已知Br2初始浓度为520mmol·L-1,下列说法不正确的是_______ 。

A.0~5min内,Br2的平均消耗速率为24mmol·L-1·min-1
B.根据图象判断,Br2的浓度随时间变化符合零级反应动力学特征
C.该反应的决速步为iii
D.该方法也可测定NaOH催化丙酮与Br2反应的化学反应速率
| 消毒剂 | 10min | 30min | 1h | 2h | 5h |
| 1%84消毒液。 1%季铵盐 5%季铵盐 0.1%过氧乙酸 | 5/5 5/5 0/5 0/5 | 3/5 5/5 0/5 0/5 | 2/5 5/5 0/5 0/5 | 0/5 5/5 0/5 0/5 | 0/5 5/5 0/5 0/5 |
下列说法不正确的是
A.84消毒液的有效成分为NaClO
B.过氧乙酸的结构简式为

C.质量分数相同时,上述消毒剂消毒效果最好的是季铵盐
D.使用消毒剂浸泡消毒时,要选择合适的浓度和适当的浸泡时间
(2)14C是碳的放射性同位素,半衰期为5730年,常用来估算动植物生存的年代,其原理为:动植物的生命活动需要不断与大气进行碳交换,因此活体内的14C丰度与大气中的14C丰度接近;没有生命体征之后,体内的14C因放射性衰变导致丰度降低,依据衰变量可估计其生存年代。2021年3月,考古学家对三星堆遗址4号坑的碳屑样品进行了分析,测得14C的丰度约为大气中的67.9%,试推测三星堆4号坑距今约
A.1400年 B.3200年 C.4100年 D.9400年
(3)测定海水中溶解无机碳(主要为HCO
 )的总含量。取zmL海水样品酸化,用N2将生成的CO2全部吹出并用NaOH吸收(装置如下图)。充分反应后,将两瓶NaOH吸收液倒入锥形瓶中混合,滴加酚酞,用cmol·L-1盐酸标准溶液滴定至红色恰好褪去(pH=8.0),消耗v1mL标准溶液。再向锥形瓶内滴加溴甲酚绿-甲基红,继续滴定至溶液恰好变红(pH=5.0),又消耗v2mL盐酸标准溶液(v1>v2)。下列说法错误的是
)的总含量。取zmL海水样品酸化,用N2将生成的CO2全部吹出并用NaOH吸收(装置如下图)。充分反应后,将两瓶NaOH吸收液倒入锥形瓶中混合,滴加酚酞,用cmol·L-1盐酸标准溶液滴定至红色恰好褪去(pH=8.0),消耗v1mL标准溶液。再向锥形瓶内滴加溴甲酚绿-甲基红,继续滴定至溶液恰好变红(pH=5.0),又消耗v2mL盐酸标准溶液(v1>v2)。下列说法错误的是
A.用两瓶NaOH吸收溶液的目的是保证CO2全部被吸收
B.v1>v2说明吸收液中NaOH过量
C.海水样品中溶解无机碳的物质的量浓度为
 mol·L-1
mol·L-1D.若将硫酸改为盐酸,会因HCl挥发进入吸收瓶而影响无机碳的测定结果
(4)麦角新碱属于吲哚类衍生物,其结构简式如图所示,分子结构中存在3个手性碳原子,它们的绝对构型从1到3依次为

A.R,S,S B.R,R,S C.S,R,R D.S,S,R
(5)氮气在常温常压下转化成氨气具有重要意义。近期报道的我国学者研究成果,使用MoSe2负载氮化碳(C3N4)为光电催化剂,利用光电化学方法实现常温常压合成氨。其可能的催化原理和能量变化如下图所示(图b中“*”表示催化剂的活性位点)。

下列说法不正确的是
A.NH3在阴极生成
B.8步历程中有3步需要吸收能量
C.仅④涉及氮氮之间共价键的断裂
D.催化剂中的Mo具有空轨道,有利于“吸附”N2并催化反应
(6)某小组研究在25℃的水溶液中,HClO4催化丙酮与Br2的反应:
 +Br2
+Br2
 +HBr
+HBr其机理为:

通过分光光度法测出Br2单质的浓度随时间的变化,数据如下图所示。已知Br2初始浓度为520mmol·L-1,下列说法不正确的是

A.0~5min内,Br2的平均消耗速率为24mmol·L-1·min-1
B.根据图象判断,Br2的浓度随时间变化符合零级反应动力学特征
C.该反应的决速步为iii
D.该方法也可测定NaOH催化丙酮与Br2反应的化学反应速率
您最近一年使用:0次



