下表中的实线表示元素周期表的部分边界,已知A、B、C、D、E为短周期元素。

回答下列问题:
(1)请在上表中用实线补出元素周期表的上边界。___________
(2)某主族元素原子的核外电子排为: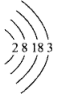 ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为___________ 。
(3)元素E的非金属性___________ (填“强于”或“弱于”)元素D的非金属性,从原子结构的角度解释原因___________ 。下列方法能验证以上结论的是___________ (填序号)。
a.比较这两种元素的单质与氢气化合的难易
b.比较这两种元素的常见单质的沸点
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的含氧酸的酸性
(4)X是由A、B、C、D四种元素组成的一种离子化合物,已知:①1molX能与足量NaOH浓溶液反应生成22.41L气体(标准状况);②X能与盐酸反应产生气体Y,该气体能与氯水反应,则X是___________ (填化学式),气体Y与氯水反应的离子方程式___________ 。

回答下列问题:
(1)请在上表中用实线补出元素周期表的上边界。
(2)某主族元素原子的核外电子排为:
 ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为(3)元素E的非金属性
a.比较这两种元素的单质与氢气化合的难易
b.比较这两种元素的常见单质的沸点
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的含氧酸的酸性
(4)X是由A、B、C、D四种元素组成的一种离子化合物,已知:①1molX能与足量NaOH浓溶液反应生成22.41L气体(标准状况);②X能与盐酸反应产生气体Y,该气体能与氯水反应,则X是
20-21高一下·山东菏泽·期末 查看更多[2]
更新时间:2021-07-13 16:26:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表短周期的一部分:

请按要求用化学式回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为:_______ (用化学式回答,下同)
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:_______ ;
(3)写出由①④⑤三种元素组成的一种离子化合物的电子式_______ ,若将其溶于水,破坏了其中的_______ (填“离子键”、“共价键”或“离子键和共价键”):
(4)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物反应的离子方程式_______ 。

请按要求用化学式回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为:
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:
(3)写出由①④⑤三种元素组成的一种离子化合物的电子式
(4)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分,参照元素①~⑫在表中的位置,请回答下列问题。
(1)表中元素,化学性质最稳定的是________ ,金属性最强的是__________ ,非金属性最强的是_______ (写编号);最高价氧化物的水化物的酸性最强的是(写化学式)___________ 。
(2)④、⑩的气态氢化物中的稳定性强些的是_______ 。(填化学式)
(3)④、⑥、⑦、⑩元素形成的离子,离子半径的大小顺序是____________ (填化学式)
(4)写出一种由①④组成且含有非极性键的物质的电子式_____________ 。
(5)实验室制取⑪气体的离子方程式为_____________________________
(6)利用较强酸能制出较弱酸的原理,写出一个能证明②和⑧非金属性强弱的一个常见反应的化学方程式_______________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)④、⑩的气态氢化物中的稳定性强些的是
(3)④、⑥、⑦、⑩元素形成的离子,离子半径的大小顺序是
(4)写出一种由①④组成且含有非极性键的物质的电子式
(5)实验室制取⑪气体的离子方程式为
(6)利用较强酸能制出较弱酸的原理,写出一个能证明②和⑧非金属性强弱的一个常见反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表前四周期部分,针对表中的①~⑨9种元素,用化学用语填写下列空白:
(1)①~⑨中,单质化学性质最不活泼的是__________ ,最高价氧化物对应的水化物的酸性最强的是__________ 。
(2)②、③、④的简单离子按离子半径从小到大排列顺序为_________________ 。
(3)④在③单质中燃烧的产物的电子式为_________________ 。
(4)⑤的原子结构示意图为________ ,从原子结构分析,④比⑤活泼的原因是_________ 。
(5)②和⑦形成一种化合物分子,各原子均达到8电子稳定结构,则该化合物的化学式为_________________ 。
(6)②、③的最简单氢化物中,沸点较高的是_____________ 。
(7)②的简单氢化物与②的最高价氧化物的水化物溶液反应的化学方程式为:________ 。
| ① | ② | ③ | |||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | |||||||||||||||||
(1)①~⑨中,单质化学性质最不活泼的是
(2)②、③、④的简单离子按离子半径从小到大排列顺序为
(3)④在③单质中燃烧的产物的电子式为
(4)⑤的原子结构示意图为
(5)②和⑦形成一种化合物分子,各原子均达到8电子稳定结构,则该化合物的化学式为
(6)②、③的最简单氢化物中,沸点较高的是
(7)②的简单氢化物与②的最高价氧化物的水化物溶液反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】I、下表为长式周期表的一部分,其中的编号代表对应的元素。请依据下表回答下列问题:

(1)写出元素⑩的一价离子的核外电子排布式:___________ ,该元素属于___________ 区元素。
(2)在标号 的主族元素 中,电负性最大的是___________ (填元素符号 )。
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱 的顺序为:___________ (填化学式 )。
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式___________ 。
II.利用如图装置可验证同主族元素非金属性的变化规律。

(5)仪器A的名称为___________ 。
(6)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是___________ ,此装置存在的不足之处是___________ 。

(1)写出元素⑩的一价离子的核外电子排布式:
(2)在
(3)元素④⑥⑦的气态氢化物热稳定性由
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
II.利用如图装置可验证同主族元素非金属性的变化规律。

(5)仪器A的名称为
(6)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】氮化硅(Si3N4)耐高温、硬度大,可用石英与焦炭在1400~1450℃的氮气中合成:3SiO2(s)+6C(s)+2N2(g)  Si3N4(s)+6CO(g) -Q(Q>0)
Si3N4(s)+6CO(g) -Q(Q>0)
(1)该反应中所涉及物质属于非极性分子的电子式为_____ 。硅元素在周期表中的位置是_____ ,其原子的最外层电子轨道表示式为_____ ,最外层有______ 种运动状态不同的电子。
(2)反应的主要产物氮化硅所属的晶体类型为_____ 。例举一个化学事实说明氮元素比硅元素非金属性强_____ ,并从原子结构角度解释两元素的非金属性强弱关系______ 。
(3)碳元素形成的单质有金刚石、足球烯(分子式为C60)等。金刚石的熔点远高于足球烯的原因是___ 。
(4)叠氮化钠(NaN3)是一种无色结晶,其固体中阴阳离子的个数比为1:1,则该固体中含有的化学键是____ (填化学键名称)。叠氮化钠受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生 40.32 L(标准状况下)氮气,至少需要叠氮化钠____ g。
 Si3N4(s)+6CO(g) -Q(Q>0)
Si3N4(s)+6CO(g) -Q(Q>0)(1)该反应中所涉及物质属于非极性分子的电子式为
(2)反应的主要产物氮化硅所属的晶体类型为
(3)碳元素形成的单质有金刚石、足球烯(分子式为C60)等。金刚石的熔点远高于足球烯的原因是
(4)叠氮化钠(NaN3)是一种无色结晶,其固体中阴阳离子的个数比为1:1,则该固体中含有的化学键是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如表是元素周期表的一部分,请据表标注的元素回答(用相应的化学符号作答):

(1)形成单质不含化学键的是_____ (填化学式)。
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是_____ (填化学式)。
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为_____ (用物质化学式表示)。
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为_____ (用离子符号表示)。
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有_____ 。
(6)写出由元素a、e、g组成的化合物的电子式:_____ 。
(7)写出由元素b、e组成的化合物be2的结构式:_____ 。
(8)下列不能说明氯元素的非金属性比硫元素强的是_____ (填字母)。

(1)形成单质不含化学键的是
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有
(6)写出由元素a、e、g组成的化合物的电子式:
(7)写出由元素b、e组成的化合物be2的结构式:
(8)下列不能说明氯元素的非金属性比硫元素强的是
| A.氯、硫的最低负价分别为-1、-2 |
| B.硫化氢在300℃时开始分解,HCl在1500℃时开始缓慢分解 |
| C.HClO4的酸性比H2SO3的强 |
| D.向Na2S水溶液中通入Cl2有淡黄色沉淀生成 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】几种主族元素在周期表中的位置如下,根据上表回答下列问题:

(1)⑥元素的简单氢化物是_______ (填化学式),该氢化物的电子式是_______ 。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的 3 倍,该元素的原子结构示意图为_______ , 该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式),①与水反应的化学方程式为_______ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与①元素形成的物质的化学式是_______ ,该物质所含的化学键是_______ 。

(1)⑥元素的简单氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的 3 倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(6)④与①元素形成的物质的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】短周期主族元素①~⑧在元素周期表中的位置如图所示。
请按要求回答下列问题:
(1)元素①在周期表中的位置为_______ 。
(2)元素②、④形成的化合物A呈淡黄色,则A中所含的化学键类型为_______ 。
(3)元素⑦、⑧二者最高价氧化物对应水化物的酸性较强的是_______ 。(填化学式)
(4)元素③、⑥、⑧简单离子半径由大到小的顺序为_______ 。(填离子符号)
(5)元素Tl与⑥同主族,下列关于Tl的说法正确的是_______。(填序号)
| ① | ② | ③ | |||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)元素①在周期表中的位置为
(2)元素②、④形成的化合物A呈淡黄色,则A中所含的化学键类型为
(3)元素⑦、⑧二者最高价氧化物对应水化物的酸性较强的是
(4)元素③、⑥、⑧简单离子半径由大到小的顺序为
(5)元素Tl与⑥同主族,下列关于Tl的说法正确的是_______。(填序号)
| A.原子最外层有3个电子 | B.最高价氧化物对应水化物为两性氢氧化物 |
| C.单质不能与稀盐酸反应 | D.单质的还原性比⑥强 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语 回答下列问题。

(1)元素①的原子结构示意图为_______ 。
(2)元素③和⑥可形成化合物,用电子式表示形成其过程_______ 。
(3)元素②、③形成简单离子的半径(填离子符号)_______ >_______ 。
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)_______ >_______ ;元素③、④形成的最高价氧化物水化物的碱性_______ >_______ 。
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式_______ 。
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式_______

(1)元素①的原子结构示意图为
(2)元素③和⑥可形成化合物,用电子式表示形成其过程
(3)元素②、③形成简单离子的半径(填离子符号)
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式
您最近一年使用:0次



