实验发现加入M能提高 和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
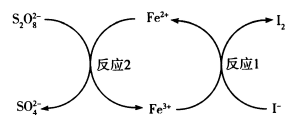
 和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
和I-的反应速率,其原理如图所示,依次发生反应1、2,下列说法正确的是
| A.M可能是Fe(OH)3 |
| B.Fe2+是该反应的催化剂 |
| C.反应1为2Fe3++2I-=2Fe2++I2 |
D.将反应2设计成原电池, 在负极反应 在负极反应 |
更新时间:2021/07/21 17:19:58
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3═bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法不正确的是
| A.由反应可推断氧化性:HClO4<HClO3 |
| B.变蓝的淀粉碘化钾试纸褪色是因为可能发生了:5Cl2+I2+6H2O═12H++10Cl-+2IO3- |
| C.若氯酸分解所得混合气体,1 mol混合气体质量为47.6 g,则反应方程式可表示为26HClO3 ═15O2↑+8Cl2↑+10HClO4+8H2O |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硼单质及其化合物有重要的应用。硼晶体熔点为2076℃,可形成多种卤化物。 可与
可与 反应生成
反应生成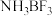 。
。 可与
可与 反应生成乙硼烷
反应生成乙硼烷 (标准燃烧热为
(标准燃烧热为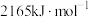 ),其分子中一个硼与周围的四个氢形成正四面体,结构式为
),其分子中一个硼与周围的四个氢形成正四面体,结构式为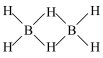 ,具有还原性。乙硼烷易水解生成
,具有还原性。乙硼烷易水解生成 与
与 ,
, 是一种一元弱酸,可作吸水剂。乙硼烷可与
是一种一元弱酸,可作吸水剂。乙硼烷可与 反应生成氨硼烷(
反应生成氨硼烷(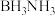 ),其在一定条件下可以脱氢,最终得到BN。乙硼烷也可与NaH反应生成
),其在一定条件下可以脱氢,最终得到BN。乙硼烷也可与NaH反应生成 ,是一种常用的还原剂。下列物质的结构、性质、用途之间
,是一种常用的还原剂。下列物质的结构、性质、用途之间
A.B电负性小于H, 可用作还原剂 可用作还原剂 | B. 有弱酸性,可用作吸水剂 有弱酸性,可用作吸水剂 |
C. 中B有空轨道,易与 中B有空轨道,易与 形成 形成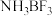 | D.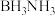 可以脱氢,可用作储氢材料 可以脱氢,可用作储氢材料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验、现象与结论正确且相符的是( )
| 实验 | 现象 | 结论 | |
| A | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应: 2NO2 (g)  N2O4(g)ΔH<0 N2O4(g)ΔH<0 |
| C | SO2通入新制氯水 | 溶液褪色 | SO2具有漂白性 |
| D | 向2支盛有2mL相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液 | 一支无明显现象,另一支产生黄色沉淀 | 相同条件下,AgI比AgCl的溶解度大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国科学家开发了FeCo-NSC催化剂,设计一种新型锌-空气电池,装置如图所示。
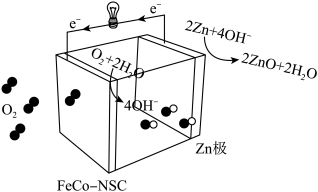
放电时,下列说法错误的是

放电时,下列说法错误的是
| A.“FeCo-NSC”能降低正极反应的活化能 |
B.正极反应式为 |
C. 向Zn极附近迁移 向Zn极附近迁移 |
| D.右侧电极电势比左侧电极高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有人设计出利用CH4和O2反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法中正确的是
①每消耗1molCH4可以向外电路提供8mol e—
②电池放电时,溶液pH不断升高
③负极上是O2获得电子,电极反应式为:O2+2H2O+4e—=4OH—
④负极上CH4失去电子,电极反应式为:CH4+10OH——8e—= +7H2O
+7H2O
①每消耗1molCH4可以向外电路提供8mol e—
②电池放电时,溶液pH不断升高
③负极上是O2获得电子,电极反应式为:O2+2H2O+4e—=4OH—
④负极上CH4失去电子,电极反应式为:CH4+10OH——8e—=
 +7H2O
+7H2O| A.①④ | B.①③ | C.①② | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电子表中电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应式为:Ag2O+Zn+H2O=2Ag+Zn(OH)2.下列说法不正确的是
| A.锌是负极,氧化银是正极 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.溶液中OH-向负极移动,K+、H+向正极移动 |
| D.随着电极反应的不断进行,电解质溶液的pH会增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用如图所示装置可以将温室气体CO2转化为燃料气体CO,下列说法不正确的是
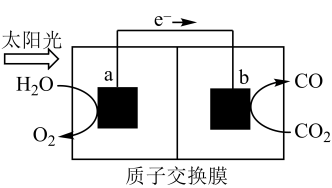

| A.电池工作时a极区溶液的pH降低 |
| B.电极b表面发生反应CO2+2e-+2H+=CO+H2O |
| C.该装置工作时,H+从a极区向b极区移动 |
| D.标准状况下,电极a生成1.12LO2时,两极电解质溶液质量相差3.2g |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
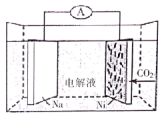
【推荐2】我国科学学研发了一种室温下“可呼吸”的Na-CO2二次电池,其原理如图所示。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na 2Na2CO3+C,下列说法正确的是
2Na2CO3+C,下列说法正确的是
 2Na2CO3+C,下列说法正确的是
2Na2CO3+C,下列说法正确的是
| A.放电时,Na电极为负极,发生还原反应 |
| B.充电时,Na+向阳极区移动 |
| C.充电时,阳极电极反应为:C+O2--4e-=CO2 |
| D.放电时,理论上当外电路通过0.1 mole-时,正极区消耗CO2体积1.68L(标准状况下) |
您最近一年使用:0次

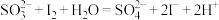 。某溶液中可能含有
。某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 ,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断错误的是
,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断错误的是 可在催化剂
可在催化剂 或
或 作用下产生·OH,·OH能将烟气中的NO、
作用下产生·OH,·OH能将烟气中的NO、 氧化。·OH产生机理如下:
氧化。·OH产生机理如下: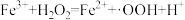 (慢反应);
(慢反应);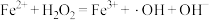 (快反应)。
(快反应)。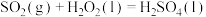 ,下列有关说法不正确的是
,下列有关说法不正确的是 ,
,
 不变
不变



 向锂电极迁移
向锂电极迁移

