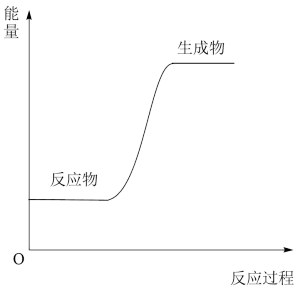
有关下列图像的叙述不正确的是


| A.图(1)表示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=-41kJ·mol-1 |
| B.图(2)表示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=+41kJ·mol-1 |
| C.由图可知正逆反应的热效应的数值相同 |
| D.两个图像表示的含义不 |
18-19高三上·陕西西安·阶段练习 查看更多[6]
甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(A班)化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(B班)化学试题江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷A卷化学试题(已下线)1.1.1 化学反应的焓变-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)广东省揭阳市揭西县河婆中学2020-2021学年高二上学期第一次月考化学试题【全国百强校】陕西省西安市长安区第一中学2019届高三上学期第二次检测化学试题
更新时间:2021-07-27 23:02:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的组合是( )
①氢元素有三种核素H、D、T,它们互称为同位素,HD属于化合物
②吸热反应必须加热才能完成
③化学反应过程包括旧化学键断裂和新化学键形成的过程
④石墨变金刚石要吸热,故金刚石比石墨稳定
⑤铅蓄电池工作时两极的质量均增加
⑥燃煤发电的能量转化关系为化学能→热能→机械能→电能
⑦可在周期表金属和非金属的分界处寻找半导体材料,如硅、锗等
⑧1mol酸和1mol碱发生中和反应生成水所释放的热量叫中和热
⑨碱性锌锰电池属于二次电池
⑩NH3和HCl的化合反应与NH4Cl的分解反应称为可逆反应
①氢元素有三种核素H、D、T,它们互称为同位素,HD属于化合物
②吸热反应必须加热才能完成
③化学反应过程包括旧化学键断裂和新化学键形成的过程
④石墨变金刚石要吸热,故金刚石比石墨稳定
⑤铅蓄电池工作时两极的质量均增加
⑥燃煤发电的能量转化关系为化学能→热能→机械能→电能
⑦可在周期表金属和非金属的分界处寻找半导体材料,如硅、锗等
⑧1mol酸和1mol碱发生中和反应生成水所释放的热量叫中和热
⑨碱性锌锰电池属于二次电池
⑩NH3和HCl的化合反应与NH4Cl的分解反应称为可逆反应
| A.①③⑥⑨ | B.③⑤⑥⑦ | C.②③⑧⑨ | D.①③④⑦⑩ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
A.已知 , , ,则a<b ,则a<b |
B. 、 、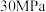 下,将 下,将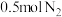 和 和 置于密闭容器中反应生成 置于密闭容器中反应生成 ,放热 ,放热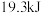 ,其热化学方程式为 ,其热化学方程式为 |
| C.等质量的硫固体和硫蒸汽分别完全燃烧,前者放出的热量少 |
D.已知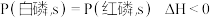 ,则白磷比红磷稳定 ,则白磷比红磷稳定 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
A.甲烷的燃烧热为 890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+ O2(g) ═ 3CO(g) + 2H2O(l) △H = -890.3 kJ/mol O2(g) ═ 3CO(g) + 2H2O(l) △H = -890.3 kJ/mol |
| B.已知稀溶液中,H+(aq)+OH-(aq)= H2O(l) ΔH=-57.3 kJ/mol,则稀醋酸与稀氢氧化钠溶液反应生成1mol 水时放出的热量大于 57.3kJ |
C.500℃下,将 0.5mol I2(g)和 0.5molH2(g)置于密闭的容器中充分反应生成 HI(g),放热 10kJ,其热化学方程式为:I2(g) + H2(g) 2HI(g) △H = -20 kJ/mol 2HI(g) △H = -20 kJ/mol |
| D.已知 25℃、101kPa 条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9 kJ/mol,4Al(s) + 2O3(g) ═2A12O3(s) △H = -3119.1 kJ/mol,所以,O2比O3稳定 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学研究所报道了化合物1催化 氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
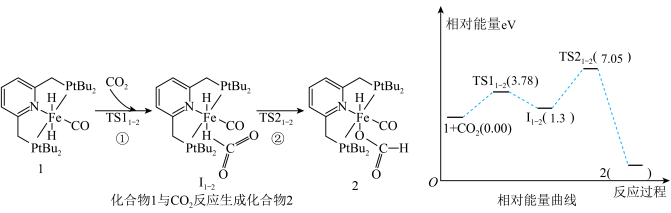
 氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
A.化合物 是该过程的催化剂 是该过程的催化剂 |
B.图中化合物1和 的总能量小于化合物2的总能量 的总能量小于化合物2的总能量 |
| C.化合物2中,CO作为配体,由C原子提供孤电子对 |
D.过程①的热化学方程式为: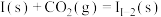  |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知:
①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
①CO(g)+1/2O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
| A.通常状况下,氢气的燃烧热为241.8 kJ·mol-1 |
| B.由①可知,1 mol CO(g)和1/2 mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量 |
C.可用右图表示2CO2(g)===2CO(g)+O2(g)反应过程中的能量变化关系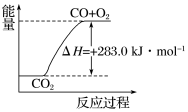 |
| D.分解1 mol H2O(g),其反应热为-241.8 kJ |
您最近半年使用:0次
【推荐1】化学反应中的能量变化常表现为热量变化,如有的反应为放热反应,有的为吸热反应,请从下列选项中选出对此解释合理的为
| A.旧化学键断裂时吸收的能量高于新化学键形成时所释放的总能量为吸热反应 |
| B.旧化学键断裂时吸收的能量低于新化学键形成时所释放的总能量为吸热反应 |
| C.在化学反应中需要加热的反应就是吸热反应 |
| D.在化学反应中需要使用催化剂的反应为放热反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法不正确的是
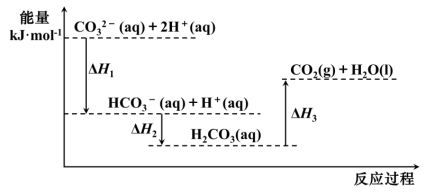

A.反应HCO (aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应 (aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应 |
| B.ΔH1<ΔH2,ΔH2<ΔH3 |
C.CO (aq)+2H+(aq)=CO2(g)+H2O(l) ΔH=ΔH1+ΔH2+ΔH3 (aq)+2H+(aq)=CO2(g)+H2O(l) ΔH=ΔH1+ΔH2+ΔH3 |
| D.H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则ΔH3变小 |
您最近半年使用:0次

 放出
放出 ,其反应历程如下图所示:
,其反应历程如下图所示: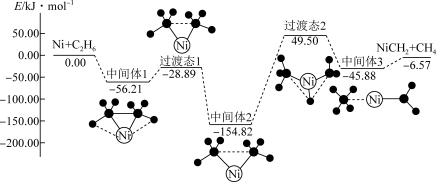
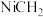 和
和