按要求填空
(1)标准状况下5.6L的CO2中含有的分子数为___________ ,含有的电子数为___________ (用NA表示)。
(2)在200mL0.5 mol∙L−1的Al2(SO4)3溶液中,Al3+的物质的量浓度是___________
(3)比较下列物质中氢原子数目多少(填“>”“<”或“=”):4.9g H2SO4___________ 3.6g H2O
(4)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:___________
(1)标准状况下5.6L的CO2中含有的分子数为
(2)在200mL0.5 mol∙L−1的Al2(SO4)3溶液中,Al3+的物质的量浓度是
(3)比较下列物质中氢原子数目多少(填“>”“<”或“=”):4.9g H2SO4
(4)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:
20-21高一上·内蒙古巴彦淖尔·期中 查看更多[2]
更新时间:2021-07-28 15:46:28
|
相似题推荐
计算题
|
较易
(0.85)
名校
【推荐1】请将下列表格填写完整.
| 标号 | 物质 | 分子(微粒)数 | 质量/g | 物质的量/mol | 体积/L |
| ⑴ | Cl2 | 71 | |||
| ⑵ | H2SO4 | 0.5 | |||
| ⑶ | H2O | 3.01×1023 | |||
| ⑷ | NaCl | 1.204×1022 |
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】化学计量在化学中占有重要地位,请回答下列问题(用NA表示阿伏加德罗常数):
(1)质量为3.6g的NH 离子含有的电子数为
离子含有的电子数为___________
(2)4.8g CH4中所含氢原子的物质的量为___________
(3)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为___________
(4)同温同压下,有0.4mol O3与0.6mol O2,它们的体积之比为___________ 。
(5)1mol Na2SO4溶于水能电离出___________ 个Na+;若5L Al2(SO4)3溶液中含Al3+离子数目为4NA个,则含SO 离子的物质的量浓度
离子的物质的量浓度___________ mol·L−1。
(1)质量为3.6g的NH
 离子含有的电子数为
离子含有的电子数为(2)4.8g CH4中所含氢原子的物质的量为
(3)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为
(4)同温同压下,有0.4mol O3与0.6mol O2,它们的体积之比为
(5)1mol Na2SO4溶于水能电离出
 离子的物质的量浓度
离子的物质的量浓度
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)0.5mol CH4含______ 个分子,含______ 个电子;
(2)硫酸的摩尔质量是________ ,24.5 g硫酸的物质的量是________ ,
(3)同温同压下,等物质的量H2S、NH3、CH4 三种气体的体积之比为________ 。
(4)现有100mL 0.3mol/L氯化铁溶液,用量筒量取10mL溶液,其中氯离子的浓度为_____ 。在沸水中滴入饱和氯化铁的水溶液,继续煮沸可制得一种红褐色胶体,生成的胶体直径一般为1nm至______ nm之间
(2)硫酸的摩尔质量是
(3)同温同压下,等物质的量H2S、NH3、CH4 三种气体的体积之比为
(4)现有100mL 0.3mol/L氯化铁溶液,用量筒量取10mL溶液,其中氯离子的浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)该气体所含原子总数为__________ 个。
(3)该气体在标准状况下的体积为____________ L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为___________ 。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_______ mol/L。
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解)。试计算:
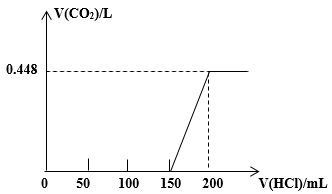
(1)盐酸的物质的量浓度为_______ mol/L;
(2)该样品中混合物的成分及其物质的量之比为_______ 。

(1)盐酸的物质的量浓度为
(2)该样品中混合物的成分及其物质的量之比为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】(1)1.204×1024个H2SO4分子共含_______ 个氢原子。将上述H2SO4溶于水配成600 mL溶液,再加水稀释到1000 mL,稀释后溶液的物质的量浓度为_______ mol/L。
(2)22 gNa2R2中含0.4 mol的Na+,则R的相对原子质量是_____________ 。
(3)把100mL0.3mol/LNa2SO4溶液和400mL0.2mol/LNaCl溶液混合后,溶液中Na+的物质的量浓度为_____________ (假设混合时溶液体积变化忽略不计)
(4)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5 mol/L,SO42-浓度为0.9 mol/L,则K+的物质的量浓度为_______________ mol/L。
(5)把标准状况下V L气体(摩尔质量M g/mol)溶于1 L水中(不考虑反应),所得溶液密度为ρg/cm3,则此溶液的物质的量浓度为__________________ 。
(2)22 gNa2R2中含0.4 mol的Na+,则R的相对原子质量是
(3)把100mL0.3mol/LNa2SO4溶液和400mL0.2mol/LNaCl溶液混合后,溶液中Na+的物质的量浓度为
(4)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5 mol/L,SO42-浓度为0.9 mol/L,则K+的物质的量浓度为
(5)把标准状况下V L气体(摩尔质量M g/mol)溶于1 L水中(不考虑反应),所得溶液密度为ρg/cm3,则此溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】回答下列问题
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)_______ ,质量最大的是_______ ,体积最小的是_______ 。
(2)同温同压下,质量相同的CO和CH4气体的体积之比为_______ 。
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是_______ 。
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)
(2)同温同压下,质量相同的CO和CH4气体的体积之比为
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】试回答下列问题
(1)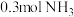 ,分子中所含质子数与
,分子中所含质子数与___________ 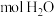 分子中所含质子数相等。
分子中所含质子数相等。
(2)正常人的血液中葡萄糖(简称血糖,分子式为 )的浓度在
)的浓度在 之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于
之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于___________ 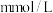 。
。
(3)质量分数为36.5%浓盐酸(密度为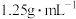 )的物质的量浓度为
)的物质的量浓度为___________ ,若配制250mL 的盐酸,需要量取浓盐酸的体积为
的盐酸,需要量取浓盐酸的体积为___________ mL。
(1)
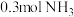 ,分子中所含质子数与
,分子中所含质子数与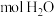 分子中所含质子数相等。
分子中所含质子数相等。(2)正常人的血液中葡萄糖(简称血糖,分子式为
 )的浓度在
)的浓度在 之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于
之间,今测得某病人1mL血液中含葡萄糖0.60mg,相当于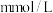 。
。(3)质量分数为36.5%浓盐酸(密度为
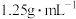 )的物质的量浓度为
)的物质的量浓度为 的盐酸,需要量取浓盐酸的体积为
的盐酸,需要量取浓盐酸的体积为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐3】以物质的量为中心的相关计算,已知阿伏加 德罗常数为 .
.
(1)质量相同的 、
、 、
、 、
、 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是______________ ,含有原子数最多的是______________ ,在相同温度和相同压强条件下,体积最大的是______________ 。
(2)23.75g某 价金属的氯化物(
价金属的氯化物( )中含有
)中含有 个
个 ,则M的摩尔质量为
,则M的摩尔质量为_____________ g/mol。
(3)将标准状况下的aL 溶于100g水中,得到 的盐酸密度为
溶于100g水中,得到 的盐酸密度为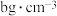 ,则该盐酸的物质的量浓度是
,则该盐酸的物质的量浓度是______________ mol/L。
(4)某 溶液1mL中含有0.81克
溶液1mL中含有0.81克 ,取出
,取出 mL溶液稀释成3mL后,硫酸根离子的物质的量浓度为
mL溶液稀释成3mL后,硫酸根离子的物质的量浓度为______________ mol/L。
 .
.(1)质量相同的
 、
、 、
、 、
、 四种气体中,含有分子数目最少的是
四种气体中,含有分子数目最少的是(2)23.75g某
 价金属的氯化物(
价金属的氯化物( )中含有
)中含有 个
个 ,则M的摩尔质量为
,则M的摩尔质量为(3)将标准状况下的aL
 溶于100g水中,得到 的盐酸密度为
溶于100g水中,得到 的盐酸密度为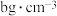 ,则该盐酸的物质的量浓度是
,则该盐酸的物质的量浓度是(4)某
 溶液1mL中含有0.81克
溶液1mL中含有0.81克 ,取出
,取出 mL溶液稀释成3mL后,硫酸根离子的物质的量浓度为
mL溶液稀释成3mL后,硫酸根离子的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】将117gNaCl溶于水配成1L溶液。求:
(1)该溶液中NaCl的物质的量浓度___ ;
(2)配制1mol/L的NaCl溶液500mL,需要该溶液的体积___ 。
(1)该溶液中NaCl的物质的量浓度
(2)配制1mol/L的NaCl溶液500mL,需要该溶液的体积
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】把质量分数为98%密度为1.84g/cm3的浓H2SO4配制成500ml0.5mol/L的稀H2SO4,计算:
(1)浓H2SO4的物质的量浓度是多少?_____
(2)所需浓H2SO4的体积是多少?_____ (写出相关公式及计算过程)
(1)浓H2SO4的物质的量浓度是多少?
(2)所需浓H2SO4的体积是多少?
您最近一年使用:0次



