回答下列问题
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)_______ ,质量最大的是_______ ,体积最小的是_______ 。
(2)同温同压下,质量相同的CO和CH4气体的体积之比为_______ 。
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是_______ 。
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)
(2)同温同压下,质量相同的CO和CH4气体的体积之比为
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是
更新时间:2024-02-08 17:29:44
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】2 mol O3和3 mol O2的质量之比________ ,分子数之比________ ,同温同压的密度之比为________ ,含氧原子数之比为________ ,体积之比为________ 。
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】(1)标况下5.6L的CO2质量为 _____ g,其中含有______ 个分子,含有_____ 个原子;
(2)质量均为m g的 HCl、NH3、CO2、O2四种气体,所含分子数目最少的是_________ ,体积最大的是_____ ,密度最小的是_______ (在相同温度和压强条件下)。
(2)质量均为m g的 HCl、NH3、CO2、O2四种气体,所含分子数目最少的是
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】标况下11.2L CH4的质量是____ g,其中含有H数目为_____ 个。
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】向含0.002molCa(OH)2的澄清石灰水中,通入标准状况下的二氧化碳气体67.2mL,求生成沉淀的质量________ 。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】“84”消毒液能有效杀灭新型冠状病毒,某同学购买了一瓶“84”消毒液,其说明中有如下信息:NaClO质量分数25%、密度1.20g•cm-3、1000mL,稀释后使用。请根据信息和相关知识回答下列问题:
(1)该“84”消毒液中 NaClO的物质的量浓度为_______ mol•L-1。(保留至小数点后一位)
(2)现实验室需要480mL 0.4mol•L-1的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液,应用托盘天平称取 NaClO固体_______ g。
(3)若用氯气和氢氧化钠反应制备NaClO,理论上每消耗标准状况下22.4L Cl2,转移电子总数为_______ 。
(4)工业上常利用次氯酸钠在碱性条件下氧化三价铁离子来制备高铁酸钠(Na2FeO4),若过程中消耗3mol NaClO,则制得Na2FeO4的物质的量为_______ mol。
(1)该“84”消毒液中 NaClO的物质的量浓度为
(2)现实验室需要480mL 0.4mol•L-1的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液,应用托盘天平称取 NaClO固体
(3)若用氯气和氢氧化钠反应制备NaClO,理论上每消耗标准状况下22.4L Cl2,转移电子总数为
(4)工业上常利用次氯酸钠在碱性条件下氧化三价铁离子来制备高铁酸钠(Na2FeO4),若过程中消耗3mol NaClO,则制得Na2FeO4的物质的量为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】完成下列填空:
(1) 个氨分子的物质的量是
个氨分子的物质的量是_______ mol,标准状况下的体积是_______ L,质量为_______ g。
(2)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO 的物质的量浓度为
的物质的量浓度为_______ mol/L;
(3)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为_______ 。
(4)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和0.2mol E物质,则E物质的摩尔质量为_______ 。
(5)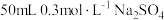 溶液和
溶液和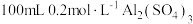 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(6)某盐混合溶液中含有离子: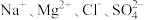 ,测得
,测得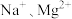 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
_______ 。
(1)
 个氨分子的物质的量是
个氨分子的物质的量是(2)VLFe2(SO4)3溶液中含Fe3+mg,则溶液中SO
 的物质的量浓度为
的物质的量浓度为(3)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量为
,含有0.6mol氯离子,则金属R的相对原子质量为(4)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和0.2mol E物质,则E物质的摩尔质量为
(5)
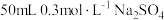 溶液和
溶液和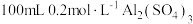 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(6)某盐混合溶液中含有离子:
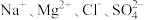 ,测得
,测得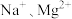 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐2】按要求填空
(1)标准状况下5.6L的CO2中含有的分子数为___________ ,含有的电子数为___________ (用NA表示)。
(2)在200mL0.5 mol∙L−1的Al2(SO4)3溶液中,Al3+的物质的量浓度是___________
(3)比较下列物质中氢原子数目多少(填“>”“<”或“=”):4.9g H2SO4___________ 3.6g H2O
(4)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:___________
(1)标准状况下5.6L的CO2中含有的分子数为
(2)在200mL0.5 mol∙L−1的Al2(SO4)3溶液中,Al3+的物质的量浓度是
(3)比较下列物质中氢原子数目多少(填“>”“<”或“=”):4.9g H2SO4
(4)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:
您最近一年使用:0次

 )与5体积的水混合得到一种稀硫酸,试计算该硫酸(密度
)与5体积的水混合得到一种稀硫酸,试计算该硫酸(密度 )物质的量浓度
)物质的量浓度

