已知X和Y、Z为中学化学中的常见元素,根据如图所示转化关系(反应条件及部分产物已略去),回答以下问题。
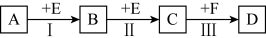
(1)若A、B、C、D均为含X的化合物,且A常用作制冷剂,D是一种强酸,则
①写出工业制备A的化学反应方程式:___________ 。
②将16 g铜粉与一定量的D的稀溶液反应后,收集到896 mL无色气体(标准状况),则被还原的D的物质的量为___________ mol。向所得溶液中继续加稀硫酸至反应不能再进行,需加入含___________ mol H2SO4的稀硫酸。
(2)若A、B、C、D均为含Y的化合物,其中A是一元强碱且焰色为黄色,E是有刺激性气味的气态酸性氧化物,则B的化学式为___________ ;A与C反应的离子方程式为___________ 。
(3)若A、B、C、D均为含Z的化合物,其中A由两种元素组成,且A的摩尔质量为34 g/mol,D为强酸。将Na2Z溶液滴加到NaClO溶液中,有淡黄色沉淀生成,请写出所发生反应的离子方程式:___________ 。
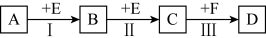
(1)若A、B、C、D均为含X的化合物,且A常用作制冷剂,D是一种强酸,则
①写出工业制备A的化学反应方程式:
②将16 g铜粉与一定量的D的稀溶液反应后,收集到896 mL无色气体(标准状况),则被还原的D的物质的量为
(2)若A、B、C、D均为含Y的化合物,其中A是一元强碱且焰色为黄色,E是有刺激性气味的气态酸性氧化物,则B的化学式为
(3)若A、B、C、D均为含Z的化合物,其中A由两种元素组成,且A的摩尔质量为34 g/mol,D为强酸。将Na2Z溶液滴加到NaClO溶液中,有淡黄色沉淀生成,请写出所发生反应的离子方程式:
更新时间:2021-08-06 10:47:34
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,
它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素,C是当今产量和用量最多的金属。请回答下列问题:

(1)写出金属B和气体丙的化学式______________ 、 ____________ 。
(2)写出反应①的化学反应方程式________________________________________ 。
(3)沉淀H的化学式为_______________ 。
(4)往溶液G中滴入KSCN溶液,现象是_________________________
它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素,C是当今产量和用量最多的金属。请回答下列问题:

(1)写出金属B和气体丙的化学式
(2)写出反应①的化学反应方程式
(3)沉淀H的化学式为
(4)往溶液G中滴入KSCN溶液,现象是
您最近一年使用:0次
【推荐2】下图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、H、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。
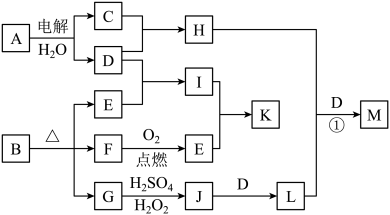
根据以上信息,回答下列问题:
(1)B的组成元素为_____ 。
(2)鉴别等物质的量浓度的I、K稀溶液的实验方法为_____ 。
(3)G→J的离子方程式为_____ 。
(4)M是含氧酸盐,反应①中H、L、D的物质的量之比为3:2:4,则M的化学式为_____ 。

根据以上信息,回答下列问题:
(1)B的组成元素为
(2)鉴别等物质的量浓度的I、K稀溶液的实验方法为
(3)G→J的离子方程式为
(4)M是含氧酸盐,反应①中H、L、D的物质的量之比为3:2:4,则M的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A-F为中学化学常见物质,它们的焰色实验均为黄色。其中A为单质,B与C的组成元素相同,且B为淡黄色固体;D、E、F的溶液均显碱性,其中E和F属于盐,E被广泛用于玻璃、造纸和纺织等。它们之间的相互转化关系如下图。(“”表示一步反应即可转化,部分反应物、生成物和反应条件已略去)
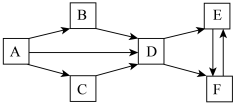
请回答下列问题:
(1)写出下列物质的化学式:B___ ,C___ ,E___ 。
(2)AD的化学方程式是___ 。
(3)BD的化学方程式是___ 。
(4)区分E和F两种固体的方法是:分别取等量的E和F两种固体少许于试管中,操作,现象和结论是___ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)AD的化学方程式是
(3)BD的化学方程式是
(4)区分E和F两种固体的方法是:分别取等量的E和F两种固体少许于试管中,操作,现象和结论是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】亚硝酸钙 是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):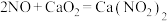 ;
; 。
。
请回答下列问题:
(1)请写出装置A中发生的化学反应方程式___________ 。
(2)装置D中盛装无水氯化钙的仪器名称是___________ ;装置B所加试剂是___________ 。
(3)加入稀硝酸之前,应向装置中通入一段时间的 ,原因是
,原因是___________ 。
(4)将 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为___________ mol。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为
,反应原理为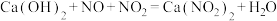 。其部分工艺流程如图所示:
。其部分工艺流程如图所示: 的物质的量之比接近1∶1。
的物质的量之比接近1∶1。
①若 ,则会导致
,则会导致___________ ;
②若 ,则会导致
,则会导致___________ 。
③已知 溶液需要保持弱碱性,因为其与酸会发生分解,产生NO气体。取2.5g某样品加入过量的稀硫酸中,发生反应产生0.448L(标准状况)气体,则该样品的纯度是
溶液需要保持弱碱性,因为其与酸会发生分解,产生NO气体。取2.5g某样品加入过量的稀硫酸中,发生反应产生0.448L(标准状况)气体,则该样品的纯度是___________ 。(结果保留两位小数)
 是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去):
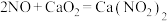 ;
; 。
。请回答下列问题:
(1)请写出装置A中发生的化学反应方程式
(2)装置D中盛装无水氯化钙的仪器名称是
(3)加入稀硝酸之前,应向装置中通入一段时间的
 ,原因是
,原因是(4)将
 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为(5)工业上可用石灰乳和硝酸工业的尾气(含NO、
 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为
,反应原理为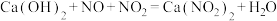 。其部分工艺流程如图所示:
。其部分工艺流程如图所示:
 的物质的量之比接近1∶1。
的物质的量之比接近1∶1。①若
 ,则会导致
,则会导致②若
 ,则会导致
,则会导致③已知
 溶液需要保持弱碱性,因为其与酸会发生分解,产生NO气体。取2.5g某样品加入过量的稀硫酸中,发生反应产生0.448L(标准状况)气体,则该样品的纯度是
溶液需要保持弱碱性,因为其与酸会发生分解,产生NO气体。取2.5g某样品加入过量的稀硫酸中,发生反应产生0.448L(标准状况)气体,则该样品的纯度是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则B的结构式是_________ ,用电子式表示B的形成过程_________________ 反应①的化学方程式为_______________ 。反应④的化学方程式为______________________ 。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是___________________

(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则B的结构式是
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】巴蜀中学趣味化学实验小组的同学通过“ 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.
实验一:验证 的还原性
的还原性
(1)红棕色气体是__________ 。(写化学式)
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加 溶液,溶液变为红色,该现象说明
溶液,溶液变为红色,该现象说明__________ 。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的 或
或 与溶液中的
与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。
【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ii.向甲中加入适量浓 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
iii.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
iv.继续向甲中加入浓 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。
(3)通入 的目的是
的目的是__________ 。
(4)铜与浓硝酸反应的化学方程式是__________________ 。
(5)装置乙的作用是_______________________ 。
(6)实验结论:溶液的深棕色可能是因为__________。
【反思与改进】
实验三:验证 的还原性
的还原性
(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有__________ 的试管中滴入几滴__________ ,振荡。
 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.实验一:验证
 的还原性
的还原性实验操作 | 预期现象 | 实验现象 |
向盛有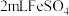 溶液的试管中,滴入几滴浓硝酸,振荡。 溶液的试管中,滴入几滴浓硝酸,振荡。 | 试管中产生红棕色气体,溶液变为黄色。 | 试管中产生红棕色气体,溶液变为深棕色。 |
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加
 溶液,溶液变为红色,该现象说明
溶液,溶液变为红色,该现象说明实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的
 或
或 与溶液中的
与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
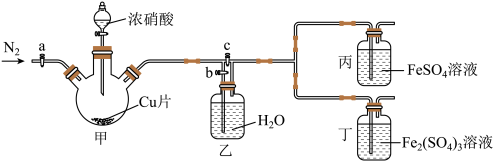
ii.向甲中加入适量浓
 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;iii.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
iv.继续向甲中加入浓
 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。(3)通入
 的目的是
的目的是(4)铜与浓硝酸反应的化学方程式是
(5)装置乙的作用是
(6)实验结论:溶液的深棕色可能是因为__________。
A. 与 与 发生了反应 发生了反应 | B. 与 与 发生了反应 发生了反应 |
C.Fe3+与 发生了反应 发生了反应 | D. 与 与 发生了反应 发生了反应 |
【反思与改进】
实验三:验证
 的还原性
的还原性(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C 外,另一产物是盐酸盐。

(1)A物质的化学式为_______ ,与A物质对应的酸式盐溶液与足量NaOH溶液加热条件下反应的离子方程式为_______ 。
(2)当X为强酸时,B的电子式为_______ ,B与D发生反应的化学方程式为_______ 。
(3)当X为强碱时,写出足量B与Cl2反应的化学方程式_______ 。
Ⅱ.金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:

已知气体D和F反应可生成盐。请回答下列问题:
(4)气体D和A溶液反应生成白色沉淀,该反应的离子方程式为_______ 。
(5)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,任意写出其中一个反应的化学方程式:_______ 。
(6)自来水中的 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,根据框图信息写出铝在碱性条件下与
,根据框图信息写出铝在碱性条件下与 反应的离子方程式:
反应的离子方程式:_______ 。
(7)除去气体C中的杂质气体E的化学方法:_______ (用化学方程式表示)。

(1)A物质的化学式为
(2)当X为强酸时,B的电子式为
(3)当X为强碱时,写出足量B与Cl2反应的化学方程式
Ⅱ.金属铝在酸性或碱性溶液中均可与
 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:
已知气体D和F反应可生成盐。请回答下列问题:
(4)气体D和A溶液反应生成白色沉淀,该反应的离子方程式为
(5)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,任意写出其中一个反应的化学方程式:
(6)自来水中的
 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原 ,根据框图信息写出铝在碱性条件下与
,根据框图信息写出铝在碱性条件下与 反应的离子方程式:
反应的离子方程式:(7)除去气体C中的杂质气体E的化学方法:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D均为中学所学的常见物质且均含有同一中元素,它们之间的转化关系如图所示(反应条件及其它物质已经略去):
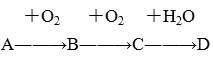
(1)若A是黄色晶体;B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为_____ ;体现B的_________ (填“氧化性”“还原性”“漂白性”);请写出D的浓溶液与单质铜反应的化学方程式:__________ ;此反应中作氧化剂的D与参加反应的D的物质的量之比为_____________ ;
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:_______________ ;请写出C→D的离子方程式_________________ 。
(3)若A是一种活泼金属,C是淡黄色固体,则C的名称为______ ,试用化学方程式表示该物质与二氧化碳气体的反应_______________ ;将C长期露置于空气中,最后将变成物质E,E的化学式为_______ 。
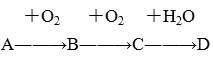
(1)若A是黄色晶体;B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:
(3)若A是一种活泼金属,C是淡黄色固体,则C的名称为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】氮的氧化物和硫的氧化物是导致酸雨的物质。
(1)形成酸雨的原理之一可简单表示如下:
回答下列问题:
①酸雨的pH________ (填“>”、“<”或“=”)5.6。
②D物质的化学式为____________ 。
③反应②的化学方程式为_________________________________________ 。
(2)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:__________________ ,反应中氧化剂是____________ ,还原剂是_______________ 。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
现有V L某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为________ mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=______ 。
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=________ 。
(1)形成酸雨的原理之一可简单表示如下:

回答下列问题:
①酸雨的pH
②D物质的化学式为
③反应②的化学方程式为
(2)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O
现有V L某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=
您最近一年使用:0次



