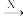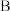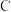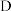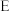A、B、C、D均为中学所学的常见物质且均含有同一中元素,它们之间的转化关系如图所示(反应条件及其它物质已经略去):
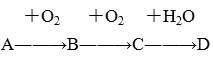
(1)若A是黄色晶体;B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为_____ ;体现B的_________ (填“氧化性”“还原性”“漂白性”);请写出D的浓溶液与单质铜反应的化学方程式:__________ ;此反应中作氧化剂的D与参加反应的D的物质的量之比为_____________ ;
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:_______________ ;请写出C→D的离子方程式_________________ 。
(3)若A是一种活泼金属,C是淡黄色固体,则C的名称为______ ,试用化学方程式表示该物质与二氧化碳气体的反应_______________ ;将C长期露置于空气中,最后将变成物质E,E的化学式为_______ 。
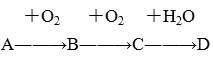
(1)若A是黄色晶体;B为酸雨的成因之一,且可使品红溶液褪色,则将B通入KMnO4溶液的现象为
(2)若A气体可使湿润的红色石蕊试纸变蓝,常温下D的浓溶液能使金属Fe、Al钝化,请写出实验室制备A的化学方程式:
(3)若A是一种活泼金属,C是淡黄色固体,则C的名称为
更新时间:2016-12-09 14:43:16
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有A、B、C、D、E、F六种物质的溶液,分别为NH3·H2O、NaHSO4、AlCl3、AgNO3、NaAlO2、NaOH中的一种,已知:
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答下列问题:
(1)写出下列化学式:A________ ;D_________ ;E_________ 。
(2)过量A溶液与B溶液反应的离子方程式为_____________________ 。
(3)将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为
________________________________________ 。
(4)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的大小关系为
_______________________________________ 。
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答下列问题:
(1)写出下列化学式:A
(2)过量A溶液与B溶液反应的离子方程式为
(3)将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为
(4)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的大小关系为
您最近一年使用:0次
【推荐2】现有金属单质A、B、C和气体甲、乙以及物质D、E、F、G、H,它们之间的相互转化关系如图 (图中有些反应的生成物和反应的条件没有标出)。
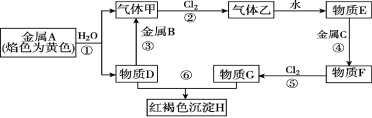
(1)写出下列物质的化学式:B_______ 、乙_______ 。
(2)写出下列反应的离子方程式:
反应①__________________________________________ ;
反应⑤__________________________________________ ;
反应⑥__________________________________________ 。
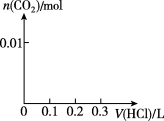
(3)将0.4 g D和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。在如图所示的坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象。________

(1)写出下列物质的化学式:B
(2)写出下列反应的离子方程式:
反应①
反应⑤
反应⑥
(3)将0.4 g D和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。在如图所示的坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象。

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
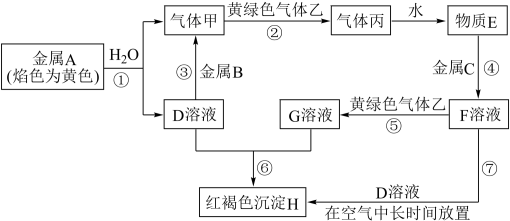
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B_______ ,丙_______ 。
(2)写出实验室制备黄绿色气体乙的化学方程式:_______ ,
(3)反应③中的离子方程式是_______
(4)反应⑤的离子方程式是_______
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:_______ 。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B
(2)写出实验室制备黄绿色气体乙的化学方程式:
(3)反应③中的离子方程式是
(4)反应⑤的离子方程式是
(5)反应⑦中如果可以长时间看到白色沉淀,应如何进行实验操作:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰化钾。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 _______ 。
②一段时间后,当观察到三颈烧瓶内_______ 时, 停止通入气体,反应完成。关闭K1和K2,将三颈烧瓶继续加热一段时间。
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为_______ 。
(2)制备KSCN晶体:
打开K3,_______ , 干燥,得到硫氰化钾晶体。(须用的试剂:5mol/LKOH、蒸馏水、稀硫酸)
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为_______ 。

已知:①CS2为不溶于水且密度比水大的非极性试剂。
②NH4HS、(NH4)2S 在热水中易分解生成NH3和H2S。
③装置B中,滴液漏斗中装有一定体积5mol/L KOH溶液。
回答下列问题:
(1)制备NH4SCN溶液:
①三颈烧瓶内盛放有76g CS2、水和难溶于水的固体做催化剂。实验开始时,打开K1,水浴加热装置B,发生反应CS2+ 3NH3
 NH4SCN + NH4HS, 则装置A中固体a的成分为
NH4SCN + NH4HS, 则装置A中固体a的成分为 ②一段时间后,当观察到三颈烧瓶内
③装置C中用酸性KMnO4溶液吸收尾气后得澄清溶液,H2S所发生反应的离子方程式为
(2)制备KSCN晶体:
打开K3,
(3)测定产品中KSCN的含量:
称取0.85g样品,配成100mL溶液。量取25.00mL溶液锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,滴定时发生的反应:SCN—+Ag+=AgSCN↓(白色)。达到滴定终点,三次滴定平均消耗AgNO3标准溶液20.00mL。产品中KSCN的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】上世纪30~40年代,侯德榜率技术团队突破外国公司垄断的索维尔制碱法的生成工艺,另辟蹊径,发明了侯氏联合制碱法,开创了世界制碱工业的新纪元。已知侯氏制碱法的主要原理为:
a. NaCl + NH3 + H2O + CO2 = NH4Cl + NaHCO3↓
b.2NaHCO3 Na2CO3 + CO2↑+ H2O
Na2CO3 + CO2↑+ H2O
(1)如图是某化学兴趣小组模拟“侯氏制碱法”制取NaHCO3的部分装置。为了提高CO2的利用率,须先向___________ (填“a”或“b”)管通入NH3,装置c中的试剂为___________ (填“碱石灰”“浓硫酸” 或“无水氯化钙”)。

(2)实验室给该兴趣小组提供了一份Na2CO3样品,为测定其纯度,小组成员设计了如下实验装置: B装置中盛有m1g碳酸钠样品( 假设杂质不参加反应,原装置中的CO2含量忽略不计,忽略CO2的溶解,各装置内反应完全)。实验室可供选择的试剂和药品还有Zn粒、稀硫酸、稀盐酸、CaCO3(s)。
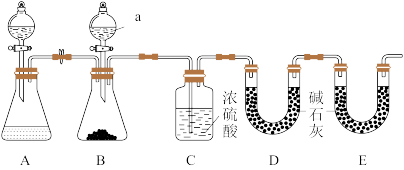
①仪器a的名称是___________ ,仪器a中所盛放的最佳试剂为___________ ,原因是___________ 。
②装置A的作用是___________ 。
③装置B中发生反应的离子方程式为___________ 。
④若无装置E,实验测定结果将___________ (填“偏高”“偏低”或“不变”),其原因是___________ 。若实验后,装置D增重m2g,则该碳酸钠样品的质量分数为___________ (用含m1、m2的代数式表示)。
a. NaCl + NH3 + H2O + CO2 = NH4Cl + NaHCO3↓
b.2NaHCO3
 Na2CO3 + CO2↑+ H2O
Na2CO3 + CO2↑+ H2O(1)如图是某化学兴趣小组模拟“侯氏制碱法”制取NaHCO3的部分装置。为了提高CO2的利用率,须先向

(2)实验室给该兴趣小组提供了一份Na2CO3样品,为测定其纯度,小组成员设计了如下实验装置: B装置中盛有m1g碳酸钠样品( 假设杂质不参加反应,原装置中的CO2含量忽略不计,忽略CO2的溶解,各装置内反应完全)。实验室可供选择的试剂和药品还有Zn粒、稀硫酸、稀盐酸、CaCO3(s)。

①仪器a的名称是
②装置A的作用是
③装置B中发生反应的离子方程式为
④若无装置E,实验测定结果将
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室用下图装置(夹持装置已省略)制备氨基甲酸铵(NH2COONH4)。已知:
①2NH3(g)+CO2(g) NH2COONH4(s)△H<0;
NH2COONH4(s)△H<0;
②NH2COONH4+H2O=(NH4)2CO3;
③常压下,CO2沸点—56.55℃,熔点—78.45℃。
请回答:

(1)装置A中发生的反应方程式是___________ 。
(2)装置B的名称为___________ ,装置B内盛放的试剂是___________ 。
(3)若无装置B,D中可能发生的副反应为___________ 。
(4)装置E的作用是___________ 。反应一段时间后,若发现E中有气体逸出,接下来具体操作是___________ 。
(5)用装置C代替稀盐酸与碳酸钙产生CO2的优点有___________ 。
A.可以升温,加快反应速率
B.得到的CO2无需干燥
C.有利于生成更多产品
(6)产品分析:称取1.976g样品(内含杂质(NH4)2CO3·H2O),溶于100mL容量瓶,用蒸馏水定容到刻度,每次取25mL试样于锥形瓶中进行滴定。已知滴定过程中发生以下反应:
NH2COONH4+H2O=(NH4)2CO3
(NH4)2CO3+BaCl2=2NH4Cl+BaCO3↓
4NH4Cl+6HCHO=(CH2)6N4+6H2O+4HClNaOH+HCl=NaCl+H2O
为避免碳酸钡的溶解,采用盐酸回滴过量的氢氧化钠标准液,计算氨基甲酸铵的氨含量。实验数据如下表:
氨基甲酸铵纯度为___________ 。(保留一位小数,已知氨基甲酸铵的摩尔质量为78g/mol)
①2NH3(g)+CO2(g)
 NH2COONH4(s)△H<0;
NH2COONH4(s)△H<0;②NH2COONH4+H2O=(NH4)2CO3;
③常压下,CO2沸点—56.55℃,熔点—78.45℃。
请回答:

(1)装置A中发生的反应方程式是
(2)装置B的名称为
(3)若无装置B,D中可能发生的副反应为
(4)装置E的作用是
(5)用装置C代替稀盐酸与碳酸钙产生CO2的优点有
A.可以升温,加快反应速率
B.得到的CO2无需干燥
C.有利于生成更多产品
(6)产品分析:称取1.976g样品(内含杂质(NH4)2CO3·H2O),溶于100mL容量瓶,用蒸馏水定容到刻度,每次取25mL试样于锥形瓶中进行滴定。已知滴定过程中发生以下反应:
NH2COONH4+H2O=(NH4)2CO3
(NH4)2CO3+BaCl2=2NH4Cl+BaCO3↓
4NH4Cl+6HCHO=(CH2)6N4+6H2O+4HClNaOH+HCl=NaCl+H2O
为避免碳酸钡的溶解,采用盐酸回滴过量的氢氧化钠标准液,计算氨基甲酸铵的氨含量。实验数据如下表:
| 加入NaOH物质的量(mmol) | 25.000 |
| 回滴消耗盐酸物质的量(mmol) | 12.925 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】下表是部分城市某日空气质量日报:
(1)由上表可知,空气质量日报中涉及的污染物主要是_______ 和可吸入颗粒物(PM10)。
(2)汽车尾气是城市大气中氮氧化物的主要来源之一,治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NO反应生成可参与大气生态环境循环的无毒气体,写出反应的化学方程式:_______ 。
(3)SO2的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:

请回答下列问题:
①酸雨的pH_______ (填“>”“<”或“=”)5.6。
②反应b的化学方程式为:_______ 。
③在一段时间内连续不断测定溶液D的pH,发现pH变小,表示该变化的化学方程式是:_______ 。
④若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:_______ 。
⑤现有某地含酸雨水样1 m3,其中c(H+)=0.005 mol·L-1,若用生石灰处理该水样至中性,理论上需生石灰_______ kg。
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
| SO2 | NO2 | PM10 | |||
| A | 98 | 23 | 67 | SO2 | Ⅱ |
| B | 47 | 29 | 35 | SO2 | Ⅰ |
| C | 62 | 80 | 113 | PM10 | Ⅲ |
| D | 52 | 76 | 59 | NO2 | Ⅰ |
(2)汽车尾气是城市大气中氮氧化物的主要来源之一,治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NO反应生成可参与大气生态环境循环的无毒气体,写出反应的化学方程式:
(3)SO2的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:

请回答下列问题:
①酸雨的pH
②反应b的化学方程式为:
③在一段时间内连续不断测定溶液D的pH,发现pH变小,表示该变化的化学方程式是:
④若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:
⑤现有某地含酸雨水样1 m3,其中c(H+)=0.005 mol·L-1,若用生石灰处理该水样至中性,理论上需生石灰
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系:
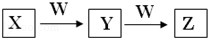
(1)若该反应是非氧化还原反应
①X为强碱溶液,W是形成酸雨的主要气体,则Y到Z的离子方程式为________________
②X是一种盐,焰色反应为黄色,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Y的化学式为_____________ .
③若W为一种强碱,Y具有两性,则向Z溶液中通入少量二氧化碳的离子方程式为_________________ .
(2)若该反应是氧化还原反应
①X常温下为黄绿色气体,W是生活中应用最广泛的金属之一,则Y的水溶液中加入W生成Z溶液的离子方程式为_________________________ .
②X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法_________________ ,X转化为Y的化学方程式为____________________ .
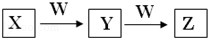
(1)若该反应是非氧化还原反应
①X为强碱溶液,W是形成酸雨的主要气体,则Y到Z的离子方程式为
②X是一种盐,焰色反应为黄色,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Y的化学式为
③若W为一种强碱,Y具有两性,则向Z溶液中通入少量二氧化碳的离子方程式为
(2)若该反应是氧化还原反应
①X常温下为黄绿色气体,W是生活中应用最广泛的金属之一,则Y的水溶液中加入W生成Z溶液的离子方程式为
②X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某化学小组在实验室制取 Na2O2。查阅资料可知:钠与空气在 453∼473K 之间可生成 Na2O,迅速提高温度到 573∼673K 之间可生成 Na2O2,若温度提高到 733∼873K 之间 Na2O2 可分解。
(1)甲组设计制取 Na2O2 装置如图1。

①使用该装置制取的 Na2O2 中可能含有的杂质为_____ 。.
A.NaCl B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的 Na2O2 样品的纯度,设计可能用到的装置如图 2:烧瓶中发生的主要反应的化学方程式是_________ 。测定装置的接口从 左至右正确的连接顺序是_____ 。
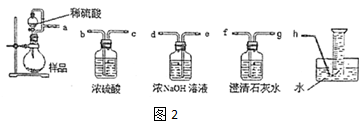
(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果_____ (填“偏大”或“偏 小”)。为证明其分析的正确性,设计实验方案如下:
在上述实验中,能够证明乙组分析正确的最佳方案是_________ (填实验序号)。_______________ 组实验得不出结论,原因是_____ 。
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需 要测定的有关数据__________________________________
(1)甲组设计制取 Na2O2 装置如图1。

①使用该装置制取的 Na2O2 中可能含有的杂质为
A.NaCl B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的 Na2O2 样品的纯度,设计可能用到的装置如图 2:烧瓶中发生的主要反应的化学方程式是

(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果
| 实验方案 | 产生的现象 |
| Ⅰ.取烧瓶中的反应液加入少量 MnO2 粉末 | 有大量气泡逸出 |
| Ⅱ.向 NaOH 稀溶液中加入 2〜3 滴酚酞试液,然后加入少量的反应液 | 溶液先变红后褪色开始无明显现象。 |
| Ⅲ.向反应液中加入 2〜3 滴酚酞试液,充分振荡,然后逐滴加入 过量的 NaOH 稀溶液 | 加 NaOH 溶液先 变红后褪色 |
在上述实验中,能够证明乙组分析正确的最佳方案是
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需 要测定的有关数据
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】有X、Y、Z三种短周期元素,已知X的气态氢化物的分子式为H2X,该氢化物的相对分子质量与X最高价氧化物的相对分子质量之比为17∶40,X原子核内质子数与中子数相等;Y与X可形成离子化合物Y2X,Y的阳离子的电子层结构与Ne相同。Z与X处于同一周期,其气态单质是双原子分子,两原子共用一对电子。
(1)写出各元素的符号:X______ ,Y______ ,Z______ 。
(2)X的相对原子质量为____________ ,其离子的结构示意图为________ 。
(3)Y单质在空气中燃烧的化学方程式是________________________ ,该生成物与水反应的化学方程式是______________________ 。
(4)X与氢气化合的产物的电子式为________ 。
(1)写出各元素的符号:X
(2)X的相对原子质量为
(3)Y单质在空气中燃烧的化学方程式是
(4)X与氢气化合的产物的电子式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设2:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设3:__________________________ ,证明______________________ 。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下。

(2)试剂A可以选用________ ,试剂B的作用是________ 。
(3)实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断,SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________ ,完全被氧化:____________ 。
(4)若SO2完全被氧化,写出反应的化学方程式__________________________ 。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设2:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设3:
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下。

(2)试剂A可以选用
(3)实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断,SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:
(4)若SO2完全被氧化,写出反应的化学方程式
您最近一年使用:0次