现有mg某气体,它由四原子分子构成,它的摩尔质量为Mg/mol.则:
(1)该气体的物质的量为________ mol。
(2)该气体中所含的原子总数约为___________________ 个。
(3)该气体在标准状况下的体积为________ L。
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________ mol/L。
(1)该气体的物质的量为
(2)该气体中所含的原子总数约为
(3)该气体在标准状况下的体积为
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
12-13高二上·甘肃兰州·期中 查看更多[2]
更新时间:2012-11-12 23:29:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】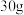 重水(
重水( )中所含质子的物质的量为
)中所含质子的物质的量为_________  ,所含中子数与
,所含中子数与_________ g水( )所含的中子数相等。
)所含的中子数相等。
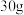 重水(
重水( )中所含质子的物质的量为
)中所含质子的物质的量为 ,所含中子数与
,所含中子数与 )所含的中子数相等。
)所含的中子数相等。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.将39g锌与50mL18.4mol/L的浓硫酸充分反应,锌完全溶解,同时收集到标准状况下气体VL,将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08mol/L。
(1)反应过程中消耗 的物质的量是
的物质的量是_______ 。
(2)气体的成分是_______ ,V=_______ 。
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(3)此时加入的1.0mol/LNaOH溶液的体积为_______ mL。
(4)混合气体中,NO和 的物质的量之比为
的物质的量之比为_______ 。
(5)若将上述生成的混合气体全部与 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少_______ mL。
(1)反应过程中消耗
 的物质的量是
的物质的量是(2)气体的成分是
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和
 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。(3)此时加入的1.0mol/LNaOH溶液的体积为
(4)混合气体中,NO和
 的物质的量之比为
的物质的量之比为(5)若将上述生成的混合气体全部与
 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】判断正误
1.取0.1 mol/L Na2CO3溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L______
2.把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度为1.5 mol·L-1______
3.把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%______
4.把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1______
5.把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%______
6.溶质的质量分数为w溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w______
7.将1 L 18.4 mol·L-1的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol·L-1______
8.V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1 倍,可将溶液加热浓缩到0.5 V L______
1.取0.1 mol/L Na2CO3溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol/L
2.把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度为1.5 mol·L-1
3.把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%
4.把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol·L-1
5.把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%
6.溶质的质量分数为w溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
7.将1 L 18.4 mol·L-1的H2SO4溶液加入到1 L水中,所得溶液的物质的量浓度为9.2 mol·L-1
8.V L浓度为0.5 mol·L-1的盐酸,欲使其浓度增大1 倍,可将溶液加热浓缩到0.5 V L
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的量是联系宏观和微观的桥梁,请完成以下有关计算:
(1)23.75g某+2价金属的氯化物( )中含有
)中含有 个
个 ,则
,则 的摩尔质量为
的摩尔质量为_______ ,M的相对原子质量为_______ 。
(2)标准状况下,448mL某气体的质量为0.64g。这种气体的摩尔质量是_______ 。
(3)在V mL的硫酸铁溶液中,含有m g 离子,则此溶液中
离子,则此溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4)由CO、 两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、
两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、 的物质的量之比为
的物质的量之比为_______ 。
(5)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中 ,
,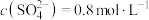 ,
, ,则
,则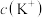 为
为_______ 。
(6)用质量分数为98%、密度为1.84 的浓
的浓 来配制500mL 0.2
来配制500mL 0.2 的稀
的稀 ,则需浓
,则需浓 的体积为
的体积为_______ mL(保留1位小数)
(1)23.75g某+2价金属的氯化物(
 )中含有
)中含有 个
个 ,则
,则 的摩尔质量为
的摩尔质量为(2)标准状况下,448mL某气体的质量为0.64g。这种气体的摩尔质量是
(3)在V mL的硫酸铁溶液中,含有m g
 离子,则此溶液中
离子,则此溶液中 的物质的量浓度为
的物质的量浓度为(4)由CO、
 两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、
两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、 的物质的量之比为
的物质的量之比为(5)由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中
 ,
,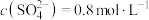 ,
, ,则
,则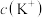 为
为(6)用质量分数为98%、密度为1.84
 的浓
的浓 来配制500mL 0.2
来配制500mL 0.2 的稀
的稀 ,则需浓
,则需浓 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)2L0.1mol/LNa2SO4溶液中Na+的物质的量浓度为__ mol/L,SO 的物质的量为
的物质的量为__ mol。
(2)1克Cl2中含n个分子,则NA=__ (用含n的式子表示)。
(3)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中分子数之比是__ ,原子数之比是__ ,密度之比是__ ,质量之比是__ 。
(4)在标准状况下,将224L氯化氢溶于635mL水,所得盐酸溶液的密度是1.18g/cm3,该盐酸溶液溶质的质量分数为___ ,物质的量浓度为__ 。
(5)气体化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10mLA气体能分解生成15mLO2和10mLF2(同温同压下),则A的化学式是__ ,推断的依据是__ 。
a.质量守恒定律 b.能量守恒定律 c.阿伏伽德罗定律
(1)2L0.1mol/LNa2SO4溶液中Na+的物质的量浓度为
 的物质的量为
的物质的量为(2)1克Cl2中含n个分子,则NA=
(3)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中分子数之比是
(4)在标准状况下,将224L氯化氢溶于635mL水,所得盐酸溶液的密度是1.18g/cm3,该盐酸溶液溶质的质量分数为
(5)气体化合物A是一种不稳定的物质,它的分子组成可用OxFy表示。10mLA气体能分解生成15mLO2和10mLF2(同温同压下),则A的化学式是
a.质量守恒定律 b.能量守恒定律 c.阿伏伽德罗定律
您最近一年使用:0次



