回答下列问题
(1)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;AB为离子交换膜。
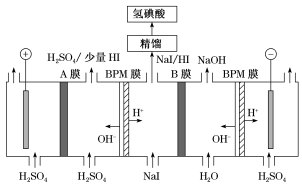
①B膜最佳应选择___________ 。
②阳极的电极反应式是___________ 。
③少量的I-因浓度差通过BPM膜,若撤去A膜,其缺点是___________ 。
(2)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚(C6H5OH)废水更加高效,装置如下图所示。已知a极主要发生的反应是O2生成H2O2,然后在电解液中产生·OH并迅速与苯酚反应。

①b极连接电源的___________ 极(填“正”或“负”)。
②a极的电极反应式为___________ 。
③除电极反应外,电解液中主要发生的反应方程式有___________ 。
(1)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;AB为离子交换膜。

①B膜最佳应选择
②阳极的电极反应式是
③少量的I-因浓度差通过BPM膜,若撤去A膜,其缺点是
(2)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚(C6H5OH)废水更加高效,装置如下图所示。已知a极主要发生的反应是O2生成H2O2,然后在电解液中产生·OH并迅速与苯酚反应。

①b极连接电源的
②a极的电极反应式为
③除电极反应外,电解液中主要发生的反应方程式有
2021高三·全国·专题练习 查看更多[4]
(已下线)专题讲座(六) 电解质介质和隔膜在电化学的作用(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)秘籍13 电解原理及应用-备战2022年高考化学抢分秘籍(全国通用)2021年北京高考化学试题变式题11-19(已下线)第17讲 电解池 金属的腐蚀与防护(练)— 2022年高考化学一轮复习讲练测(新教材新高考)
更新时间:2021-08-19 07:38:08
|
【知识点】 电解原理的应用
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
(1)如图所示,能够组成原电池(烧杯里为相应物质的溶液),并且产生明显电流的是_______ 。

(2)某化学小组探究不同条件下化学能转变为电能的装置如图所示。回答问题:若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式是_______ 。燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的化学能直接转化为电能,现设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液做电解液,则CH4应通入_______ 极 (填“a”或“b”);电池的负极反应式是_______ 。
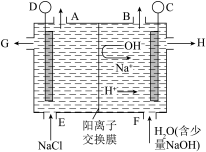
(3)工业电解饱和食盐水制烧碱时必须阻止OH- 移向阳极,目前采用阳离子交换膜将两极溶液分开(如下图所示)。F处加少量NaOH的目的是_______ ;C、D分别是直流电源的两电极,则C是电源_______ 极;若不采用阳离子交换膜,OH-向阳极移动,发生的反应可用离子方程式表示为_______ 。
(1)如图所示,能够组成原电池(烧杯里为相应物质的溶液),并且产生明显电流的是

(2)某化学小组探究不同条件下化学能转变为电能的装置如图所示。回答问题:若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式是

(3)工业电解饱和食盐水制烧碱时必须阻止OH- 移向阳极,目前采用阳离子交换膜将两极溶液分开(如下图所示)。F处加少量NaOH的目的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某实验小组尝试在钢制钥匙上镀铜。
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。
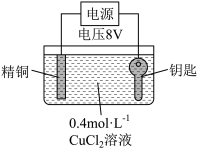
实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是_______ 。
(2)实验II中钥匙应与电源的_______ 极连接。
(3)钥匙表面产生的气体是_______ 。
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是________ 。
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是________ 。(已知CuOH是一种难溶于水的黄色固体)
实验I:将钥匙直接浸入0.4 mol·L-1 CuCl2溶液中,20s后取出,钥匙表面变红,但镀层疏松,用纸即可擦掉。
实验II:用图装置对钥匙进行电镀铜。钥匙表面迅速变红,同时有细小气泡产生,精铜表面出现少量白色固体。30s后取出钥匙检验,镀层相对实验I略好,但仍能用纸巾擦掉一部分。经调整实验条件后获得了较好的电镀产品。

实验III:用0.4 mol·L-1 CuSO4溶液代替CuCl2溶液重复实验II,精铜表面未出现白色固体。
回答下列问题:
(1)实验I反应的化学方程式是
(2)实验II中钥匙应与电源的
(3)钥匙表面产生的气体是
(4)为了避免实验III中钥匙表面产生气体,应该采取的措施是
(5)常见化合物中铜元素有+1、+2两种价态,结合实验III推测实验II中精铜表面产生的白色固体的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
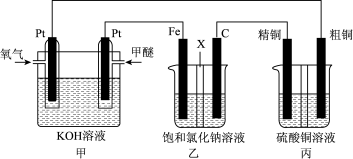
(1)通入氧气的电极为________ 极,写出负极电极反应式____________________ 。
(2)铁电极为________ 极,石墨电极(C)的电极反应式为____________________ 。
(3)反应一段时间后,乙装置中生成NaOH主要在_____ 极区(填电极材料)。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为___________ 、___________ 。反应一段时间,硫酸铜溶液浓度将________ (填“增大”、“减小”或“不变”)。

(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成NaOH主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
您最近一年使用:0次



