A、B两种同族元素,B的原子序数是A的两倍;A与B既可形成BA2型,也可形成BA3型化合物。这两种化合物与水反应生成两种不同的二元酸。试回答下列问题:
(1)A是___________ ,B是___________ ;其原子的电子结构示意图分别为A:___________ ,B:___________ 。
(2)A、B生成BA2化合物的反应___________ ;(配平,并注明条件)
(3)A、B生成BA3化合物的反应___________ ;(配平,并注明条件)
(4)BA2与水的反应方程式___________ ;BA3与水的反应方程式___________ 。
(1)A是
(2)A、B生成BA2化合物的反应
(3)A、B生成BA3化合物的反应
(4)BA2与水的反应方程式
更新时间:2021-08-22 19:08:00
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】H、C、N、O、Mg、Al、Si、S、Cu是中学化学中常见的元素,请根据题意回答与这些元素有关的问题:
(1)S的原子结构示意图为_______ 。
(2)14C可用于古代文物年代鉴定,其原子核内的中子数为_______ 。
(3)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示_______ 。
(4)粉末状的Si3N4对空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在一定条件下的密闭容器中热处理,可以得到对空气、水、和酸都相当稳定的固体材料,同时还可生成对水不稳定的Mg3N2,热处理后除去MgO和Mg3N2的方法是_______ 。
(5)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。若沉淀质量为7.8g,则合金的质量为_______ g。
(6)将由NO和NO2组成的混合气体通入如图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2)。

已知:(i)浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
(ii)NaOH溶液与NO2能发生反应生成两种盐和水,NaOH溶液与NO不反应。
a.装置②、③、④中盛放的药品依次是_______ 、_______ 、_______ 。
b.能够说明实验已成功的现象是_______ 。
(1)S的原子结构示意图为
(2)14C可用于古代文物年代鉴定,其原子核内的中子数为
(3)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示
(4)粉末状的Si3N4对空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在一定条件下的密闭容器中热处理,可以得到对空气、水、和酸都相当稳定的固体材料,同时还可生成对水不稳定的Mg3N2,热处理后除去MgO和Mg3N2的方法是
(5)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。若沉淀质量为7.8g,则合金的质量为
(6)将由NO和NO2组成的混合气体通入如图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2)。

已知:(i)浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
(ii)NaOH溶液与NO2能发生反应生成两种盐和水,NaOH溶液与NO不反应。
a.装置②、③、④中盛放的药品依次是
b.能够说明实验已成功的现象是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】1887年,英国人赫勒森发明了最早的干电池,如今干电池已经发展成为一个庞大的家族,种类达100多种。应用广泛的是Zn—MnO2干电池,其电解质溶液是ZnCl2—NH4Cl混合溶液。电池工作一段时间后,电池内存在7种物质:NH3、Mn2O3、ZnCl2、MnO2、NH4Cl、Zn和H2O。请回答下列问题
(1)该电池的负极材料是__ ;电池工作时,电子流向__ (填“正极”或“负极”,下同);放电时NH4+向___ 移动。
(2)该氧化还原反应的化学方程式为__ ,发生还原反应的物质是__ ,被氧化的元素是__ 。若有17.4g氧化剂参与反应,则电子转移数目为__ NA(NA表示阿伏加 德罗常数的值)。
(3)普通锌锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是___ 。
(4)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__ 。欲除去Cu2+,最好选用下列试剂中的__ (填序号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(1)该电池的负极材料是
(2)该氧化还原反应的化学方程式为
(3)普通锌锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是
(4)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
a.NaOH b.Zn c.Fe d.NH3·H2O
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】据所学知识完成以下题目:
(1)在下列反应中,HCl做还原剂的是_______ ,HCl做氧化剂的是_______ 。
①CaCO3+2HCl=CaCl2+CO2↑+H2O
②Fe+2HCl=FeCl2+H2↑
③PbO2+4HCl(浓) PbCl2+Cl2↑+2H2O
PbCl2+Cl2↑+2H2O
④KClO3+6HCl(浓) KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
⑤CuO+2HCl=CuCl2+H2O
(2)在横线上补充所需的离子或分子,并配平方程式,。
①KMnO4+HCl=KCl+MnCl2+Cl2↑+H2O,_______ 。
②Mn2++ +H2O=MnO2↓+Cl2↑+___ ,
+H2O=MnO2↓+Cl2↑+___ ,_______ 。
(3)用单线桥表示下列反应中电子转移方向和数目:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,_______ 。
(4)钙元素是人体必需的常量元素,所有的细胞都需要钙元素。测定人体血液中钙元素的含量常用到如下两个反应:
①CaC2O4+H2SO4=H2C2O4+CaSO4
②2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
上述反应②的还原剂是____ ;若收集到44.8mL(标准状况)的CO2时,消耗氧化剂_____ mol,有_____ mol电子发生转移,相当于测出含钙元素的质量是_____ g。
(5)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:_____ 。
(1)在下列反应中,HCl做还原剂的是
①CaCO3+2HCl=CaCl2+CO2↑+H2O
②Fe+2HCl=FeCl2+H2↑
③PbO2+4HCl(浓)
 PbCl2+Cl2↑+2H2O
PbCl2+Cl2↑+2H2O④KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O⑤CuO+2HCl=CuCl2+H2O
(2)在横线上补充所需的离子或分子,并配平方程式,。
①KMnO4+HCl=KCl+MnCl2+Cl2↑+H2O,
②Mn2++
 +H2O=MnO2↓+Cl2↑+___ ,
+H2O=MnO2↓+Cl2↑+___ ,(3)用单线桥表示下列反应中电子转移方向和数目:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O,
(4)钙元素是人体必需的常量元素,所有的细胞都需要钙元素。测定人体血液中钙元素的含量常用到如下两个反应:
①CaC2O4+H2SO4=H2C2O4+CaSO4
②2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
上述反应②的还原剂是
(5)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】工业废水中的氨氮(以 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。
(1)微生物法:酸性废水中的部分 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。
① 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
② 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为_______ 。
(2)次氯酸钠氧化法:向氨氮废水中加入 ,氨氮转化为
,氨氮转化为 而除去。
而除去。
① 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
②一定 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。 :
: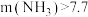 时,总氮的去除率随
时,总氮的去除率随 :
: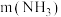 的增大不升反降的原因是
的增大不升反降的原因是_______ 。
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,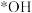 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。_______ 。
②其它条件不变调节废水的 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是_______ 。 晶体进行纯度测定:
晶体进行纯度测定:
a.称取 样品,将其配成
样品,将其配成 溶液。
溶液。
b.先向锥形瓶内加入一定浓度的 溶液,加热至
溶液,加热至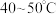 。冷却后再向其中加入
。冷却后再向其中加入
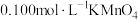 溶液,充分混合。
溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液 。
。
(NaNO2与 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)
通过计算,该样品中 的质量分数是
的质量分数是_______ 。(写出计算过程)
 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。(1)微生物法:酸性废水中的部分
 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。①
 转化为
转化为 的离子方程式为
的离子方程式为②
 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为(2)次氯酸钠氧化法:向氨氮废水中加入
 ,氨氮转化为
,氨氮转化为 而除去。
而除去。①
 氧化
氧化 的离子方程式为
的离子方程式为②一定
 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。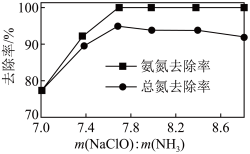
 :
: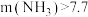 时,总氮的去除率随
时,总氮的去除率随 :
: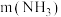 的增大不升反降的原因是
的增大不升反降的原因是(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,
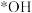 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。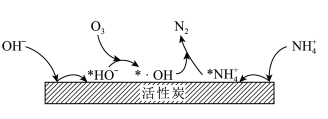
②其它条件不变调节废水的
 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是
 晶体进行纯度测定:
晶体进行纯度测定:a.称取
 样品,将其配成
样品,将其配成 溶液。
溶液。b.先向锥形瓶内加入一定浓度的
 溶液,加热至
溶液,加热至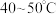 。冷却后再向其中加入
。冷却后再向其中加入
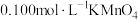 溶液,充分混合。
溶液,充分混合。c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液
 。
。(NaNO2与
 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)通过计算,该样品中
 的质量分数是
的质量分数是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】安全气囊是行车安全的重要设施。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、O四种元素。
(1)氧元素在元素周期表中的位置是__________________ ,Na原子结构示意图为_____________ ,其中三种主族元素的离子半径从大到小的顺序是___________________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类 型是
型是____________________ 。
(3)水溶性实验表明,安全气囊中固体粉末部分溶解,不溶物为一种红棕色固体,可溶于盐酸,写出反应的化学方程式_______________________________________________ 。
(1)氧元素在元素周期表中的位置是
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类
 型是
型是(3)水溶性实验表明,安全气囊中固体粉末部分溶解,不溶物为一种红棕色固体,可溶于盐酸,写出反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】元素周期表中的数量应用
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为_______ 。
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是_______ 。
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为_______ 。
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
(1)甲、乙是元素周期表中同一周期的第ⅡA族和第ⅦA族元素,原子序数分别为m、n,则m、n的关系为
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲的原子序数为x,则乙的原子序数可能是
(3)若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为
(4)下列各表为元素周期表中的一部分,表中数字为原子序数,其中M的原子序数为37的是_______。
A. | B.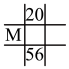 | C.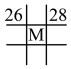 | D.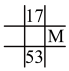 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】综合利用CO2对环境保护及能开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是______ 。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是______ 。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A: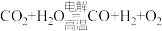
已知:

反应A的热化学方程式是_______ 。
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:
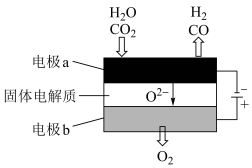
① 电极b发生_______ (填“氧化”或“还原”)反应。
② CO2在电极a放电的反应式是______ 。
(5)CO与H2在高温下合成C5H12(汽油的一种成分)减少碳排放。已知燃烧1 mol C5H12(g)生成H2O(g)放出约3540 kJ的热量。根据化学平衡原理,说明提高合成C5H12的产率可采取的措施是______ 。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
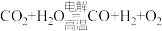
已知:

反应A的热化学方程式是
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生
② CO2在电极a放电的反应式是
(5)CO与H2在高温下合成C5H12(汽油的一种成分)减少碳排放。已知燃烧1 mol C5H12(g)生成H2O(g)放出约3540 kJ的热量。根据化学平衡原理,说明提高合成C5H12的产率可采取的措施是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】(1)给出下列四种化合物的化学名称:
A. 的名称:
的名称:_______
B.CH3OCH2CH2OCH3的名称:_______
C. 的名称:
的名称:_______
D. 的名称:
的名称:_______
(2)常用上述溶剂将芳香烃和丁二烯等化工原料从石油馏分中抽提出来,请简要说明它们的作用原理_______ 。
(3)选出下列顺磁性物种_______ (用物种前面的字母表示);
A.Cr(H2O) B.Fe(CO)5 C.N2O-ON2 D.[N(C6H4OCH3)3]+
B.Fe(CO)5 C.N2O-ON2 D.[N(C6H4OCH3)3]+
A.
 的名称:
的名称:B.CH3OCH2CH2OCH3的名称:
C.
 的名称:
的名称:D.
 的名称:
的名称:(2)常用上述溶剂将芳香烃和丁二烯等化工原料从石油馏分中抽提出来,请简要说明它们的作用原理
(3)选出下列顺磁性物种
A.Cr(H2O)
 B.Fe(CO)5 C.N2O-ON2 D.[N(C6H4OCH3)3]+
B.Fe(CO)5 C.N2O-ON2 D.[N(C6H4OCH3)3]+
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】下面各问题涉及到卤素的反应,请通过推理计算填空。
(1)将9.13gKI溶解于100g热水中,加入13.96gI2,并剧烈搅拌直至溶液澄清。然后浓缩溶液,之后降温至2°C,静置结晶,生成了深棕色的盐A.分离出晶体A,洗净,干燥。取0.9500g产物A溶解于水中,在淀粉指示剂下用0.2000 mol·L-1 Na2S2O3 溶液滴定,消耗21.70 mL。请给出A的化学式:___________ 。
(2)向热浓KI溶液中通入氯气至饱和,反应至最初生成的棕色沉淀物消失。反应结束后,向溶液中加入少量KI固体,冷却至0°C会出现橙色的含结晶水的盐B.X射线衍射表明B的阴离子与A的阴离子有类似的结构。B在空气中不稳定,并且在通入保护气体的环境下加热至215.C即分解。取15.32gB,在N2下加热至250 °C,剩余固体产物质量为4.48g,是白色水溶性固体。其水溶液与AgNO3溶液混合后产生白色沉淀,此沉淀在氨水中可溶。
①给出B的化学式:___________ 。
②写出生成B和B分解的化学方程式:___________ ,___________ 。
(3)碘的吡啶( 化学式为C5H5N,结构式为 ,简写为Py, 相对分子质量79.10)溶液是可以导电的,为了确定溶液中的阳离子,做了以下实验:在分液漏斗中加入碘的吡啶溶液,再加入高氯酸银的氯仿和水混合液。振荡数分钟后,水层产生黄色不溶物,并与氯仿层分离。将氯仿溶液转移至结晶设备中结晶,过滤得到晶体C (含高氯酸根),洗净干燥。取0.9460 g化合物C溶解于水中,加入足量KI,生成的I2用0.2000 mol·L-1 的Na2S2O3溶液滴定,消耗24.60 mL。通过晶体学分析得知C的阳离子结构与A、B的阴离子相似。
,简写为Py, 相对分子质量79.10)溶液是可以导电的,为了确定溶液中的阳离子,做了以下实验:在分液漏斗中加入碘的吡啶溶液,再加入高氯酸银的氯仿和水混合液。振荡数分钟后,水层产生黄色不溶物,并与氯仿层分离。将氯仿溶液转移至结晶设备中结晶,过滤得到晶体C (含高氯酸根),洗净干燥。取0.9460 g化合物C溶解于水中,加入足量KI,生成的I2用0.2000 mol·L-1 的Na2S2O3溶液滴定,消耗24.60 mL。通过晶体学分析得知C的阳离子结构与A、B的阴离子相似。
①给出C的化学式:___________ ;
②写出在碘的吡啶溶液中的平衡反应:___________ ;
③写出合成C的反应方程式:___________ ;
④画出C中阳离子的结构:___________ 。
(1)将9.13gKI溶解于100g热水中,加入13.96gI2,并剧烈搅拌直至溶液澄清。然后浓缩溶液,之后降温至2°C,静置结晶,生成了深棕色的盐A.分离出晶体A,洗净,干燥。取0.9500g产物A溶解于水中,在淀粉指示剂下用0.2000 mol·L-1 Na2S2O3 溶液滴定,消耗21.70 mL。请给出A的化学式:
(2)向热浓KI溶液中通入氯气至饱和,反应至最初生成的棕色沉淀物消失。反应结束后,向溶液中加入少量KI固体,冷却至0°C会出现橙色的含结晶水的盐B.X射线衍射表明B的阴离子与A的阴离子有类似的结构。B在空气中不稳定,并且在通入保护气体的环境下加热至215.C即分解。取15.32gB,在N2下加热至250 °C,剩余固体产物质量为4.48g,是白色水溶性固体。其水溶液与AgNO3溶液混合后产生白色沉淀,此沉淀在氨水中可溶。
①给出B的化学式:
②写出生成B和B分解的化学方程式:
(3)碘的吡啶( 化学式为C5H5N,结构式为
 ,简写为Py, 相对分子质量79.10)溶液是可以导电的,为了确定溶液中的阳离子,做了以下实验:在分液漏斗中加入碘的吡啶溶液,再加入高氯酸银的氯仿和水混合液。振荡数分钟后,水层产生黄色不溶物,并与氯仿层分离。将氯仿溶液转移至结晶设备中结晶,过滤得到晶体C (含高氯酸根),洗净干燥。取0.9460 g化合物C溶解于水中,加入足量KI,生成的I2用0.2000 mol·L-1 的Na2S2O3溶液滴定,消耗24.60 mL。通过晶体学分析得知C的阳离子结构与A、B的阴离子相似。
,简写为Py, 相对分子质量79.10)溶液是可以导电的,为了确定溶液中的阳离子,做了以下实验:在分液漏斗中加入碘的吡啶溶液,再加入高氯酸银的氯仿和水混合液。振荡数分钟后,水层产生黄色不溶物,并与氯仿层分离。将氯仿溶液转移至结晶设备中结晶,过滤得到晶体C (含高氯酸根),洗净干燥。取0.9460 g化合物C溶解于水中,加入足量KI,生成的I2用0.2000 mol·L-1 的Na2S2O3溶液滴定,消耗24.60 mL。通过晶体学分析得知C的阳离子结构与A、B的阴离子相似。①给出C的化学式:
②写出在碘的吡啶溶液中的平衡反应:
③写出合成C的反应方程式:
④画出C中阳离子的结构:
您最近一年使用:0次
【推荐3】在30 ℃以下,将过氧化氢加到硼酸和氢氧化钠的混合溶液中,析出一种无色晶体X。组成分析证实,该晶体的质量组成为Na:14.90%,B:7.03%,H:5.24%。加热X,得无色晶体Y。Y含Na 23.0%,是一种温和的氧化剂,常温下在干燥空气里稳定,但在潮湿热空气中分解放氧,广泛用作洗涤剂、牙膏、织物漂白剂和美发产品,也用于有机合成。结构分析证实X和Y的晶体中有同一种阴离子Z2-,该离子中硼原子的化学环境相同,而氧原子却有两种成键方式。
(1)写出X、Y的最简式,给出推理过程。
X的最简式:_______ Y的最简式:_______ 。
推理过程:____________
(2)用最恰当的视角画出Z2-离子的立体结构____ (原子用元素符号表示,共价键用短线表示)。
(1)写出X、Y的最简式,给出推理过程。
X的最简式:
推理过程:
(2)用最恰当的视角画出Z2-离子的立体结构
您最近一年使用:0次



