下列指定反应的离子方程式正确的是
A.铜与稀硝酸反应: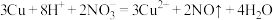 |
B.AgNO3溶液中加入过量氨水: |
C.向NaClO溶液中通入足量SO2气体: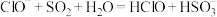 |
D.用惰性电极电解NaCl溶液: |
更新时间:2021-08-30 15:27:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列分子或离子在指定的分散系中能大量共存的一组是( )
| A.饱和氯水中:Na+、K+、Cl-、CO32- |
| B.淀粉溶液中:K+、NH4+、SO42-、I- |
| C.Na2SiO3溶液中:Cl-、I-、K+、CO2 |
| D.葡萄糖溶液中:Na+、H+、SO42-、Cr2O72- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,下列离子组在指定溶液中一定能大量共存的是
A.能与金属铝反应产生H2 的溶液:Na+、 Al3+、 NO 、I- 、I- |
B.pH=13 的溶液:K+、 Ca2+、Cl-、 HCO |
C.由水电离产生的c(OH-) = 1×1013mol·L-1 的溶液:Na+、 Fe2+、 NO 、 Cl- 、 Cl- |
D.c(CO ) = 0.1 mol·L-1的溶液:Na+、 NH ) = 0.1 mol·L-1的溶液:Na+、 NH 、 Br-、 SO 、 Br-、 SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列过程中的化学反应相应的离子方程式正确的是
| A.向氯化铁溶液中通入过量硫化氢:2Fe3++H2S = 2Fe2++S↓+2H+ |
| B.向FeBr2溶液中通入等量Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| C.BaCl2溶液中通入CO2:Ba2++H2O+CO2=BaCO3↓+2H+ |
D.用酸化的高锰酸钾溶液氧化双氧水:2 +6H++H2O2=2Mn2++3O2↑+4H2O +6H++H2O2=2Mn2++3O2↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式能用来解释相应实验操作或现象,且操作和现象均描述正确的是
| 实验操作或现象 | 离子方程式 | |
| A | 用酸化的硝酸铁溶液腐蚀铜箔 | 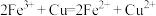 |
| B | 在稀硫酸中加入铜粉,铜粉不溶解,再加入 固体,铜粉溶解 固体,铜粉溶解 |  |
| C | 用浓氢氧化钠溶液反萃取法提取碘 | 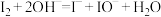 |
| D | 氧化亚铁溶于稀硝酸 | 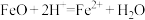 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用食盐水制取ClO2的工业流程如图所示,下列关于该流程的说法正确的是


| A.该流程可以循环利用的物质是H2、Cl2 |
B.装置①中发生反应的化学方程式为NaCl+3H2O NaClO3+3H2↑ NaClO3+3H2↑ |
| C.装置②中,每生成1 mol ClO2转移的电子数为5NA |
| D.为了提高H2的转化率,可向装置③通入过量的H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式正确的是
| A.磁性氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O |
| B.四氯化钛的浓溶液制备水合二氧化钛:Ti4++(x+2)H2O=TiO2·xH2O↓+4H+ |
C.水玻璃中通入少量CO2:Na2SiO3+CO2+H2O=CO +H2SiO3↓+2Na+ +H2SiO3↓+2Na+ |
D.酸性KMnO4溶液滴定双氧水:2MnO +H2O2+6H+=2Mn2++3O2↑+4H2O +H2O2+6H+=2Mn2++3O2↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法不正确的是
| A.可用铁作阳极材料 |
| B.电解过程中阴极附近溶液的pH升高 |
C.阳极反应方程式为: |
| D.1mol二价镍全部转化为三价镍时,外电路中通过了1mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】溶液电池是最具潜力的大规模储能电化学器件,然而不同的水溶液电池的发展又受到不同因素的限制。醌类( )电极的酸碱混合电池能够实现高能量密度和优异的循环稳定性。电池工作示意图如图所示,下列有关说法错误的是
)电极的酸碱混合电池能够实现高能量密度和优异的循环稳定性。电池工作示意图如图所示,下列有关说法错误的是

| A.放电时,右侧醌类电极为负极 |
| B.放电时,左侧电极反应式为MnO2+2e-+4H+=Mn2++2H2O |
| C.充电时,阳极区电解质溶液的pH保持不变 |
| D.充电时,电路中每转移1mol电子,阴极增重质量为20g |
您最近一年使用:0次




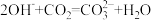

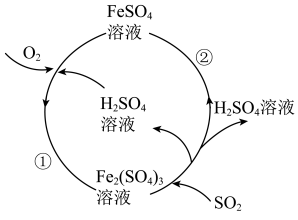
 ,再用下图电化学装置除去
,再用下图电化学装置除去


