已知A、B两种元素,A的原子序数为x,A和B所在周期的元素种类数目分别为m和n。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为___________ ,当B在A的下一周期时,B的原子序数为___________ ;
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ ;当B在A的下一周期时,B的原子序数为___________ 。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
19-20高一下·云南曲靖·期中 查看更多[4]
云南省曲靖市罗平县第二中学2019-2020学年高一下学期期中考试化学试题(已下线)4.1.2 元素周期表 核素-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)5.1.2 元素周期表(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)海南省琼海市嘉积中学2023-2024学年高一上学期期末考试化学试题B卷
更新时间:2021-09-02 22:19:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)⑤、⑥、⑨、⑩的简单离子半径由小到大的顺序____ ,写出⑥的原子结构示意图:____ 。
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于____ (填“晶体”或“非晶体”)。
(3)元素②、③、④的简单气态氢化物的稳定性最强的是____ (用化学式表示,下同),元素③、⑨简单氢化物沸点较高的是____ 。
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是____ ,元素⑪最高价氧化物对应的水化物的化学式是____ 。
(5)请用电子式表示元素⑤的氧化物的形成过程:____ ,该化合物属于____ (填“共价”或“离子”)化合物。
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于
(3)元素②、③、④的简单气态氢化物的稳定性最强的是
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是
(5)请用电子式表示元素⑤的氧化物的形成过程:
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)F的元素符号为_______ ,B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______(填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)F的元素符号为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质_______(填标号)。
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
(1)元素①在周期表中的位置为_____ 。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____ (填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____ ,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______ (填化学式)。
(4)元素②、⑤形成化合物的电子式为_____ 。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为______
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为
(3)元素①、③形成的18电子化合物的电子式为
(4)元素②、⑤形成化合物的电子式为
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。_________
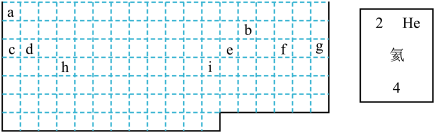
(2)表中所列元素,属于短周期元素的有_______ ,属于主族元素的有_______ ;g元素位于第_______ 周期________ 族;i元素位于第_______ 周期__________ 族。
(3)元素f是第_________ 周期、第_________ 族元素,请在下边方框中按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。_________

(4)元素在元素周期表中的位置与元素原子结构的关系__________________ 。
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。

(2)表中所列元素,属于短周期元素的有
(3)元素f是第

(4)元素在元素周期表中的位置与元素原子结构的关系
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】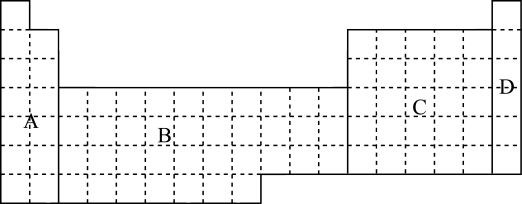
(1)在上面元素周期表中全部是金属元素的区域为____ 。
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____ (写出元素符号)。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:_____ 。
② 甲、乙两元素相比较,金属性较强的是____ (填名称),可以验证该结论的实验是__ 。
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
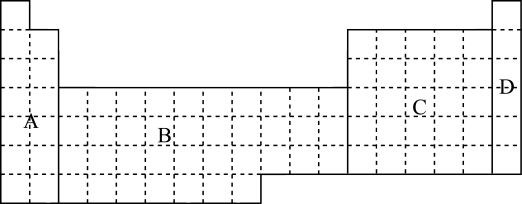
(1)在上面元素周期表中全部是金属元素的区域为
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:
② 甲、乙两元素相比较,金属性较强的是
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
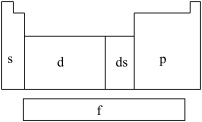
(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为___________ ,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分。
(1)表中原子半径最小的元素符号是____ ;
(2)表中氧化性最强的单质的化学式为____ ;
(3)表中最高价氧化物的水化物中碱性最强的物质的化学式是__ ,酸性最强的物质的化学式是_______ ;
(4)④⑤⑥三种元素中,离子半径大小的顺序为____ >____ >____ (填离子符号);
(5)③⑦⑧三种元素的气态氢化物的稳定性强弱顺序为__ >__ >___ (填化学式);
(6)元素②的氢化物与元素⑧的氢化物反应的化学方程式为________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
(1)表中原子半径最小的元素符号是
(2)表中氧化性最强的单质的化学式为
(3)表中最高价氧化物的水化物中碱性最强的物质的化学式是
(4)④⑤⑥三种元素中,离子半径大小的顺序为
(5)③⑦⑧三种元素的气态氢化物的稳定性强弱顺序为
(6)元素②的氢化物与元素⑧的氢化物反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,针对表中的①~⑩种元素,回答下列问题:
(1)元素③的单质的电子式为_______ ,元素③的气态氢化物与其最高价氧化物的水化物反应的化学方程式为___________ 。
(2)用电子式表示元素⑨与⑥的化合物的形成过程:_______________ 。
(3)元素⑥的氢化物的结构式为_______ ;该氢化物常温下和元素⑦的单质反应的化学方程式为________________ ;
(4)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)____________ 。
(5)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为;4核18电子的分子__________ ,10电子的阳离子____________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)元素③的单质的电子式为
(2)用电子式表示元素⑨与⑥的化合物的形成过程:
(3)元素⑥的氢化物的结构式为
(4)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)
(5)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为;4核18电子的分子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】右表是元素周期表的一部分。
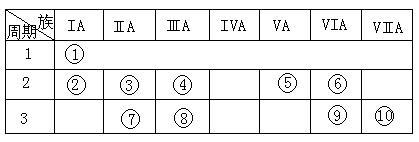
(1)表中元素⑩的氢化物的化学式为__________ ,此氢化物的还原性比元素⑨的氢化物的还原性_____________ (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,其单质的电子式为________________ 。
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式____________________ ;又如表中与元素⑦的性质相似的不同族元素是___________ (填元素符号)

(1)表中元素⑩的氢化物的化学式为
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
您最近一年使用:0次



