在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
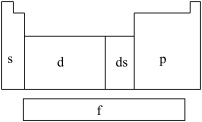
(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为___________ ,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期ⅤA族元素原子的价电子排布图为
(5)当今常用于核能开发的元素是铀和钚,它们在
2016高二·全国·课时练习 查看更多[9]
2.2.1原子核外电子排布的周期性 课后专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第1课时 原子核外电子排布的周期性(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第30讲 原子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题高中化学人教版 选修三 第1章 原子结构与性质 原子结构与元素周期表(已下线)同步君 选修3 第一章 第二节 原子结构与元素周期表
更新时间:2021-12-04 21:50:36
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】原子结构特点(F→I)
(1)相似性:最外层电子数均为_______ 。
(2)递变性:电子层数逐渐_______ ,原子半径逐渐_______ 。
(1)相似性:最外层电子数均为
(2)递变性:电子层数逐渐
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
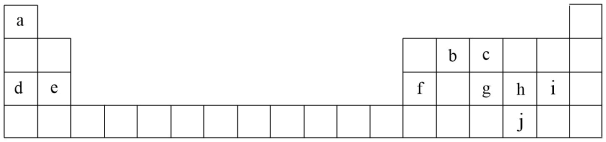
(1)元素c代表的元素是(写元素符号)_______
(2)请写出元素e在元素周期表中所在的位置_______
(3)请画出元素f的简单离子结构示意图_______ 。请写出单质f与d的最高价氧化物对应水化物的离子反应方程式_______ 。
(4)元素a和b能构成最简单的有机化合物(用结构式表示)_______ 。请写出元素a和b构成的最简单有机化合物与i单质发生的第一步化学反应方程式_______ 。
(5)元素h的最高价氧化物对应的水化物呈_______ (酸性、中性或碱性);请写出元素h的最高价氧化物对应的水化物与单质b的化学反应方程式_______ 。

(1)元素c代表的元素是(写元素符号)
(2)请写出元素e在元素周期表中所在的位置
(3)请画出元素f的简单离子结构示意图
(4)元素a和b能构成最简单的有机化合物(用结构式表示)
(5)元素h的最高价氧化物对应的水化物呈
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:_______ 。
(2)原子符号为 X的元素属于第
X的元素属于第_______ 周期_______ 族。
(3)周期表中位于第8纵列的铁元素属于第_______ 族。
(4)周期表中第三周期最活泼的金属元素是_______ 。
(5)已知某微粒的结构示意图为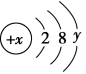 ,试回答下列问题:
,试回答下列问题:
①当x-y=10时,该微粒为_______ (填“原子”“阳离子”或“阴离子”)。
②当y=6时,元素最高价氧化物对应水化物的化学式为_______ 。
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)原子符号为
 X的元素属于第
X的元素属于第(3)周期表中位于第8纵列的铁元素属于第
(4)周期表中第三周期最活泼的金属元素是
(5)已知某微粒的结构示意图为
 ,试回答下列问题:
,试回答下列问题:①当x-y=10时,该微粒为
②当y=6时,元素最高价氧化物对应水化物的化学式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】基态钾原子中,其占据的最高能层的符号是___________ ;基态钾离子占据的最高能级共有___________ 个原子轨道,其形状是___________ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是s能级和p能级的电子云轮廓图,试回答问题。
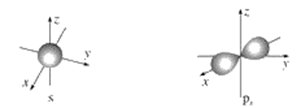
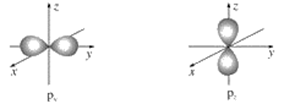
(1)s电子云轮廓图呈________ 形,每个s能级有________ 个原子轨道;p电子云轮廓图呈________ 状,每个p能级有________ 个原子轨道,其能量关系为____________ (填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是________ 电子;元素X的名称是____ ,它的氢化物的电子式是________ 。
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为________ ,原子的电子排布图为______________________________ 。
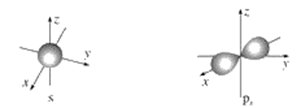
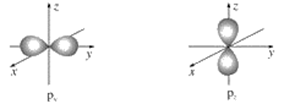
(1)s电子云轮廓图呈
(2)元素X的原子最外层的电子排布式为nsnnpn+1,原子中能量最高的是
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】硼元素、钙元素、铜元素在化学中站有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为______ 。
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的 键数目为
键数目为______ 。
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是______ ,构成丙烯腈元素中第一电离能最大的是______ 。
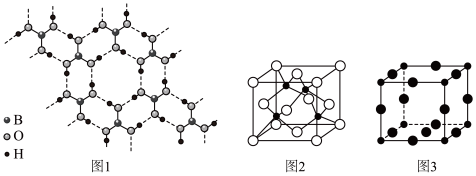
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图1)则1molH3BO3的晶体中有______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为______ 。
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
 该晶体化学式为
该晶体化学式为______ 。
 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______ (填“离子”、“共价”)化合物。
(4)Cu3N的晶胞结构如上图3,N3-的配位数为______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为______ g•cm-3(阿伏加 德罗常数用NA表示)。
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的
 键数目为
键数目为③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是

(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图1)则1molH3BO3的晶体中有
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
 该晶体化学式为
该晶体化学式为 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于(4)Cu3N的晶胞结构如上图3,N3-的配位数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空。
I.元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为 21 世纪金属,画出基态钛的价电子的轨道表示式_______ 。
(2)能区别[Co(NH3)4Cl2]Cl 和[Co(NH3)4Cl2]NO3两种溶液的试剂是_______ (填选项)。
(3)K3[Fe(CN)6]是鉴别 Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是_______ (填元素符号),K3[Fe(CN)6]中碳的杂化方式与下列物质中碳杂化方式相同的是_______ (填选项)。
A.CH2Cl2 B.C2H2 C.溴苯 D.乙烯
II.根据题意写出化学方程式:
(4)写出肉桂醛 ( )与银氨溶液反应的化学方程式
)与银氨溶液反应的化学方程式_______ 。
(5)写出有机物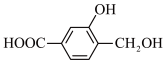 与足量 NaOH 反应的化学方程式
与足量 NaOH 反应的化学方程式_______ 。
(6)两分子苹果酸(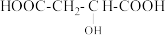 )在浓硫酸作用下可生成六元环状化合物,写出该化学方程式
)在浓硫酸作用下可生成六元环状化合物,写出该化学方程式_______ 。
(7)写出苯甲酸甲酯(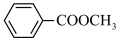 )在 NaOH 溶液中发生水解反应的化学方程式
)在 NaOH 溶液中发生水解反应的化学方程式_____ 。
I.元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为 21 世纪金属,画出基态钛的价电子的轨道表示式
(2)能区别[Co(NH3)4Cl2]Cl 和[Co(NH3)4Cl2]NO3两种溶液的试剂是_______ (填选项)。
| A.浓氨水 | B.NaOH 溶液 | C.稀 H2SO4 | D.AgNO3溶液 |
A.CH2Cl2 B.C2H2 C.溴苯 D.乙烯
II.根据题意写出化学方程式:
(4)写出肉桂醛 (
 )与银氨溶液反应的化学方程式
)与银氨溶液反应的化学方程式(5)写出有机物
 与足量 NaOH 反应的化学方程式
与足量 NaOH 反应的化学方程式(6)两分子苹果酸(
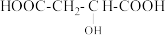 )在浓硫酸作用下可生成六元环状化合物,写出该化学方程式
)在浓硫酸作用下可生成六元环状化合物,写出该化学方程式(7)写出苯甲酸甲酯(
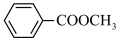 )在 NaOH 溶液中发生水解反应的化学方程式
)在 NaOH 溶液中发生水解反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钛被视为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”,钛和钛的化合物在航天、化工、建筑、医疗中都有着广泛的用途。
回答下列问题:
(1)基态钛原子核外有_______ 种能量不同的电子,其能量最高的电子所在的能级符号为_______ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
① 中所含元素电负性由小到大的顺序为
中所含元素电负性由小到大的顺序为_______ 。
② 与
与 互为等电子体,
互为等电子体, 的立体构型为
的立体构型为_______ 。
③ 由
由 和
和 构成,
构成, 中B原子的杂化类型是
中B原子的杂化类型是_______ 。
④ 存在
存在_______ (填字母)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
回答下列问题:
(1)基态钛原子核外有
(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①
 中所含元素电负性由小到大的顺序为
中所含元素电负性由小到大的顺序为②
 与
与 互为等电子体,
互为等电子体, 的立体构型为
的立体构型为③
 由
由 和
和 构成,
构成, 中B原子的杂化类型是
中B原子的杂化类型是④
 存在
存在A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铝及其化合物在生产和科研中有广泛的应用。回答下列问题:
(1)Al位于元素周期表的_______ 区,基态Al原子价层电子的轨道表示式为_______ 。
(2)AlN是一种应用广泛的新型无机非金属材料,其结构与晶体硅类似,由此推测AlN的熔点比AlCl3_______ (填“高”或“低”),原因是_______ 。
(3)Al(OH)3溶解在NaOH溶液中可形成Na[Al(OH)4](四羟基合铝酸钠)溶液,在Na[Al(OH)4]溶液中存在的化学键有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(4)近年来,人们发现NH3AlH3可与多种小分子氢化物形成双氢键。双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用,其结构可用如图表示。根据上述信息,NH3AlH3与HF形成的双氢键可表示为_______ 。
(5)Al单质晶体中原子的堆积方式与干冰中CO2分子的相同,其晶胞如图所示。
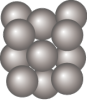
在该晶体中,一个Al原子周围距离最近的Al原子有_______ 个。
(1)Al位于元素周期表的
(2)AlN是一种应用广泛的新型无机非金属材料,其结构与晶体硅类似,由此推测AlN的熔点比AlCl3
(3)Al(OH)3溶解在NaOH溶液中可形成Na[Al(OH)4](四羟基合铝酸钠)溶液,在Na[Al(OH)4]溶液中存在的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(4)近年来,人们发现NH3AlH3可与多种小分子氢化物形成双氢键。双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用,其结构可用如图表示。根据上述信息,NH3AlH3与HF形成的双氢键可表示为
| X-H…H-Y “一”表示共价键,“…”表示形成的双氢键) |
(5)Al单质晶体中原子的堆积方式与干冰中CO2分子的相同,其晶胞如图所示。

在该晶体中,一个Al原子周围距离最近的Al原子有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图是元素周期表的一部分,图中所列字母分别代表一种化学元素。
(1)元素b位于周期表中________ 区,其基态原子电子排布式为________ 。
(2)基态c原子中有________ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为________ 形。
(3)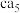 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为________ 。
(4)基态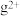 外围电子的轨道表示式为
外围电子的轨道表示式为________ ,已知高温下化合物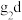 比化合物gd更稳定,试从核外电子排布的角度解释原因
比化合物gd更稳定,试从核外电子排布的角度解释原因________ 。
(5)基态f原子的原子结构示意图为________ 。

(1)元素b位于周期表中
(2)基态c原子中有
(3)
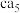 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为(4)基态
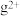 外围电子的轨道表示式为
外围电子的轨道表示式为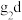 比化合物gd更稳定,试从核外电子排布的角度解释原因
比化合物gd更稳定,试从核外电子排布的角度解释原因(5)基态f原子的原子结构示意图为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D、E是前四周期的元素。A、B、C同周期,C、D同主族且原子半径C>D,A的原子结构示意图为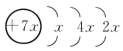 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A___________ ,B___________ ,C___________ ,D___________ 。
(2)用元素符号表示D所在周期第一电离能最大的元素是___________ ,电负性最大的元素是___________ 。
(3)E原子价电子排布式是___________ ,E元素在周期表的位置是___________ ,则E元素在___________ 区。
(4)基态D原子的价电子排布图___________ ,元素D的原子最外层共有___________ 种不同运动状态的电子。基态原D子电子占据最高能级的电子云轮廓图为___________ 形。
(5)A、B、C三者原子半径由大到小的顺序为___________ (用元素符号回答)
(6)某同学推断Mg的基态原子的轨道表示式为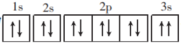 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
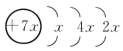 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:(1)写出下列元素的符号:A
(2)用元素符号表示D所在周期第一电离能最大的元素是
(3)E原子价电子排布式是
(4)基态D原子的价电子排布图
(5)A、B、C三者原子半径由大到小的顺序为
(6)某同学推断Mg的基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了
您最近半年使用:0次



