请回答下列问题。
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:
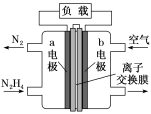
①该燃料电池中正极通入的物质是___________ ,负极发生的反应式为___________ 。
②电池工作时,OH-移向极___________ (填“a”或“b”)。
③当电池放电转移5 mol电子时,至少消耗燃料肼___________ g.
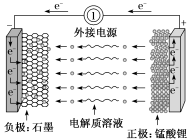
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:

①该燃料电池中正极通入的物质是
②电池工作时,OH-移向极
③当电池放电转移5 mol电子时,至少消耗燃料肼
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix
 LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
| A.放电时电池的正极反应式为Li1-xMnO4+xLi++xe-=LiMnO4 |
| B.放电过程中,石墨没有得失电子 |
| C.该电池也能在KOH溶液的环境中正常工作 |
| D.充电时电池上标有“-”的电极应与外接电源的负极相连 |
2021高三·全国·专题练习 查看更多[2]
(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第四章第一节 原电池(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)
更新时间:2021-09-23 21:33:09
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】电化学原理在工业生产及生活中发挥着巨大的作用。
Ⅰ.利用微电解技术可以处理工业废水,如酸性含铬废水(主要含有Cr2O )。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
)。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
(1)通常以铁板和石墨作为电极材料,应选________ 作阴极。
(2)废水中的Cr2O 通过反应转化为Cr3+,此过程的离子反应方程式为
通过反应转化为Cr3+,此过程的离子反应方程式为________ ,最终Cr3+以Cr(OH)3形式除去。
(3)当电路中每转移1.2mol电子,最多有________ mol Cr2O 参加反应。
参加反应。
Ⅱ.红矾钠(Na2Cr2O7•2H2O)是一种重要的化工原料。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑。
2Na2Cr2O7+4NaOH+2H2↑+O2↑。
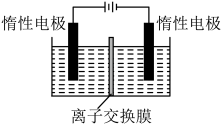
(4)电解时应选择________ (填“阴”“阳”)离子交换膜。阳极区的反应有________ ,NaOH在________ (填“阴”或“阳”)极室制得。
Ⅲ.用C3H8、O2和熔融Na2CO3组成的燃料电池作电源,电解饱和的K2S溶液和2mol•L-1AgNO3溶液制备某些单质,盐桥中充有饱和的KNO3溶液。
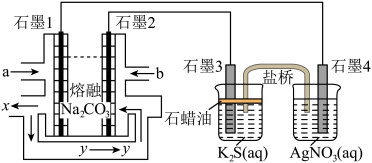
(5)石墨1电极反应式为________ ,物质y为________ 。
(6)若此装置通入C3H8的体积为2.24L(标准状况下),则可以制取单质硫的质量为________ 。
Ⅰ.利用微电解技术可以处理工业废水,如酸性含铬废水(主要含有Cr2O
 )。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
)。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。(1)通常以铁板和石墨作为电极材料,应选
(2)废水中的Cr2O
 通过反应转化为Cr3+,此过程的离子反应方程式为
通过反应转化为Cr3+,此过程的离子反应方程式为(3)当电路中每转移1.2mol电子,最多有
 参加反应。
参加反应。Ⅱ.红矾钠(Na2Cr2O7•2H2O)是一种重要的化工原料。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O
 2Na2Cr2O7+4NaOH+2H2↑+O2↑。
2Na2Cr2O7+4NaOH+2H2↑+O2↑。
(4)电解时应选择
Ⅲ.用C3H8、O2和熔融Na2CO3组成的燃料电池作电源,电解饱和的K2S溶液和2mol•L-1AgNO3溶液制备某些单质,盐桥中充有饱和的KNO3溶液。

(5)石墨1电极反应式为
(6)若此装置通入C3H8的体积为2.24L(标准状况下),则可以制取单质硫的质量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】电化学原理在工农业生产中有重要应用。已知肼( )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,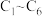 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
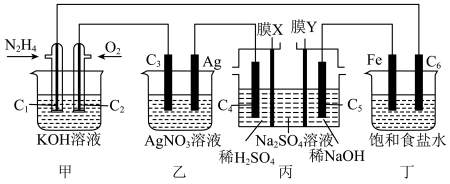
回答下列问题:
(1)甲装置中, 电极为
电极为___________ 极(填“正”“负”“阳”或“阴”), 电极的电极反应式为
电极的电极反应式为___________ 。
(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为___________ 。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为___________ 交换膜(填“阳离子”或“阴离子”)。当外电路中通过0.04mol电子时,中间 废水的质量改变了
废水的质量改变了___________ g。
(4)丁装置工作中发生反应的化学方程式为___________ 。
 )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,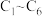 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
回答下列问题:
(1)甲装置中,
 电极为
电极为 电极的电极反应式为
电极的电极反应式为(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为
 废水的质量改变了
废水的质量改变了(4)丁装置工作中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】铁是目前人类使用量最大的金属,它能形成多种化合物.
(l)工业上,向炽热铁屑中通入氯化氢可生成无水氯化亚铁,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3,常用的试剂是___________ ;为防止FeC12溶液中含有FeCl3,最好在FeCl2溶液中加入___________
(2)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
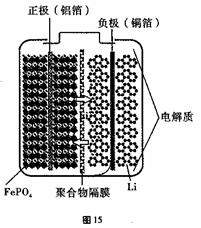
①以FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,同时伴随产生一种可燃性气体,该反应的化学方程式为___________________ 。若有1mol C参与反应,则转移的电子数目为___________
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开,只允许锂离子通过)工作原理为FePO4+Li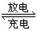 LiFePO4。如图所示,则放电时FePO4一端为电池的
LiFePO4。如图所示,则放电时FePO4一端为电池的___ 极,充电时阳极上的电极反应式为______________________________ 。
(3)硫化亚铁常用于工业废水的处理。已知25℃时,溶度积常数Ksp[FeS]=6.3×10-18,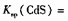 3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:
3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:
在FeS、CdS的悬浊液中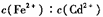 =
=________________
(4)已知25℃时,尺,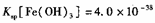 ,此温度下若在实验室中配制
,此温度下若在实验室中配制 溶液,为使配制过程中不出现浑浊现象,则至少需要加入
溶液,为使配制过程中不出现浑浊现象,则至少需要加入_________ mL 2lnol/L的盐酸〔体积变化忽略不计)
(l)工业上,向炽热铁屑中通入氯化氢可生成无水氯化亚铁,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3,常用的试剂是
(2)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。

①以FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,同时伴随产生一种可燃性气体,该反应的化学方程式为
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开,只允许锂离子通过)工作原理为FePO4+Li
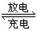 LiFePO4。如图所示,则放电时FePO4一端为电池的
LiFePO4。如图所示,则放电时FePO4一端为电池的(3)硫化亚铁常用于工业废水的处理。已知25℃时,溶度积常数Ksp[FeS]=6.3×10-18,
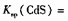 3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:
3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:在FeS、CdS的悬浊液中
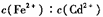 =
=(4)已知25℃时,尺,
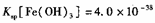 ,此温度下若在实验室中配制
,此温度下若在实验室中配制 溶液,为使配制过程中不出现浑浊现象,则至少需要加入
溶液,为使配制过程中不出现浑浊现象,则至少需要加入
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】《联合国评估报告》(联合国政府间气候变化专门委员会于2014年发布的第五份评估报告)指出,温室气体累积排放量与全球平均气温上升之间存在正相关关系。
为了缓解全球变暖和气候变化对人类的共同威胁,一项直接而有效的措施是控制和减少大气中温室气体的浓度。近年来,全世界都在努力减少二氧化碳排放。
在2020年第75届联合国大会上,中国提出力争在2030年前实现碳达峰,在2060年前实现碳中和。碳中和的技术战略包括植树造林、捕获和储存二氧化碳、扩大电动汽车等清洁能源的使用、推广可再生能源等。
使用二氧化碳作为化学原料可以通过“把废物变成财富”来增加其价值。在工业纯碱生产中, 、
、 和
和 NaCl为原料。中国著名科学家和化学工程师侯德榜发明了改进索尔维工艺的侯氏制碱法。下图显示了侯氏制碱工艺的简化流程图(Soda指纯碱,crystal指晶体)。
NaCl为原料。中国著名科学家和化学工程师侯德榜发明了改进索尔维工艺的侯氏制碱法。下图显示了侯氏制碱工艺的简化流程图(Soda指纯碱,crystal指晶体)。
(1)写出反应1的化学方程式_______ 。
(2)过程A获得的溶液中,比较离子的数量: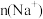 _______
_______ 
(3)侯氏制碱法工艺特点是氯化钠的利用率高。关键是 在室温下的溶解度比
在室温下的溶解度比 的溶解度
的溶解度_______ (填“高”“低”或“相等”,下同),而在低温下,前者比后者_______ 。
(4)金属—二氧化碳电池分别在阳极和阴极中使用金属和 作为活性材料,是一种具有吸引力的装置,同时固定/利用
作为活性材料,是一种具有吸引力的装置,同时固定/利用 和发电。
和发电。
以 电池为例,假设总反应为:
电池为例,假设总反应为: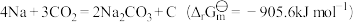 ,阳极在放电期间释放电子,金属Na在充电时沉积。
,阳极在放电期间释放电子,金属Na在充电时沉积。
①写出 电池两极的电极方程式
电池两极的电极方程式_______ 。
②在标准状态下计算该电池的标准电动势_______ 。
(5)二氧化碳被视为人类活动排放的主要温室气体。减少温室气体浓度的重要途径之一是捕获和储存 。假设1mol
。假设1mol (视为理想气体)在273.15K的温度(T)下进行等温膨胀,如果膨胀过程是可逆的,已知膨胀功
(视为理想气体)在273.15K的温度(T)下进行等温膨胀,如果膨胀过程是可逆的,已知膨胀功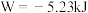 ,熵变
,熵变 。计算该过程的热量
。计算该过程的热量 、焓变
、焓变 和自由能变
和自由能变
_______ 。
为了缓解全球变暖和气候变化对人类的共同威胁,一项直接而有效的措施是控制和减少大气中温室气体的浓度。近年来,全世界都在努力减少二氧化碳排放。
在2020年第75届联合国大会上,中国提出力争在2030年前实现碳达峰,在2060年前实现碳中和。碳中和的技术战略包括植树造林、捕获和储存二氧化碳、扩大电动汽车等清洁能源的使用、推广可再生能源等。
使用二氧化碳作为化学原料可以通过“把废物变成财富”来增加其价值。在工业纯碱生产中,
 、
、 和
和 NaCl为原料。中国著名科学家和化学工程师侯德榜发明了改进索尔维工艺的侯氏制碱法。下图显示了侯氏制碱工艺的简化流程图(Soda指纯碱,crystal指晶体)。
NaCl为原料。中国著名科学家和化学工程师侯德榜发明了改进索尔维工艺的侯氏制碱法。下图显示了侯氏制碱工艺的简化流程图(Soda指纯碱,crystal指晶体)。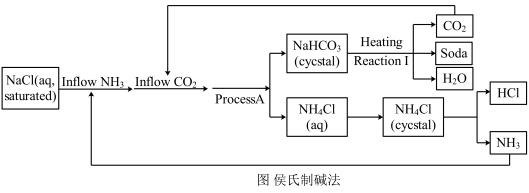
(1)写出反应1的化学方程式
(2)过程A获得的溶液中,比较离子的数量:
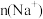 _______
_______ 
| A.多于 | B.少于 | C.等于 | D.无法确定 |
 在室温下的溶解度比
在室温下的溶解度比 的溶解度
的溶解度(4)金属—二氧化碳电池分别在阳极和阴极中使用金属和
 作为活性材料,是一种具有吸引力的装置,同时固定/利用
作为活性材料,是一种具有吸引力的装置,同时固定/利用 和发电。
和发电。以
 电池为例,假设总反应为:
电池为例,假设总反应为: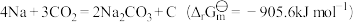 ,阳极在放电期间释放电子,金属Na在充电时沉积。
,阳极在放电期间释放电子,金属Na在充电时沉积。①写出
 电池两极的电极方程式
电池两极的电极方程式②在标准状态下计算该电池的标准电动势
(5)二氧化碳被视为人类活动排放的主要温室气体。减少温室气体浓度的重要途径之一是捕获和储存
 。假设1mol
。假设1mol (视为理想气体)在273.15K的温度(T)下进行等温膨胀,如果膨胀过程是可逆的,已知膨胀功
(视为理想气体)在273.15K的温度(T)下进行等温膨胀,如果膨胀过程是可逆的,已知膨胀功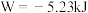 ,熵变
,熵变 。计算该过程的热量
。计算该过程的热量 、焓变
、焓变 和自由能变
和自由能变
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】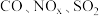 都是大气污染物,可利用化学反应原理给予消除。
都是大气污染物,可利用化学反应原理给予消除。
(1)在一定条件下利用反应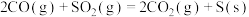 消除
消除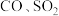 ,并获得硫黄。已知:①
,并获得硫黄。已知:①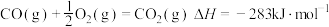 ,②
,②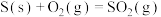
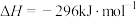 ,则
,则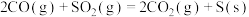

___________ 。
(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如下图所示,(Na+交换膜两侧为等体积等浓度的 溶液):
溶液):
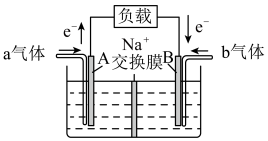
①电极A的电极反应式为___________ 。
②工作一段时间后,若B极区与A极区相差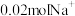 时,外电路中转移电子的物质的量是
时,外电路中转移电子的物质的量是___________ mol。
(3)利用下图所示的电化学装置可消除雾霾中的 、
、 。
。

①该装置中电子的流向是___________ (填“ ”或“
”或“ ”)。
”)。
②电极B的电极反应式为___________ 。
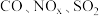 都是大气污染物,可利用化学反应原理给予消除。
都是大气污染物,可利用化学反应原理给予消除。(1)在一定条件下利用反应
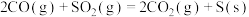 消除
消除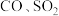 ,并获得硫黄。已知:①
,并获得硫黄。已知:①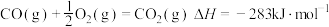 ,②
,②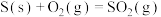
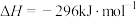 ,则
,则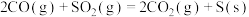

(2)利用CO还原NO的反应可消除汽车尾气引起的污染并获得电能,其简易装置如下图所示,(Na+交换膜两侧为等体积等浓度的
 溶液):
溶液):
①电极A的电极反应式为
②工作一段时间后,若B极区与A极区相差
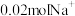 时,外电路中转移电子的物质的量是
时,外电路中转移电子的物质的量是(3)利用下图所示的电化学装置可消除雾霾中的
 、
、 。
。
①该装置中电子的流向是
 ”或“
”或“ ”)。
”)。②电极B的电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】锂系电池包括锂电池和锂离子电池,锂电池是一类由锂金属或锂合金为正/负极材料、使用非水电解质溶液的电池。1912年锂金属电池最早由GilbertN。Lewis提出并研究。20世纪70年代时,M。S。Whittingham提出并开始研究锂离子电池。
(1)全固态锂离子电池放电时电池发生反应: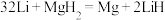 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为___________ 。
(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。
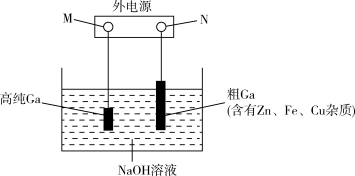
已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的___________ 极,电解精炼镓时产生的,阳极泥的主要成分是___________ 。
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式___________ 。
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=___________ (η=生成目标产物消耗的电子数÷转移的电子总数)。
(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择___________ 。少量的 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是___________ 。

(1)全固态锂离子电池放电时电池发生反应:
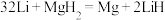 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。

已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过
 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成
 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是
您最近一年使用:0次
【推荐1】完成下列问题
(1)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理示意图如图所示:
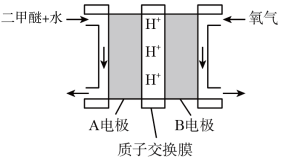
正极为___________ 电极(填“A”或“B”),H+移动方向为___________ (填“由A到B”或“由B到A”),写出A电极的电极反应式:___________ 。
(2)SO2和NOx是主要大气污染物,利用下图装置可同时吸收SO2和NO。
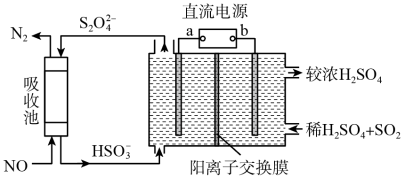
①a是直流电源的___________ 极。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为___________ 。
③用离子方程式表示吸收NO的原理___________ 。
(3)VB2-空气电池是目前储电能力最高的电池。以VB2-空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为4VB2+11O2=4B2O3+2V2O5,VB2极发生的电极反应为___________ 。

当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前CuSO4溶液的物质的量浓度是多少?(写出计算过程)___________
(1)绿色电源“直接二甲醚(CH3OCH3)燃料电池”的工作原理示意图如图所示:

正极为
(2)SO2和NOx是主要大气污染物,利用下图装置可同时吸收SO2和NO。

①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③用离子方程式表示吸收NO的原理
(3)VB2-空气电池是目前储电能力最高的电池。以VB2-空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为4VB2+11O2=4B2O3+2V2O5,VB2极发生的电极反应为

当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前CuSO4溶液的物质的量浓度是多少?(写出计算过程)
您最近一年使用:0次
【推荐2】甲烷和甲醇可以做燃料电池,具有广阔的开发和应用前景,回答下列问题


图1 图2
(1)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图1所示:通入a气体的电极是原电池的_________ 极(填“正”“负”),其电极反应式为__________________ 。
(2)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图2所示U形管中氯化钠溶液的体积为800mL.闭合K后,若每个电池甲烷用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为____________ (法拉第常数F=9.65×104C/mol,电量Q=nF),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为_______ 。


图1 图2
(1)甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图1所示:通入a气体的电极是原电池的
(2)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图2所示U形管中氯化钠溶液的体积为800mL.闭合K后,若每个电池甲烷用量均为0.224L(标况),且反应完全,则理论上通过电解池的电量为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】右图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O
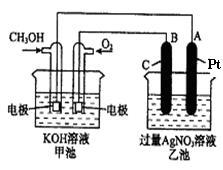
(1)请回答图中甲、乙两池的有关问题:甲池是_______________ 装置,B(石墨)电极的名称是____________ 。
(2)写出电极反应式:通入O2的电极的反应式__________ 。A(Pt)电极的反应式为_____________ ,
(3)乙池中反应的化学方程式为_______________________________ 。
(4)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中A极的质量增加5.40g时:
①甲池中理论上消耗O2体积为______________ (标准状况下);
②乙池中所得溶液的pH=____________________ 。
2CH3OH+3O2+4KOH
 2K2CO3+6H2O
2K2CO3+6H2O
(1)请回答图中甲、乙两池的有关问题:甲池是
(2)写出电极反应式:通入O2的电极的反应式
(3)乙池中反应的化学方程式为
(4)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中A极的质量增加5.40g时:
①甲池中理论上消耗O2体积为
②乙池中所得溶液的pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】在我国青海、西藏等地有许多干涸盐湖盛产一种钠盐Q。Q为一种易溶于水的白色固体。Q的水溶液用硫酸酸化,得到弱酸X。X为无色小片状透明晶体。X和甲醇在浓硫酸存在下生成易挥发的E.E在空气中点燃呈现绿色火焰。E和NaH反应得到易溶于水的白色固态化合物Z (分子量37.83)。
(1)写出由Q得到X的离子方程式________ 。
(2)写出X在水中的电离方程式_______ 。
(3)写出X和甲醇在浓硫酸存在下生成E的化学方程式________ 。
(4)写出E燃烧反应的化学方程式_____ 。
(5)写出由E和NaH制备Z的化学反应方程式______ 。
(6) Z在水溶液里的稳定性与溶液pH有关,pH越大越稳定。为什么_____ 。
(7)近年来,用Z和过氧化氢构建一种新型碱性电池已成为热门的研究课题。该电池放电时,每摩尔Z释放8摩尔电子,标准电动势大于2V。写出这种电池放电反应的离子方程式_______ 。
(1)写出由Q得到X的离子方程式
(2)写出X在水中的电离方程式
(3)写出X和甲醇在浓硫酸存在下生成E的化学方程式
(4)写出E燃烧反应的化学方程式
(5)写出由E和NaH制备Z的化学反应方程式
(6) Z在水溶液里的稳定性与溶液pH有关,pH越大越稳定。为什么
(7)近年来,用Z和过氧化氢构建一种新型碱性电池已成为热门的研究课题。该电池放电时,每摩尔Z释放8摩尔电子,标准电动势大于2V。写出这种电池放电反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。(1)用甲烷制取氢气的两步反应的能量变化如下图所示:
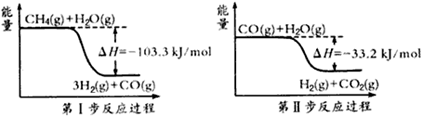
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________ 。
②第Ⅱ步反应为可逆反应。800℃时,若CO的起始浓度为2.0 mol·L-1,水蒸气的起始浓度为3.0 mol·L-1,达到化学平衡状态后,测得CO2的浓度为1.2 mol·L-1,则CO的平衡转化率为__________ 。
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B元素的化合价不变,该反应的化学方程式为___________________ ,反应消耗1mol NaBH4时转移的电子数目为_______ 。
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。
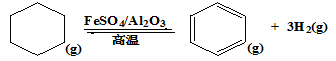
在某温度下,向恒容容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=____________________ (用含a、b的关系式表达)。
(4)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。
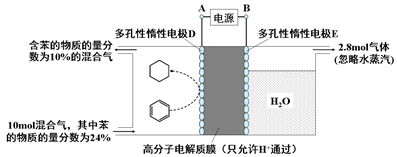
①实现有机物储氢的电极是________ ;
其电极反应方程为:________________________ 。
②该储氢装置的电流效率η明显小于100%,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是_________ 。由表中数据可知,此装置的电流效率η=______________ 。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。

①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是
②第Ⅱ步反应为可逆反应。800℃时,若CO的起始浓度为2.0 mol·L-1,水蒸气的起始浓度为3.0 mol·L-1,达到化学平衡状态后,测得CO2的浓度为1.2 mol·L-1,则CO的平衡转化率为
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B元素的化合价不变,该反应的化学方程式为
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。
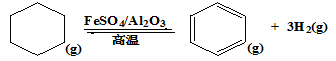
在某温度下,向恒容容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=
(4)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。

①实现有机物储氢的电极是
| A.正极 | B.负极 | C.阴极 | D.阳极 |
其电极反应方程为:
②该储氢装置的电流效率η明显小于100%,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】全球气候变暖已经成为全世界人类面临的重大问题,研究CO2的利用对促进低碳社会的构建具有重要意义。
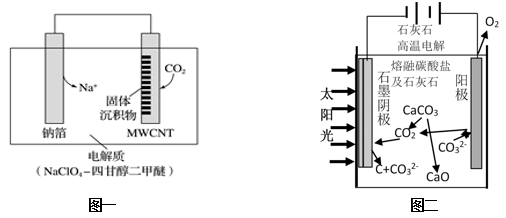
(1)利用“Na﹣CO 2”电池将CO 2变废为宝。我国科研人员研制出的可充电“Na﹣CO 2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2⇌2Na2CO3+C.放电时该电池“吸入”CO 2,其工作原理如图一所示:
①放电时,正极产物全部以固体形式沉积在电极表面,正极的电极反应式为__________________ 。
②放电时,当转移0.1mol e-时,负极质量减少_____ g。
(2)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图二所示:
①上述生产过程的能量转化方式是____________________________________ 。
②上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极放电的电极反应式为____________________________ 。

(1)利用“Na﹣CO 2”电池将CO 2变废为宝。我国科研人员研制出的可充电“Na﹣CO 2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2⇌2Na2CO3+C.放电时该电池“吸入”CO 2,其工作原理如图一所示:
①放电时,正极产物全部以固体形式沉积在电极表面,正极的电极反应式为
②放电时,当转移0.1mol e-时,负极质量减少
(2)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如图二所示:
①上述生产过程的能量转化方式是
②上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极放电的电极反应式为
您最近一年使用:0次



