电化学原理在工农业生产中有重要应用。已知肼( )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,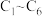 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
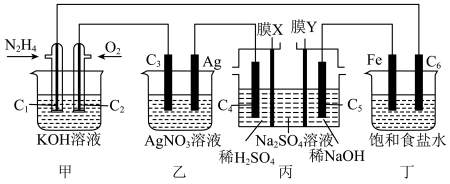
回答下列问题:
(1)甲装置中, 电极为
电极为___________ 极(填“正”“负”“阳”或“阴”), 电极的电极反应式为
电极的电极反应式为___________ 。
(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为___________ 。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为___________ 交换膜(填“阳离子”或“阴离子”)。当外电路中通过0.04mol电子时,中间 废水的质量改变了
废水的质量改变了___________ g。
(4)丁装置工作中发生反应的化学方程式为___________ 。
 )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,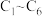 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
回答下列问题:
(1)甲装置中,
 电极为
电极为 电极的电极反应式为
电极的电极反应式为(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为
 废水的质量改变了
废水的质量改变了(4)丁装置工作中发生反应的化学方程式为
更新时间:2023-11-26 10:53:38
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】如图所示3套实验装置,分别回答下列问题。
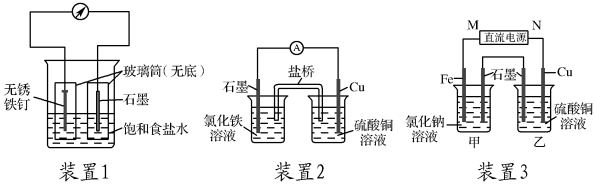
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为________ 。
(2)装置2中的石墨作________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为________ 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨附近溶液首先变红。
①电源的M端为________ 极;甲烧杯中铁极的电极反应式为________ 。
②乙烧杯中电解反应的离子方程式为___________________________
③停止通电后,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体在标准状况下的体积为________ mL。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨附近溶液首先变红。
①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止通电后,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】回答下列问题:
(1)下图是某化学兴趣小组探究化学能转变为电能的装置。_______ g。
②若电极a为Mg、电极b为Al、c为NaOH溶液,则负极电极反应式为:_______ 。
③若电极a为Fe、电极b为Cu、c为浓硝酸,则正极电极反应式为:_______ 。
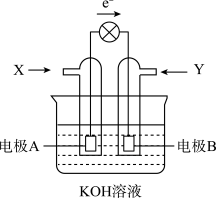
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为CH4燃料电池示意图,工作时电子流向如图所示。_______ ,电极A附近pH如何变化?_______ (填“变大”或“变小”)。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2.电池的总反应可表示为:4Li+2SOCl2= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池正极发生的电极反应式为_______ ;组装该电池必须在无水、无氧的条件下进行,原因是_______ 。
(1)下图是某化学兴趣小组探究化学能转变为电能的装置。
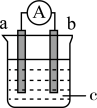
②若电极a为Mg、电极b为Al、c为NaOH溶液,则负极电极反应式为:
③若电极a为Fe、电极b为Cu、c为浓硝酸,则正极电极反应式为:
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为CH4燃料电池示意图,工作时电子流向如图所示。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl4- SOCl2.电池的总反应可表示为:4Li+2SOCl2= 4LiCl+S+ SO2。已知SOCl2会与水反应有刺激性气味的气体生成:SOCl2+ H2O=2HCl↑+ SO2↑。电池正极发生的电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。

(1)工作时,甲池内的NO3-向石墨_______ 极移动(填“I”或“II”);在相同条件下,消耗的O2和NO2的体积比为_______ 。
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的_______ 极;石墨I附近发生的电极反应式为_______ 。
(3)丙池中阳极的电极反应式为_______ ,阳极产生气体的体积为_______ L(标况下),若阴极生成气体为6.72L(标况下),则可以加入_______ 复原(填字母序号)。
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: +6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中
+6Fe2++14H+=2Cr3++6Fe3++7H2O,工作一段时间后,乙池中 减少0.1mol。
减少0.1mol。
(1)工作时,甲池内的NO3-向石墨
(2)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨I是电池的
(3)丙池中阳极的电极反应式为
A.0.3molCu(OH)2 B.0.15molCu2(OH)2CO3 C.0.3molCuO D.0.3molCuCO3
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】请回答下列问题。
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:
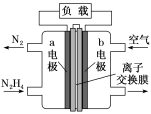
①该燃料电池中正极通入的物质是___________ ,负极发生的反应式为___________ 。
②电池工作时,OH-移向极___________ (填“a”或“b”)。
③当电池放电转移5 mol电子时,至少消耗燃料肼___________ g.
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
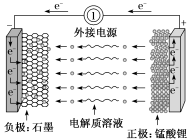
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:

①该燃料电池中正极通入的物质是
②电池工作时,OH-移向极
③当电池放电转移5 mol电子时,至少消耗燃料肼
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix
 LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
| A.放电时电池的正极反应式为Li1-xMnO4+xLi++xe-=LiMnO4 |
| B.放电过程中,石墨没有得失电子 |
| C.该电池也能在KOH溶液的环境中正常工作 |
| D.充电时电池上标有“-”的电极应与外接电源的负极相连 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】电解质溶液A:25g CuSO4·5H2O + 4mL浓H2SO4 + 200mL H2O
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
(1)正极质量改变不同的原因_______ 。
(2)电解质液中加铜粉的原因是_______ 。
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何_______ 。
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
| 电解前质量/g | 电解后质量/g | 改变量/g | ||
| 电解质液A | 正极 | 7.4 | 7.3 | -0.1 |
| 负极 | 7.5 | 7.6 | 0.1 | |
| 电解质液B | 正极 | 7.4 | 7.2 | -0.2 |
| 负极 | 7.3 | 7.5 | 0.2 |
(1)正极质量改变不同的原因
(2)电解质液中加铜粉的原因是
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】电池和电解池在日常生活中有着广泛的应用。根据所学知识完成下列题目。
Ⅰ.电化学装置如图所示
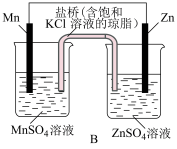
(1)已知金属活泼性: 。若装置B中负极金属的消耗速率为
。若装置B中负极金属的消耗速率为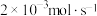 ,则盐桥中
,则盐桥中 流向
流向___________ (填“ ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为___________  。
。
Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
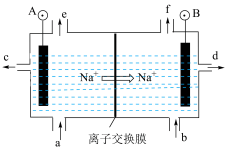
(2)①电解饱和食盐水的总反应的离子方程式是___________ 。
②在b口加入的物质为___________ (写化学式)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,供氨水式燃料电池工作原理如图2所示:
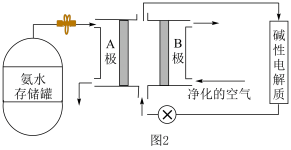
①“净化的空气”是指在进入电池装置前除去___________ (填化学式)的气体。
②氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池正极上的电极反应式是___________ 。
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为 ,图中的离子交换膜只允许
,图中的离子交换膜只允许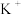 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
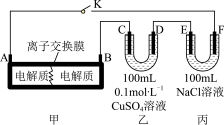
(4)装置甲中A电极为电池的___________ 极,B电极的电极反应式为___________ 。
(5)装置乙中D电极产生的气体是___________ (写化学式),体积为___________ mL(标准状况)。
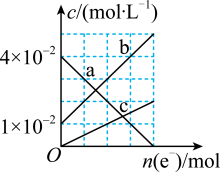
(6)若将装置丙中的 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是___________ 。
Ⅰ.电化学装置如图所示

(1)已知金属活泼性:
 。若装置B中负极金属的消耗速率为
。若装置B中负极金属的消耗速率为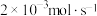 ,则盐桥中
,则盐桥中 流向
流向 ”或“
”或“ ”)溶液的迁移速率为
”)溶液的迁移速率为 。
。Ⅱ.电解饱和食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

(2)①电解饱和食盐水的总反应的离子方程式是
②在b口加入的物质为
(3)氨气是一种富氢燃料,可以直接用于燃料电池,供氨水式燃料电池工作原理如图2所示:

①“净化的空气”是指在进入电池装置前除去
②氨气燃料电池的反应原理是氨气与氧气反应生成一种常见的无毒气体和水,该电池正极上的电极反应式是
Ⅲ.如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为
 ,图中的离子交换膜只允许
,图中的离子交换膜只允许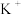 通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少1.28g。
(4)装置甲中A电极为电池的
(5)装置乙中D电极产生的气体是
(6)若将装置丙中的
 溶液改换成
溶液改换成 和
和 的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。图中生成b的电极反应式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)NH3经一系列反应可以得到HNO3和NH4NO3 , 如图所示,
在Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是:__________________________

(2)Ⅱ中,2NO(g)+ O2(g)⇌ 2NO2(g).在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图).
①p1、p2的大小关系p1________ p2(填大于、等于、小于) .
②随温度升高,该反应平衡常数变化的趋势是_________________________
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(1)再制备浓硝酸.
N2O4与O2 , H2O化合的化学方程式是______________________________
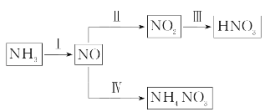
(4)Ⅳ中,电解NO制备NH4NO3 , 其原理原理如下图所示,为使电解产物全部转化为NH4NO3 , 需补充物质___________ ,说明理由:___________________ .
 .
.

在Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是:

(2)Ⅱ中,2NO(g)+ O2(g)⇌ 2NO2(g).在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下温度变化的曲线(如图).
①p1、p2的大小关系p1
②随温度升高,该反应平衡常数变化的趋势是
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(1)再制备浓硝酸.
N2O4与O2 , H2O化合的化学方程式是
(4)Ⅳ中,电解NO制备NH4NO3 , 其原理原理如下图所示,为使电解产物全部转化为NH4NO3 , 需补充物质
 .
.
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C三种强电解质,它们在水中电离出的离子如表所示:
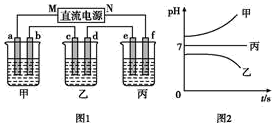
如图1所示的装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙烧杯中电极c质量增加32g。常温下各烧杯中溶液的pH与电解时间t的关系如图2。据此回答下列问题:
(1)M为电源的______ 极(填写“正”或“负”),电极b上发生的电极反应为_______ ;
(2)电极e上生成的气体在标准状态下的体积为:______ ;
(3)写出乙烧杯的电解池反应______ ;
(4)若要使丙恢复到原来的状态,正确的操作是______ 。
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42−、OH− |
如图1所示的装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙烧杯中电极c质量增加32g。常温下各烧杯中溶液的pH与电解时间t的关系如图2。据此回答下列问题:

(1)M为电源的
(2)电极e上生成的气体在标准状态下的体积为:
(3)写出乙烧杯的电解池反应
(4)若要使丙恢复到原来的状态,正确的操作是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】电化学在我们的工业生产、生活中发挥着越来越大的作用。根据题给信息,回答问题:
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。
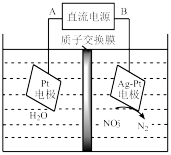
①A为直流电源的______ 极。
②Ag-Pt电极发生的电极反应为______ 。
③当阳极室溶液质量减少45g,则阴极室溶液质量减少__ g。
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:
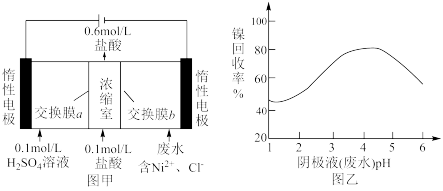
①交换膜a是____ (填“阴离子”“阳离子”)交换膜。
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:_____ 。
③当浓缩室得到1L0.6mol/L盐酸时,转移电子____ mol。
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。

①A为直流电源的
②Ag-Pt电极发生的电极反应为
③当阳极室溶液质量减少45g,则阴极室溶液质量减少
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:

①交换膜a是
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:
③当浓缩室得到1L0.6mol/L盐酸时,转移电子
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理, 其中乙装置中 X 为阳离子交换膜。
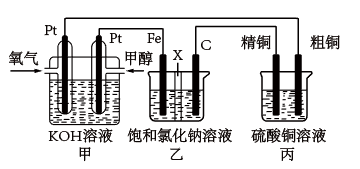
根据要求回答相关问题:
(1)写出负极的电极反应式_____
(2)写出石墨电极的电极反应式_____________
(3)反应一段时间后,乙装置中生成氢氧化钠主要在_________ (填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_________ ,反应一段时间,硫酸铜溶液浓度将_____ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子数目为_____ ;丙装置中阴极析出铜的质量为_____ 。

根据要求回答相关问题:
(1)写出负极的电极反应式
(2)写出石墨电极的电极反应式
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(5)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】电化学在生产、生活和科学研究中应用十分广泛,认识和研究化学能与电能相互转化的原理和规律具有重要意义。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。
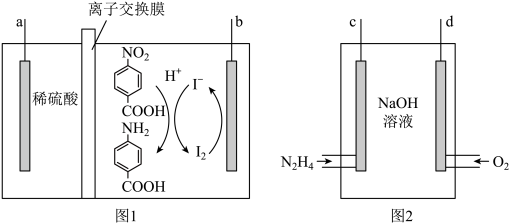
①图2为液态肼 燃料电池,c电极与
燃料电池,c电极与_______ (填“a”或“b”)相连,c电极发生的电极反应式为________ 。
②图1、图2相连时a电极为___________ (填“正”“负”“阴”或“阳”)极。生成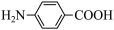 的离子方程式为
的离子方程式为___________ 。
③通过离子交换膜的离子是___________ (填离子符号);当电路中转移 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积___________ ,电解池左室质量变化___________ g。
(2)氮氧化物和 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
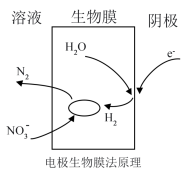
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为___________ 。
(1)有机物的电化学合成是一种环境友好的化学合成方法,图1和图2中的电极相连时可实现电化学原理制取对氨基苯甲酸。

①图2为液态肼
 燃料电池,c电极与
燃料电池,c电极与②图1、图2相连时a电极为
 的离子方程式为
的离子方程式为③通过离子交换膜的离子是
 电子时消耗标准状况下
电子时消耗标准状况下 体积
体积(2)氮氧化物和
 排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的
排放易造成酸雨及水体污染,电极生物膜法能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
,进行生物的反硝化反应。其可能反应机理如图所示。用必要的化学用语及文字来描述此过程为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】电化学在我们的工业生产、生活中发挥着越来越大的作用。根据题给信息,回答问题:
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。

①A为直流电源的______ 极。
②Ag-Pt电极发生的电极反应为______ 。
③当阳极室溶液质量减少45g,则阴极室溶液质量减少__ g。
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:

①交换膜a是____ (填“阴离子”“阳离子”)交换膜。
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:_____ 。
③当浓缩室得到1L0.6mol/L盐酸时,转移电子____ mol。
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。

①A为直流电源的
②Ag-Pt电极发生的电极反应为
③当阳极室溶液质量减少45g,则阴极室溶液质量减少
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:

①交换膜a是
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:
③当浓缩室得到1L0.6mol/L盐酸时,转移电子
您最近一年使用:0次



