电化学在我们的工业生产、生活中发挥着越来越大的作用。根据题给信息,回答问题:
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。
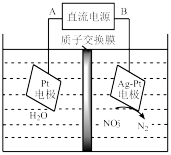
①A为直流电源的______ 极。
②Ag-Pt电极发生的电极反应为______ 。
③当阳极室溶液质量减少45g,则阴极室溶液质量减少__ g。
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:
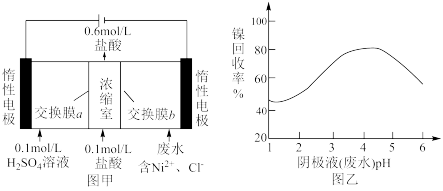
①交换膜a是____ (填“阴离子”“阳离子”)交换膜。
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:_____ 。
③当浓缩室得到1L0.6mol/L盐酸时,转移电子____ mol。
(1)电化学降解法治理硝酸盐污染的工作原理如图所示。

①A为直流电源的
②Ag-Pt电极发生的电极反应为
③当阳极室溶液质量减少45g,则阴极室溶液质量减少
(2)某工业废水中含有一定浓度的Ni2+和Cl-,现采用双膜三室电沉积法回收Ni2+。根据图甲、图乙所给信息回答下列问题:

①交换膜a是
②根据图乙分析,pH过高或过低,镍的回收率都低的原因:
③当浓缩室得到1L0.6mol/L盐酸时,转移电子
20-21高三上·山东威海·期中 查看更多[3]
山东省威海荣成市2020届高三上学期期中考试化学试题(已下线)第19讲 电解池 金属的电化学腐蚀与防护(精练)-2022年高考化学一轮复习讲练测山东省烟台市福山区第一中学2021-2022学年高三上学期9月月考化学试题.
更新时间:2020-07-28 23:59:47
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】1.
纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法:
窗体顶端
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成________ 而使Cu2O产率降低。
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =_____ 。
①阴极上的产物是________ 。
②阳极生成Cu2O,其电极反应式为_________ 。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该反应的化学方程式为____________ 。
(5)肼又称联氨,易溶于水,是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因______ 。
(6)向1L恒容密闭容器中充入0.1molN2H4,在30℃、Ni-Pt催化剂作用下发生反应N2H4(g) N2(g)+2H2(g),测得混合物体系中,
N2(g)+2H2(g),测得混合物体系中, (用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=
(用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=____ mol/(L·min);该温度下,反应的平衡常数=_______ 。
(7)肼-空气清洁燃料电池是一种碱性燃料电池,电解质溶液时20%-30%的KOH溶液。肼-空气燃料电池放电时,负极的电极反应式是_________ 。电池工作一点时间后,电解质溶液的pH将_______ (填“增大”、“减小”、“不变”)。
纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法:
窗体顶端
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,反应为2Cu+H2O Cu2O+H2↑。 Cu2O+H2↑。 |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,电解装置如下图所示。

①阴极上的产物是
②阳极生成Cu2O,其电极反应式为
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该反应的化学方程式为
(5)肼又称联氨,易溶于水,是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因
(6)向1L恒容密闭容器中充入0.1molN2H4,在30℃、Ni-Pt催化剂作用下发生反应N2H4(g)
 N2(g)+2H2(g),测得混合物体系中,
N2(g)+2H2(g),测得混合物体系中, (用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=
(用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=
(7)肼-空气清洁燃料电池是一种碱性燃料电池,电解质溶液时20%-30%的KOH溶液。肼-空气燃料电池放电时,负极的电极反应式是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】电化学原理在污染治理方面有着重要的作用。回答下列问题:
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:
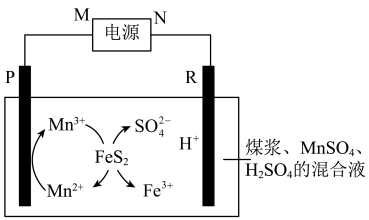
已知:两电极为完全相同的惰性电极。
(1)M为电源的___________ 极。
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式___________ 。
(3)电解池工作时,混合液中 的物质的量
的物质的量___________ (填“变大”、“变小”或“不变”)。
(4)电解过程中,混合溶液中的pH将___________ (填“变大”、“变小”或“不变”),理由是___________ 。
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:
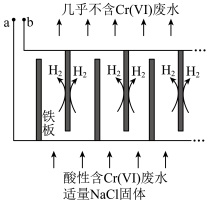
(5)酸性废水中的 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为___________ 。
(6)为了使 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中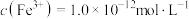 ,则溶液中
,则溶液中
___________  。{已知
。{已知 ,
,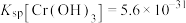 }
}
(7)随着电解的进行,阳极铁板会发生钝化,表面形成 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:___________ 。
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:

已知:两电极为完全相同的惰性电极。
(1)M为电源的
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(3)电解池工作时,混合液中
 的物质的量
的物质的量(4)电解过程中,混合溶液中的pH将
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:

(5)酸性废水中的
 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为(6)为了使
 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中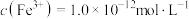 ,则溶液中
,则溶液中
 。{已知
。{已知 ,
,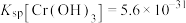 }
}(7)随着电解的进行,阳极铁板会发生钝化,表面形成
 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】镍氢电池是二十世纪九十年代发展起来的一种新型绿色电池,具有高能量、长寿命、无污染等特点。用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示。电池的总反应式为:


(如图) (如图)
(1)①镍氢电池充电时,镍电极连接直流电源的___________ 极。阳极的电极反应式为____________ 。
②镍氢电池放电时,OH-移向____________ (填“碳电极”或“镍电极”)。
(2)除了用纳米碳管等材料储氢外,还可使用有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。一定条件下,利用如图装置可实现有机物的电化学储氢(忽略其它有机物)。
①A为电源的____________ 极。
②电极E上产生的气体为____________ 。
③电极D的电极反应式为______________________________ 。



(如图) (如图)
(1)①镍氢电池充电时,镍电极连接直流电源的
②镍氢电池放电时,OH-移向
(2)除了用纳米碳管等材料储氢外,还可使用有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。一定条件下,利用如图装置可实现有机物的电化学储氢(忽略其它有机物)。
①A为电源的
②电极E上产生的气体为
③电极D的电极反应式为
您最近一年使用:0次
【推荐1】一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4的原理和粗铜的精炼原理。
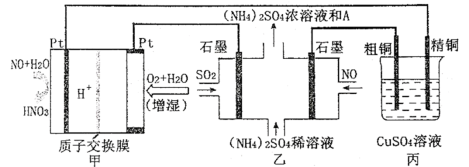
(1)燃料电池放电过程中负极的电极反应式____ 。
(2)乙装置中物质A是____ (填化学式),理由是___ ;电解过程中阳极附近pH___ (填“增大”“减小”或“不变”),阴极的电极反应式是____ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将__ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有____ mol;丙装置中阴极析出铜的质量为___ g。

(1)燃料电池放电过程中负极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质的量共有
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
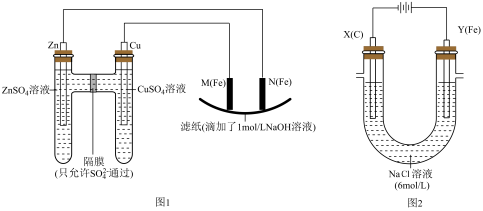
请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是_________ (填字母序号).
(2)M极发生反应的电极反应式为_________ ;
(3)实验过程中,SO
_________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有_________ ,写出产生此现象的反应方程式:_________ ;
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH_________ (填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少_________ g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为_________ 。

请回答:
Ⅰ.用如图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,能替代Cu做电极的是
| A.铝 | B.石墨 | C.镁 | D.铂 |
(3)实验过程中,SO

Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-═FeO42-+4H2O 和 4OH--4e-═2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(6)在碱性锌电池中,用高铁酸钾作为正极材料, 电池总反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为
您最近一年使用:0次
【推荐3】数十年来,化学工作者对氮的氧化物、碳的氧化物做了广泛深入的研究并取得一些重要成果。
I.已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
第一步:2NO(g) N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)
N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)
第二步:N2O2(g)+O2(g) 2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=____________ ;
II.利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放
已知重整过程中部分反应的热化方程式为:
①CH4(g)=C(s)+2H2(g)ΔH>0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
③CO(g)+H2(g)=C(s)+H2O(g)ΔH<0
固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。

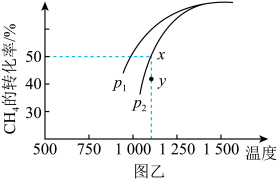
在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g)+CH4(g) 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)
2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)_____ v(逆)(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。用平衡分压代替平衡浓度可以得到平衡常数Kp,已知P2=aPa求x点对应温度下反应的平衡常数Kp=__________________ 。
III.根据2 +2H+
+2H+
 +H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的____________ 极,电解制备过程的总反应的离子方程式为____________ 。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为____________ 。若选择用熔融K2CO3作介质的甲烷燃料电池充当电源,则负极反应式为____________ 。

I.已知2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:第一步:2NO(g)
 N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)
N2O2(g)(快)∆H1<0;v1正=k1正c2(NO);v1逆=k1逆c(N2O2)第二步:N2O2(g)+O2(g)
 2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)
2NO2(g)(慢)∆H2<0;v2正=k2正c(N2O2)c(O2);v2逆=k2逆c2(NO2)一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=II.利用CO2和CH4重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放
已知重整过程中部分反应的热化方程式为:
①CH4(g)=C(s)+2H2(g)ΔH>0
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH>0
③CO(g)+H2(g)=C(s)+H2O(g)ΔH<0
固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。


在密闭容器中通入物质的量均为0.1mol的CH4和CO2,在一定条件下发生反应CO2(g)+CH4(g)
 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)
2CO(g)+2H2(g),CH4的平衡转化率与温度及压强(单位Pa)的关系如图乙所示。y点:v(正)III.根据2
 +2H+
+2H+
 +H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中左侧电极连接电源的
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】用惰性电极电解法制备硼酸[ 或
或 ]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知
]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知 与
与 的性质相似。回答下列问题:
的性质相似。回答下列问题:____________ ;
(2)B、C膜分别是________________ ;(填“阳离子交换膜”或“阴离子交换膜”)
(3)b极的电极反应式为_____________ ;
(4)产品室中发生的反应离子方程式是______________ ;
(5)每增加1mol 产品,NaOH溶液增重
产品,NaOH溶液增重____________ g。
 或
或 ]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知
]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。已知 与
与 的性质相似。回答下列问题:
的性质相似。回答下列问题:
(2)B、C膜分别是
(3)b极的电极反应式为
(4)产品室中发生的反应离子方程式是
(5)每增加1mol
 产品,NaOH溶液增重
产品,NaOH溶液增重
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】已知电解NaOH溶液即电解水:2H2O 2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。
2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。
(1)在阴极产生的氢气的体积(按标准状况计)为______
(2)阳极产生的氧气的物质的量为__________
(3)假定控制条件使Cl2未从电解液中逸出,电解结束后经充分搅拌Cl2与NaOH发生了完全反应,生成NaClO和部分NaClO3。求完全反应后电解池中三种钠盐的总质量____
 2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。
2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。(1)在阴极产生的氢气的体积(按标准状况计)为
(2)阳极产生的氧气的物质的量为
(3)假定控制条件使Cl2未从电解液中逸出,电解结束后经充分搅拌Cl2与NaOH发生了完全反应,生成NaClO和部分NaClO3。求完全反应后电解池中三种钠盐的总质量
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。

(1)甲装置中,a电极的反应式为_______________________________ 。
(2)乙装置中,阴极区产物为____________ 。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为________ (填“正”或“负”)极,该装置内发生反应的化学方程式为________________ 、______________ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为____________ (不考虑气体的溶解)。
(5)某工厂采用电解法处理含 Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为 Cr3+,Cr3+在阴极区生成 Cr(OH)3 沉淀除去,工作原理如图
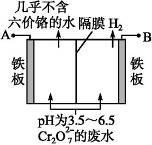
①写出电解时阴极的电极反应式______________________________ 。
②写出 Cr2O72-被还原为 Cr3+的离子方程式____________________________ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
(5)某工厂采用电解法处理含 Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为 Cr3+,Cr3+在阴极区生成 Cr(OH)3 沉淀除去,工作原理如图

①写出电解时阴极的电极反应式
②写出 Cr2O72-被还原为 Cr3+的离子方程式
您最近一年使用:0次



