电解质溶液A:25g CuSO4·5H2O + 4mL浓H2SO4 + 200mL H2O
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
(1)正极质量改变不同的原因_______ 。
(2)电解质液中加铜粉的原因是_______ 。
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何_______ 。
电解质溶液B:16g CuCl+ 100mL浓HCIl+ 100mL H2O + 4g铜粉
以铜为电极,通电电解串连的两个电解槽(分别盛电解质溶液A和电解质溶液B)。正极质量改变如下表所示:
| 电解前质量/g | 电解后质量/g | 改变量/g | ||
| 电解质液A | 正极 | 7.4 | 7.3 | -0.1 |
| 负极 | 7.5 | 7.6 | 0.1 | |
| 电解质液B | 正极 | 7.4 | 7.2 | -0.2 |
| 负极 | 7.3 | 7.5 | 0.2 |
(1)正极质量改变不同的原因
(2)电解质液中加铜粉的原因是
(3)从理论上讲,电解过程铜粉质量不会改变,为什么?实际情况如何
更新时间:2021-08-23 15:17:13
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】I.控制变量法是化学实验中的—种常用方法,如表是某课外兴趣小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点—位),分析以下数据,回答下列问题:
(1)实验①和实验②表明_____ 对反应速率有影响;研究锌的形状对反应速率的影响时,最好选取实验_______ (填3个实验序号)。
(2)下列数据推断正确的是______________________ 。
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是___________________________________ 。
(4)根据表中数据计算:硫酸的物质的量浓度是_________________ mol/L。
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g) N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
(1) 0〜15min 内,v(CO2) =__________________ 。
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是______ (填对应字母)。
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g) NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是_____
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
序号 | 硫酸的体积 /mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的 时间/s | 生成硫酸锌的质量/g |
| ① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
| ② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
| ③ | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
| ④ | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
| ⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| ⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
| ⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
| ⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
| ⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | 19.3 |
(1)实验①和实验②表明
(2)下列数据推断正确的是
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是
(4)根据表中数据计算:硫酸的物质的量浓度是
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g)
 N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。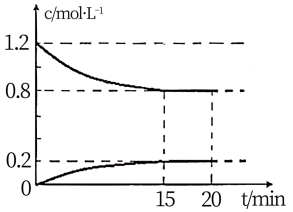
(1) 0〜15min 内,v(CO2) =
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是
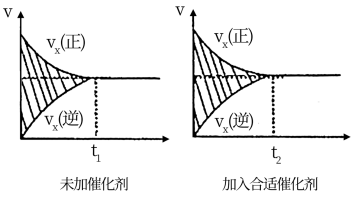
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g)
 NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(I有甲、乙两位学生均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入3mol·L—1H2SO4溶液中,乙同学将电极放入3mol·L-1的NaOH溶液中,如图所示。
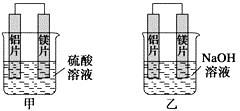
(1)写出甲池中总反应的离子方程式:_______________ 正极为:_______ (填“铝片”或“镁片”),该电池工作一段时间后,溶液的pH值________ (填“变大”“变小”或“不变”)。
(2)写出乙池中总反应的离子方程式:_____________________________________ ;工作时氢氧根离子往_____ (填“正极”或“负极”)迁移。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________ 活动性更强,而乙会判断出__________ 活动性更强(填写元素符号)。
(4)通过上述实验分析,“直接利用金属活动性顺序判断原电池的正负极”这种做法可靠吗?_________ (填“是”或“否”)若填是,下问不用回答;若填否,请写出一种判断原电池正负极的可行的实验方法。________
(5)某鱼雷采用Al-Ag2O动力电池,以溶解有氢氧化钾的流动海水为电解液,电池反应为:2Al+3Ag2O+2KOH=6Ag+2KAlO2+H2O,则该电池的负极为_______
正极离子反应式为:________________________________________________________

(1)写出甲池中总反应的离子方程式:
(2)写出乙池中总反应的离子方程式:
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出
(4)通过上述实验分析,“直接利用金属活动性顺序判断原电池的正负极”这种做法可靠吗?
(5)某鱼雷采用Al-Ag2O动力电池,以溶解有氢氧化钾的流动海水为电解液,电池反应为:2Al+3Ag2O+2KOH=6Ag+2KAlO2+H2O,则该电池的负极为
正极离子反应式为:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】如图是某同学设计的一个简易的原电池装置,回答下列问题。
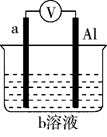
(1)若a为镁、b为CuCl2,则正极材料为_____ ,负极上的电极反应式为_________ 。
(2)若a为镁、b为NaOH,则Mg极上发生________ 反应(填“氧化”或“还原”),负极上的电极反应式为_______________ 。
(3)若a为铜、b为浓硝酸,则电流的方向为____ →___ (填电极材料),正极上的电极反应式为______ 。
(4)上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑________ 。

(1)若a为镁、b为CuCl2,则正极材料为
(2)若a为镁、b为NaOH,则Mg极上发生
(3)若a为铜、b为浓硝酸,则电流的方向为
(4)上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】请回答下列问题。
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:
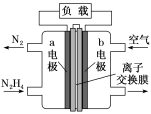
①该燃料电池中正极通入的物质是___________ ,负极发生的反应式为___________ 。
②电池工作时,OH-移向极___________ (填“a”或“b”)。
③当电池放电转移5 mol电子时,至少消耗燃料肼___________ g.
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
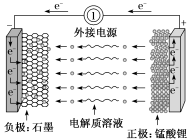
(1)肼—空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,回答下列问题:

①该燃料电池中正极通入的物质是
②电池工作时,OH-移向极
③当电池放电转移5 mol电子时,至少消耗燃料肼
(2)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电池反应式为:Li1-xMnO4+Lix
 LiMnO4,下列有关说法不正确的是___________(填字母)。
LiMnO4,下列有关说法不正确的是___________(填字母)。
| A.放电时电池的正极反应式为Li1-xMnO4+xLi++xe-=LiMnO4 |
| B.放电过程中,石墨没有得失电子 |
| C.该电池也能在KOH溶液的环境中正常工作 |
| D.充电时电池上标有“-”的电极应与外接电源的负极相连 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】请回答下列问题:
I:某兴趣小组依据反应 探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。
探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。________ (填“有”或“无”,下同)氧化还原反应发生,导线上________ 电流产生。
(2)连接K,锌片上的电极反应式为________ 。 后测得锌片和铜片之间的质量差为
后测得锌片和铜片之间的质量差为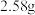 ,则导线中通过电子的物质的量为
,则导线中通过电子的物质的量为________  。
。
(3)若连接K一段时间后,实际测得铜片质量增加 ,同时锌片质量减少
,同时锌片质量减少 ,那么这段时间内该装置消耗的化学能转化为电能的百分比为
,那么这段时间内该装置消耗的化学能转化为电能的百分比为________ 。
II:常温下,将除去表面氧化膜的铝片、铜片插入浓 中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间
中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间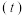 的变化如图乙所示,反应过程中有红棕色气体产生。
的变化如图乙所示,反应过程中有红棕色气体产生。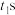 前,该原电池的正极反应式为
前,该原电池的正极反应式为________ 。
(5)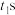 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是________ 。
I:某兴趣小组依据反应
 探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。
探究原电池的工作原理,将质量相等的锌片和铜片用导线相连浸入足量硫酸铜溶液中构成如图装置。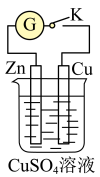
(2)连接K,锌片上的电极反应式为
 后测得锌片和铜片之间的质量差为
后测得锌片和铜片之间的质量差为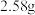 ,则导线中通过电子的物质的量为
,则导线中通过电子的物质的量为 。
。(3)若连接K一段时间后,实际测得铜片质量增加
 ,同时锌片质量减少
,同时锌片质量减少 ,那么这段时间内该装置消耗的化学能转化为电能的百分比为
,那么这段时间内该装置消耗的化学能转化为电能的百分比为II:常温下,将除去表面氧化膜的铝片、铜片插入浓
 中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间
中组成原电池装置(如图甲),测得原电池的电流强度(I)随时间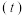 的变化如图乙所示,反应过程中有红棕色气体产生。
的变化如图乙所示,反应过程中有红棕色气体产生。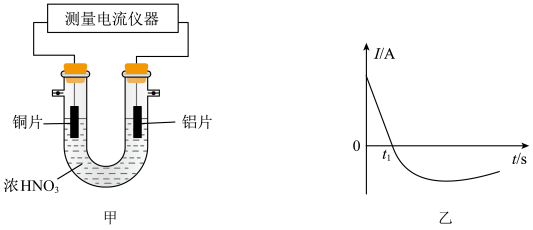
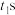 前,该原电池的正极反应式为
前,该原电池的正极反应式为(5)
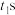 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】电化学原理在工农业生产中有重要应用。已知肼( )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,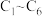 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
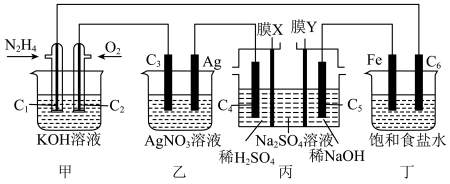
回答下列问题:
(1)甲装置中, 电极为
电极为___________ 极(填“正”“负”“阳”或“阴”), 电极的电极反应式为
电极的电极反应式为___________ 。
(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为___________ 。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为___________ 交换膜(填“阳离子”或“阴离子”)。当外电路中通过0.04mol电子时,中间 废水的质量改变了
废水的质量改变了___________ g。
(4)丁装置工作中发生反应的化学方程式为___________ 。
 )是一种重要的清洁高能燃料。下列装置中,
)是一种重要的清洁高能燃料。下列装置中,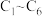 均为石墨电极,假设各装置在工作过程中溶液的体积不变。
均为石墨电极,假设各装置在工作过程中溶液的体积不变。
回答下列问题:
(1)甲装置中,
 电极为
电极为 电极的电极反应式为
电极的电极反应式为(2)若乙装置中溶液的体积为400mL,起始时溶液的pH为6,当外电路中通过0.04mol电子时,溶液的pH约为
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱和氢气,水分子不能通过膜X和膜Y。膜X为
 废水的质量改变了
废水的质量改变了(4)丁装置工作中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】金在自然界中主要以分散的单质形式存在,需要先富集再提炼。富集后的精矿用混汞法、氰化法。等工艺提取金。混汞法是使矿浆中的金粒与汞生成金汞齐,然后蒸去汞得到海绵金(又称汞金)。氰化法是在氧化剂(如空气或氧气)存在下,用可溶性氰化物(如NaCN)溶液浸出矿石中的金(浸出产物为[Au(CN)2]- ),再用置换法或电沉积法从浸出液中回收金。
(1)写出用氰化物溶金反应和用Zn粉置换金的化学反应方程式_________ 。
(2)已知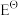 (O2/H2O)=1.229V,
(O2/H2O)=1.229V,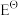 (Au+ /Au)=1, 69 V,
(Au+ /Au)=1, 69 V, 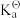 (HCN)=4.93 ×10-10,β2([Au(CN)2]-)= 2. 00× 1038,F=96.485 J·V-1·mol-1。设配制的NaCN水溶液的浓度为1.00 ×10-3 mol/L、生成的[ Au(CN)2]-配离子的浓度为1.00 ×10-4 mol/L、空气中O2的体积分数为0.210,计算298K时在空气中溶金反应的自由能变
(HCN)=4.93 ×10-10,β2([Au(CN)2]-)= 2. 00× 1038,F=96.485 J·V-1·mol-1。设配制的NaCN水溶液的浓度为1.00 ×10-3 mol/L、生成的[ Au(CN)2]-配离子的浓度为1.00 ×10-4 mol/L、空气中O2的体积分数为0.210,计算298K时在空气中溶金反应的自由能变_________ 。
(3)当电极反应中有H+或OH-时,其电极电势E将受pH的影响,E-pH图体现了这种影响。E-pH图上有3种类型的线:电极反应的E与 pH有关,为有一定斜率的直线;电极反应的E与pH无关,是一条平行于横坐标的直线;非氧化还原反应,是一条平行于纵坐标的直线。
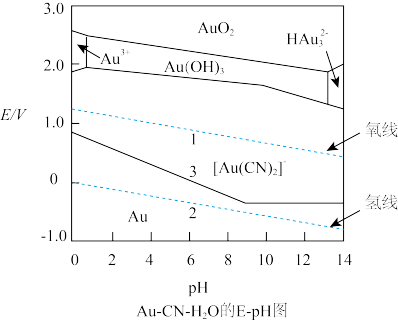
电对的E-pH线的,上方,是该电对的氧化型。的稳定区,E -pH线的下方,是还原型的稳定区;位于高位置线的氧化型易与低位置线的还原型反应;各曲线的交点所处的E和pH,是各电极的氧化型和还原型共存的条件。下图是氰化法溶金过程的Au-CN- H2O系统的E-pH图,试借助该图对溶金反应和溶金的工艺条件进行讨论_________ 。
(1)写出用氰化物溶金反应和用Zn粉置换金的化学反应方程式
(2)已知
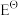 (O2/H2O)=1.229V,
(O2/H2O)=1.229V,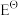 (Au+ /Au)=1, 69 V,
(Au+ /Au)=1, 69 V, 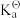 (HCN)=4.93 ×10-10,β2([Au(CN)2]-)= 2. 00× 1038,F=96.485 J·V-1·mol-1。设配制的NaCN水溶液的浓度为1.00 ×10-3 mol/L、生成的[ Au(CN)2]-配离子的浓度为1.00 ×10-4 mol/L、空气中O2的体积分数为0.210,计算298K时在空气中溶金反应的自由能变
(HCN)=4.93 ×10-10,β2([Au(CN)2]-)= 2. 00× 1038,F=96.485 J·V-1·mol-1。设配制的NaCN水溶液的浓度为1.00 ×10-3 mol/L、生成的[ Au(CN)2]-配离子的浓度为1.00 ×10-4 mol/L、空气中O2的体积分数为0.210,计算298K时在空气中溶金反应的自由能变(3)当电极反应中有H+或OH-时,其电极电势E将受pH的影响,E-pH图体现了这种影响。E-pH图上有3种类型的线:电极反应的E与 pH有关,为有一定斜率的直线;电极反应的E与pH无关,是一条平行于横坐标的直线;非氧化还原反应,是一条平行于纵坐标的直线。
电对的E-pH线的,上方,是该电对的氧化型。的稳定区,E -pH线的下方,是还原型的稳定区;位于高位置线的氧化型易与低位置线的还原型反应;各曲线的交点所处的E和pH,是各电极的氧化型和还原型共存的条件。下图是氰化法溶金过程的Au-CN- H2O系统的E-pH图,试借助该图对溶金反应和溶金的工艺条件进行讨论

您最近一年使用:0次
【推荐2】气态废气物中的硫化氢可用下法转化为可利用的硫:配制一份电解溶液,主要成分为:K4[Fe(CN)6](200g/L)和KHCO3(60g/L);通电电解,控制电解池的电流密度和槽电压,通入H2S气体。写出相应的反应式_______ 。已知:φ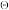 [
[ /
/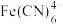 ]=0.35V;KHCO3溶液中的φ(H+/H2)~-0.5V;φ(S/S2-)~-0.3V
]=0.35V;KHCO3溶液中的φ(H+/H2)~-0.5V;φ(S/S2-)~-0.3V
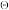 [
[ /
/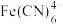 ]=0.35V;KHCO3溶液中的φ(H+/H2)~-0.5V;φ(S/S2-)~-0.3V
]=0.35V;KHCO3溶液中的φ(H+/H2)~-0.5V;φ(S/S2-)~-0.3V
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】某同学设计实验探究不同电极和电解液对电解水的影响。分别采用石墨和铁钉作为电解材料,电解硫酸和氢氧化钠溶液。预电解2分钟后收集3~8分钟内产生的气体,实验结果如下表所示:
已知氢气和氧气在水中溶解度分别为19 mol·L-1和31 mol·L-1,根据上述测定结果,回答下列问题:
(1)本实验可用如图所示装置收集并测量气体的体积。请简述读取气体体积的操作方法___________ 。

(2)该同学为探究①②中阳极气体偏少的原因(偏离V阳:V阴=1:2),又进行如下实验: 。
a.电解结束后对两电极气体同时减压,发现电极表面再次冒出气泡,相比而言,阳极冒出气体更多。
b.取②实验中少数阳极溶液,分为两份,一份加入稀盐酸溶液,生成无色气体,另一份滴加氯化钡溶液,生成白色沉淀;而取③实验中少数阳极溶液重复上述实验,无类似现象。
c.取①实验中少量阳极溶液,滴加硫酸锰溶液,逐渐变紫红色。
根据a、b、c实验得出的结论___________ 。
(3)另一同学发现③中气体体积比V阳:V阴≈1:2,说明铁作阳极未失去电子产生亚铁离子,其可能的原因是___________ 。
(4)比较实验结果,选择电解水的条件是___________ 。
| 编号 | 电极 | 电解液 | 阳极气体体积/mL | 阴极气体体积/mL | 实验现象 |
| ① | 石墨 | 0.5 mol·L-1硫酸 | 5.55 | 21.88 | 两电极表面产生气泡,阳极管底积有黑色粉末 |
| ② | 石墨 | 1 mol·L-1氢氧化钠 | 5.00 | 16.08 | 两电极表面产生气泡,阳极溶液变黄色 |
| ③ | 铁钉 | 1 mol·L-1氢氧化钠 | 9.13 | 18.22 | 两电极表面产生气泡 |
已知氢气和氧气在水中溶解度分别为19 mol·L-1和31 mol·L-1,根据上述测定结果,回答下列问题:
(1)本实验可用如图所示装置收集并测量气体的体积。请简述读取气体体积的操作方法

(2)该同学为探究①②中阳极气体偏少的原因(偏离V阳:V阴=1:2),又进行如下实验: 。
a.电解结束后对两电极气体同时减压,发现电极表面再次冒出气泡,相比而言,阳极冒出气体更多。
b.取②实验中少数阳极溶液,分为两份,一份加入稀盐酸溶液,生成无色气体,另一份滴加氯化钡溶液,生成白色沉淀;而取③实验中少数阳极溶液重复上述实验,无类似现象。
c.取①实验中少量阳极溶液,滴加硫酸锰溶液,逐渐变紫红色。
根据a、b、c实验得出的结论
(3)另一同学发现③中气体体积比V阳:V阴≈1:2,说明铁作阳极未失去电子产生亚铁离子,其可能的原因是
(4)比较实验结果,选择电解水的条件是
您最近一年使用:0次



