I.控制变量法是化学实验中的—种常用方法,如表是某课外兴趣小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点—位),分析以下数据,回答下列问题:
(1)实验①和实验②表明_____ 对反应速率有影响;研究锌的形状对反应速率的影响时,最好选取实验_______ (填3个实验序号)。
(2)下列数据推断正确的是______________________ 。
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是___________________________________ 。
(4)根据表中数据计算:硫酸的物质的量浓度是_________________ mol/L。
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g) N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
(1) 0〜15min 内,v(CO2) =__________________ 。
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是______ (填对应字母)。
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g) NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是_____
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
序号 | 硫酸的体积 /mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的 时间/s | 生成硫酸锌的质量/g |
| ① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
| ② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
| ③ | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
| ④ | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
| ⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| ⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
| ⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
| ⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
| ⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | 19.3 |
(1)实验①和实验②表明
(2)下列数据推断正确的是
A. t1<70 B.t1>t4C.m12D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是
(4)根据表中数据计算:硫酸的物质的量浓度是
II.已知在 25℃、l0l kPa 下,2NO(g)+2CO(g)
 N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。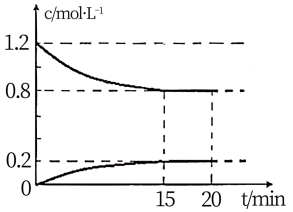
(1) 0〜15min 内,v(CO2) =
(2)该反应的速率时间图象如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如下图中右图所示。以下说法正确的是
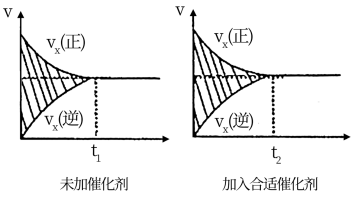
A.a1>a2B.b12C.t1>t2
(3) 一定条件下,已知反应NO2(g)+SO2(g)
 NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是
NO(g)+SO3(g),将NO2与SO2以体积比1 :2置于2L密闭容器中发生上述反应,下列能说明该反应达到平衡状态的是a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
更新时间:2017-05-16 20:03:38
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)  CO2(g)+H2(g), 某研究小组分别在体积均为2 L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
CO2(g)+H2(g), 某研究小组分别在体积均为2 L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
(1)容器③中反应达平衡时,CO的转化率为____________ 。
(2)容器①中反应达平衡这段时间,化学反应速率v (H2) =_______________ 。
(3)下列叙述正确的是_____________ (填字母序号)。
a.平衡时,容器①和容器②中CO2的体积分数相等
b.反应达平衡状态时,Q2 > Q1 > 32.8 kJ
c.达到平衡的时间:t2 > t1>2.5 min
d.该反应的热化学方程式可表示为:CO(g)+H2O(g) CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
 CO2(g)+H2(g), 某研究小组分别在体积均为2 L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:
CO2(g)+H2(g), 某研究小组分别在体积均为2 L的恒容密闭容器中加入一定量的反应物,使其发生反应,相关数据如下:| 容器 编号 | 温度 /℃ | 起始量/mol | 平衡量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||
| CO | H2O | CO2 | H2 | ||||
| ① | 650 | 1 | 2 | 0.4 | 0.4 | 5 | 16.4kJ |
| ② | 650 | 2 | 4 | t1 | Q1 kJ | ||
| ③ | 900 | 2 | 4 | 1.6 | 1.6 | t2 | Q2 kJ |
(2)容器①中反应达平衡这段时间,化学反应速率v (H2) =
(3)下列叙述正确的是
a.平衡时,容器①和容器②中CO2的体积分数相等
b.反应达平衡状态时,Q2 > Q1 > 32.8 kJ
c.达到平衡的时间:t2 > t1>2.5 min
d.该反应的热化学方程式可表示为:CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】一定温度下,向容积为2L的密闭容器中通入3 molA和2mol B,混合气体起始压强为p0。发生如下反应:3A(g)+B(g) xC(g)+ 2D(s),反应进行到1min时测得剩余1.2molA,此时C的浓度为0.6mol/L。反应进行到2min时该容器内混合气体总压强为p,5min后反应达到平衡。
xC(g)+ 2D(s),反应进行到1min时测得剩余1.2molA,此时C的浓度为0.6mol/L。反应进行到2min时该容器内混合气体总压强为p,5min后反应达到平衡。
(1)X为_________ 。
(2)反应在1min内,B的平均反应速率为_______ ;
(3)请用p0、p来表示2min时反应物B的转化率为_______________ %。
(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是_____ ;
A.v(A)=0.5 mol·L-1·min-1; B.v(B)=0.2 mol·L-1·min-1;C.v(C)=0.3 mol·L-1·min-1;D.v(D)=0.9 mol·L-1·min-1;
 xC(g)+ 2D(s),反应进行到1min时测得剩余1.2molA,此时C的浓度为0.6mol/L。反应进行到2min时该容器内混合气体总压强为p,5min后反应达到平衡。
xC(g)+ 2D(s),反应进行到1min时测得剩余1.2molA,此时C的浓度为0.6mol/L。反应进行到2min时该容器内混合气体总压强为p,5min后反应达到平衡。(1)X为
(2)反应在1min内,B的平均反应速率为
(3)请用p0、p来表示2min时反应物B的转化率为
(4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1; B.v(B)=0.2 mol·L-1·min-1;C.v(C)=0.3 mol·L-1·min-1;D.v(D)=0.9 mol·L-1·min-1;
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:① ;②
;② 。反应体系中组分M、Z的浓度随时间变化情况如图所示。
。反应体系中组分M、Z的浓度随时间变化情况如图所示。
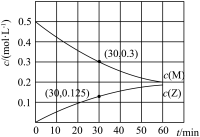
(1)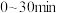 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为___________ 。
(2)其中,反应①的速率可以表示为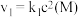 ,反应②的速率可以表示为
,反应②的速率可以表示为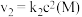 (
( 、
、 为速率常数)。下列说法正确的是___________。
为速率常数)。下列说法正确的是___________。
 ;②
;② 。反应体系中组分M、Z的浓度随时间变化情况如图所示。
。反应体系中组分M、Z的浓度随时间变化情况如图所示。
(1)
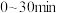 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为(2)其中,反应①的速率可以表示为
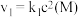 ,反应②的速率可以表示为
,反应②的速率可以表示为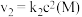 (
( 、
、 为速率常数)。下列说法正确的是___________。
为速率常数)。下列说法正确的是___________。A.反应开始后,系统中 和 和 的浓度之比保持不变 的浓度之比保持不变 |
B.如果反应能进行到底,则反应结束时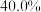 的M能转化为 的M能转化为 |
C.该温度下,两个反应的 与 与 一定都小于0 一定都小于0 |
D.该温度下,两个反应 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】一位科学家利用Zn 与某浓度的盐酸反应研究影响化学反应速率的因素,他得到的实验数据如下:

利用上述数据,完成下列问题:
(1)画出时间对温度的曲线图。___________
(2)利用所画的曲线图和上述实验数据,得出关于温度影响反应速率的什么结论?___________
(3)对比数据B与F,解释F溶于酸那么快的原因。___________

利用上述数据,完成下列问题:
(1)画出时间对温度的曲线图。
(2)利用所画的曲线图和上述实验数据,得出关于温度影响反应速率的什么结论?
(3)对比数据B与F,解释F溶于酸那么快的原因。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】下列说法正确的是________ 。
①可逆反应2NO2(g) 2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO2,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO2,能说明该反应已达到平衡状态
②可逆反应2NO2(g) 2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO,能说明该反应已达到平衡状态
③可逆反应2NO2(g) 2NO(g)+O2(g),在容积固定的密闭容器中,用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态,能说明该反应已达到平衡状态
④可逆反应2NO2(g) 2NO(g)+O2(g),在容积固定的密闭容器中,混合气体的颜色、密度、压强、平均相对分子质量不再改变,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,混合气体的颜色、密度、压强、平均相对分子质量不再改变,能说明该反应已达到平衡状态
⑤一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),混合气体的密度、压强、总物质的量、B的物质的量浓度、混合气体的平均相对分子质量不再改变的状态,能表明该反应已达到平衡状态
C(g)+D(g),混合气体的密度、压强、总物质的量、B的物质的量浓度、混合气体的平均相对分子质量不再改变的状态,能表明该反应已达到平衡状态
⑥如下图示能说明反应N2O4(g) 2NO2(g)达到平衡状态
2NO2(g)达到平衡状态
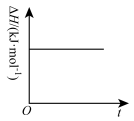
⑦反应SO2(g)+2CO(g) 2CO2(g)+S(l) ΔH<0在恒容的密闭容器中进行,平衡前,随着反应的进行,容器内压强始终不变
2CO2(g)+S(l) ΔH<0在恒容的密闭容器中进行,平衡前,随着反应的进行,容器内压强始终不变
⑧反应2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)ΔH<0在恒容密闭容器中进行,单位时间内消耗NO和N2的物质的量之比为1∶2时,反应达到平衡
2N2(g)+3H2O(g)ΔH<0在恒容密闭容器中进行,单位时间内消耗NO和N2的物质的量之比为1∶2时,反应达到平衡
⑨密闭容器中混合气体的密度不变,说明分解反应NH2COONH4(s) 2NH3(g)+CO2(g)已经达到化学平衡
2NH3(g)+CO2(g)已经达到化学平衡
⑩2v正(H2)=3v逆(NH3)能说明反应N2(g)+3H2(g) 2NH3(g)已达到平衡状态
2NH3(g)已达到平衡状态
⑪在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g) MHx+2y(s) ΔH<0达到化学平衡,容器内气体压强保持不变
MHx+2y(s) ΔH<0达到化学平衡,容器内气体压强保持不变
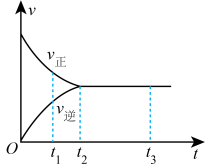
⑫由可逆反应X2+3Y2 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线可知,t1时,只有正方向反应
2Z在反应过程中的反应速率(v)与时间(t)的关系曲线可知,t1时,只有正方向反应
①可逆反应2NO2(g)
 2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO2,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO2,能说明该反应已达到平衡状态②可逆反应2NO2(g)
 2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,单位时间内生成n mol O2的同时生成2n mol NO,能说明该反应已达到平衡状态③可逆反应2NO2(g)
 2NO(g)+O2(g),在容积固定的密闭容器中,用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,用NO2、NO、O2表示的反应速率之比为2∶2∶1的状态,能说明该反应已达到平衡状态④可逆反应2NO2(g)
 2NO(g)+O2(g),在容积固定的密闭容器中,混合气体的颜色、密度、压强、平均相对分子质量不再改变,能说明该反应已达到平衡状态
2NO(g)+O2(g),在容积固定的密闭容器中,混合气体的颜色、密度、压强、平均相对分子质量不再改变,能说明该反应已达到平衡状态⑤一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g)
 C(g)+D(g),混合气体的密度、压强、总物质的量、B的物质的量浓度、混合气体的平均相对分子质量不再改变的状态,能表明该反应已达到平衡状态
C(g)+D(g),混合气体的密度、压强、总物质的量、B的物质的量浓度、混合气体的平均相对分子质量不再改变的状态,能表明该反应已达到平衡状态⑥如下图示能说明反应N2O4(g)
 2NO2(g)达到平衡状态
2NO2(g)达到平衡状态
⑦反应SO2(g)+2CO(g)
 2CO2(g)+S(l) ΔH<0在恒容的密闭容器中进行,平衡前,随着反应的进行,容器内压强始终不变
2CO2(g)+S(l) ΔH<0在恒容的密闭容器中进行,平衡前,随着反应的进行,容器内压强始终不变⑧反应2NH3(g)+NO(g)+NO2(g)
 2N2(g)+3H2O(g)ΔH<0在恒容密闭容器中进行,单位时间内消耗NO和N2的物质的量之比为1∶2时,反应达到平衡
2N2(g)+3H2O(g)ΔH<0在恒容密闭容器中进行,单位时间内消耗NO和N2的物质的量之比为1∶2时,反应达到平衡⑨密闭容器中混合气体的密度不变,说明分解反应NH2COONH4(s)
 2NH3(g)+CO2(g)已经达到化学平衡
2NH3(g)+CO2(g)已经达到化学平衡⑩2v正(H2)=3v逆(NH3)能说明反应N2(g)+3H2(g)
 2NH3(g)已达到平衡状态
2NH3(g)已达到平衡状态⑪在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
 MHx+2y(s) ΔH<0达到化学平衡,容器内气体压强保持不变
MHx+2y(s) ΔH<0达到化学平衡,容器内气体压强保持不变⑫由可逆反应X2+3Y2
 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线可知,t1时,只有正方向反应
2Z在反应过程中的反应速率(v)与时间(t)的关系曲线可知,t1时,只有正方向反应
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】一定温度下,在体积为0.5 L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2 (g)(红棕色)  N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
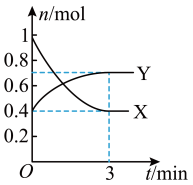
(1)曲线____ (填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3 min内,用NO2表示的反应速率为____________ 。
(3)下列叙述能说明该反应已达到化学平衡状态的是________ (填字母)。
a.容器内压强不再发生变化
b.NO2的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolN2O4的同时生成2nmol NO2
(4)反应达到平衡后,若降低温度,则v(正)______ ,v(逆)________ 。(填“增大”“减小”或“不变”)。
 N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
N2O4 (g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。
(1)曲线
(2)在0~3 min内,用NO2表示的反应速率为
(3)下列叙述能说明该反应已达到化学平衡状态的是
a.容器内压强不再发生变化
b.NO2的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolN2O4的同时生成2nmol NO2
(4)反应达到平衡后,若降低温度,则v(正)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】在一定温度下的某容积可变的密闭容器中,建立下列化学平衡: C(s)+H2O(g)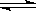 CO(g)+H2(g)试分析和回答下列问题:
CO(g)+H2(g)试分析和回答下列问题:
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是____ (选填序号)。
A 体系的压强不再发生变化
B v正(CO)=v逆(H2O)
C 生成n molCO的同时生成n mol H2
D 1mol H-H键断裂的同时断裂2mol H-O键
(2)若上述化学平衡状态从 正反应开始建立,达到平衡后,给平衡体系加压(缩小容积.其它条件不变。下同),则容器内气体的平均相对分子质量面将
正反应开始建立,达到平衡后,给平衡体系加压(缩小容积.其它条件不变。下同),则容器内气体的平均相对分子质量面将_____ (填写不变.变小.变大)
(3)若上述化学平衡状态从正.逆两反应同时建立[即起始时同时投放C(s).H2O(g).CO(g).H2(g)],达到平衡后,试讨论:
①容积内气体混合物的平均相对分子质量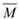 的取值范围是
的取值范围是_____________ 。
②若给平衡体系加压,请参照起始投放的气体物质的平均相对分子质量(设定为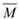 ),分别给出
),分别给出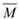 的变化(请填写条件和结论):
的变化(请填写条件和结论):______________ 、______________ 、______________ 。
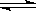 CO(g)+H2(g)试分析和回答下列问题:
CO(g)+H2(g)试分析和回答下列问题:(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是
A 体系的压强不再发生变化
B v正(CO)=v逆(H2O)
C 生成n molCO的同时生成n mol H2
D 1mol H-H键断裂的同时断裂2mol H-O键
(2)若上述化学平衡状态从
 正反应开始建立,达到平衡后,给平衡体系加压(缩小容积.其它条件不变。下同),则容器内气体的平均相对分子质量面将
正反应开始建立,达到平衡后,给平衡体系加压(缩小容积.其它条件不变。下同),则容器内气体的平均相对分子质量面将(3)若上述化学平衡状态从正.逆两反应同时建立[即起始时同时投放C(s).H2O(g).CO(g).H2(g)],达到平衡后,试讨论:
①容积内气体混合物的平均相对分子质量
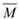 的取值范围是
的取值范围是②若给平衡体系加压,请参照起始投放的气体物质的平均相对分子质量(设定为
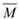 ),分别给出
),分别给出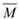 的变化(请填写条件和结论):
的变化(请填写条件和结论):
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】氢气是未来理想的能源。
(1)实验室用铁与 的硫酸反应生成
的硫酸反应生成 的物质的量与反应时间的关系如图所示。按要求回答下列问题:
的物质的量与反应时间的关系如图所示。按要求回答下列问题: 的平均反应速率最大的时间段是
的平均反应速率最大的时间段是_______ (填“0~2min”“2~4min”或“4~6min”),该时间段内对反应速率起关键作用的影响因素是_______ 。
②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是_______ 。
③要加快上述实验中产生氢气的速率,还可采取的措施是_______ (填一种)。
(2)工业上用海水制氢气的新技术的原理为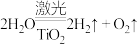 。回答下列问题:
。回答下列问题:
①分解海水的反应属于_______ 反应(填“放热”或“吸热”)。
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为
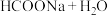 。下列说法正确的是
。下列说法正确的是_______ (填序号)。
A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键的断裂
C.储氢过程中, 被还原
被还原
D.释氢过程中,每消耗0.1mol 放出2.24L
放出2.24L
(3) 可与
可与 发生反应:
发生反应: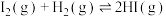 。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
(1)实验室用铁与
 的硫酸反应生成
的硫酸反应生成 的物质的量与反应时间的关系如图所示。按要求回答下列问题:
的物质的量与反应时间的关系如图所示。按要求回答下列问题: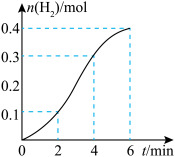
 的平均反应速率最大的时间段是
的平均反应速率最大的时间段是②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是
③要加快上述实验中产生氢气的速率,还可采取的措施是
(2)工业上用海水制氢气的新技术的原理为
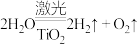 。回答下列问题:
。回答下列问题:①分解海水的反应属于
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为

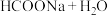 。下列说法正确的是
。下列说法正确的是A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键的断裂
C.储氢过程中,
 被还原
被还原D.释氢过程中,每消耗0.1mol
 放出2.24L
放出2.24L
(3)
 可与
可与 发生反应:
发生反应: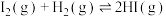 。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。
。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是_______(填序号)。A. |
| B.断裂1mol H―H键的同时形成1mol I―I键 |
| C.容器内气体的压强不变 |
| D.容器内气体的颜色不变 |
您最近一年使用:0次



