电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是____ (填序号),写出正极的电极反应式____ 。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为____ 。
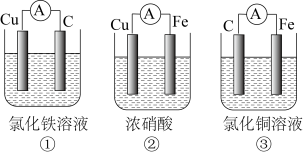
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
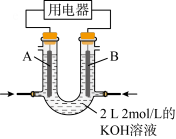
实验测得OH-向B电极定向移动,则___ (填“A”或“B”)处电极入口通甲烷,该电池正极的电极反应式为___ 当消耗甲烷的体积为33.6L(标准状况下)时,正极消耗氧气的物质的量为___ 。
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
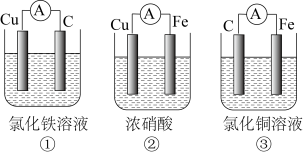
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH-向B电极定向移动,则
更新时间:2021-09-10 14:07:46
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O 的酸性废水通过铁炭混合物,在微电池正极上Cr2 O
的酸性废水通过铁炭混合物,在微电池正极上Cr2 O 转化为Cr3+,其电极反应式为
转化为Cr3+,其电极反应式为___________ 。
 的酸性废水通过铁炭混合物,在微电池正极上Cr2 O
的酸性废水通过铁炭混合物,在微电池正极上Cr2 O 转化为Cr3+,其电极反应式为
转化为Cr3+,其电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】研究去除水体中的 污染是环境保护的重要课题。
污染是环境保护的重要课题。
(1)一种活性炭载纳米铁粉吸附剂去除废水中 的可能反应机理如图1所示。图中“*”表示微粒处于吸附状态。
的可能反应机理如图1所示。图中“*”表示微粒处于吸附状态。

①相同条件下,将活性炭载纳米铁粉和纳米铁粉分别加入含 废水中,反应相同时间,采用活性炭载纳米铁粉去除
废水中,反应相同时间,采用活性炭载纳米铁粉去除 的效率更高,原因是
的效率更高,原因是_______ 。
②实验测得反应相同时间,初始pH对 去除率影响如图2所示。
去除率影响如图2所示。 时,pH越小,
时,pH越小, 去除率越低的原因是
去除率越低的原因是_______ 。
③图1所示反应机理可描述为_______ 。
(2)以石墨为阳极、铁为阴极电解含 废水可用于去除
废水可用于去除 。电解时各种含氮微粒的浓度、溶液的pH与时间的关系如图3所示。
。电解时各种含氮微粒的浓度、溶液的pH与时间的关系如图3所示。
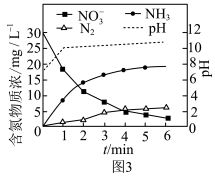
①0~1min时,阴极发生的主要电极反应方程式为_______ 。
②若向废水中加入一定量的 ,则电解后废水中的
,则电解后废水中的 几乎完全转化为
几乎完全转化为 ,原因是
,原因是_______ 。
 污染是环境保护的重要课题。
污染是环境保护的重要课题。(1)一种活性炭载纳米铁粉吸附剂去除废水中
 的可能反应机理如图1所示。图中“*”表示微粒处于吸附状态。
的可能反应机理如图1所示。图中“*”表示微粒处于吸附状态。
①相同条件下,将活性炭载纳米铁粉和纳米铁粉分别加入含
 废水中,反应相同时间,采用活性炭载纳米铁粉去除
废水中,反应相同时间,采用活性炭载纳米铁粉去除 的效率更高,原因是
的效率更高,原因是②实验测得反应相同时间,初始pH对
 去除率影响如图2所示。
去除率影响如图2所示。 时,pH越小,
时,pH越小, 去除率越低的原因是
去除率越低的原因是③图1所示反应机理可描述为
(2)以石墨为阳极、铁为阴极电解含
 废水可用于去除
废水可用于去除 。电解时各种含氮微粒的浓度、溶液的pH与时间的关系如图3所示。
。电解时各种含氮微粒的浓度、溶液的pH与时间的关系如图3所示。
①0~1min时,阴极发生的主要电极反应方程式为
②若向废水中加入一定量的
 ,则电解后废水中的
,则电解后废水中的 几乎完全转化为
几乎完全转化为 ,原因是
,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知:①将0.1 mol/LKI溶液加入到0.1 mol/LFeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;②当离子浓度相同时,氧化性:Ag+>Fe3+;③若浓度减小时,离子的氧化性也会随之减弱。
(1)甲同学猜测,0.1 mol/L KI溶液(事先加入几滴淀粉溶液)加入到0.1 mol/LAgNO3溶液中时,溶液变蓝色。请写出该猜测对应的离子方程式______ 。实验结果未见到蓝色。
(2)乙同学认为甲同学的实验方案有问题,理由是_______ 。请你用设计实验证明Ag+也能氧化I-,要求画出实验装置图,并标明电极材料及电解质溶液_______ 。
(1)甲同学猜测,0.1 mol/L KI溶液(事先加入几滴淀粉溶液)加入到0.1 mol/LAgNO3溶液中时,溶液变蓝色。请写出该猜测对应的离子方程式
(2)乙同学认为甲同学的实验方案有问题,理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按图所示,组装一种原电池装置。试回答下列问题(灯泡功率合适):
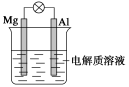
(1)电解质溶液为稀硫酸时,灯泡______ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题),回答下面问题________ 。
a.若灯泡亮,则Mg电极上发生的电极反应式、Al电极上发生的电极反应式分别为______。
b.若灯泡不亮,其理由为________。
(2)电解质溶液为NaOH(aq)时,灯泡_______ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题),回答下面问题________ 。
a.若灯泡亮,则Mg电极上发生___________(填“氧化”或“还原”)反应;Al电极作___________极。
b.若灯泡不亮,其理由为___________。

(1)电解质溶液为稀硫酸时,灯泡
a.若灯泡亮,则Mg电极上发生的电极反应式、Al电极上发生的电极反应式分别为______。
b.若灯泡不亮,其理由为________。
(2)电解质溶液为NaOH(aq)时,灯泡
a.若灯泡亮,则Mg电极上发生___________(填“氧化”或“还原”)反应;Al电极作___________极。
b.若灯泡不亮,其理由为___________。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在铜锌原电池中(如图)__ 极,电极上发生的是___ (填“氧化”或“还原”)反应。铜电极的电极反应式是___ ;原电池总反应的离子方程式为___ 。
(2)若锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气___ L(标准状况),导线中通过___ mol电子。
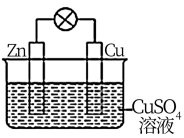
(2)若锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2023年6月9~11日,世界动力电池大会在宜宾举行,宜宾在电池研发、制造领域走在世界前列。利用原电池原理,人们研制出很多结构和性能各异的化学电池。
回答下列问题:
(1)某化学小组设计出如下图所示的甲、乙、丙三套装置。
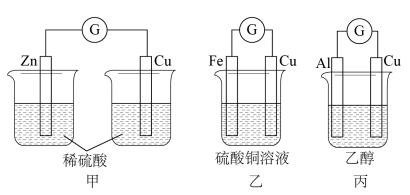
上图装置中,电流计指针会发生偏转的是___________ (填“甲”“乙”或“丙”),该装置中 电极的电极反应式为
电极的电极反应式为___________ 。
(2)铅酸蓄电池放电时发生反应: 。该电池的负极材料为
。该电池的负极材料为___________ ;该电池工作时,将___________ 能转化为___________ 能。
(3)氢氧燃料电池的简易装置如下图所示:
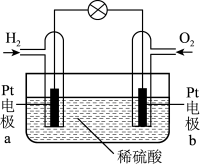
① 电极a上发生
电极a上发生___________ 反应(填“氧化”或“还原”)。
②室温下,若该电池每消耗1
 可提供电能114.4
可提供电能114.4 ,则该电池的有效能量转化率为
,则该电池的有效能量转化率为___________ 。(已知:室温下,1
 完全燃烧生成液态水时,释放286.0
完全燃烧生成液态水时,释放286.0 的能量)
的能量)
回答下列问题:
(1)某化学小组设计出如下图所示的甲、乙、丙三套装置。

上图装置中,电流计指针会发生偏转的是
 电极的电极反应式为
电极的电极反应式为(2)铅酸蓄电池放电时发生反应:
 。该电池的负极材料为
。该电池的负极材料为(3)氢氧燃料电池的简易装置如下图所示:

①
 电极a上发生
电极a上发生②室温下,若该电池每消耗1

 可提供电能114.4
可提供电能114.4 ,则该电池的有效能量转化率为
,则该电池的有效能量转化率为
 完全燃烧生成液态水时,释放286.0
完全燃烧生成液态水时,释放286.0 的能量)
的能量)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。
I.请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
(1)元素①在周期表中的位置为________ 。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为_________ (填化学式);
(3)元素①、③形成的18电子化合物的电子式为______ ;
(4)元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______ (填化学式);
(5)元素⑤、⑧的最高价氧化物对应的水化物的水溶液反应的离子方程式为_________ 。
II.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(6)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。铅蓄电池放电时正极是__ (填物质化学式)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到___ mol/L。
(7)甲醛(HCHO)燃料电池的工作原理如下图所示。
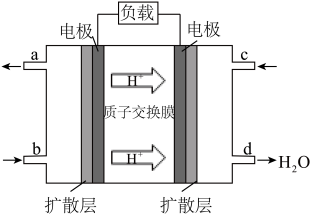
①该电池工作时,b口通入的物质为________ ;
②该电池工作时,电子的流向为___________ (填“从左到右”或“从右到左”);
③右侧电极的电极反应方程式为___________ 。
I.请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为
(3)元素①、③形成的18电子化合物的电子式为
(4)元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是
(5)元素⑤、⑧的最高价氧化物对应的水化物的水溶液反应的离子方程式为
II.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(6)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。铅蓄电池放电时正极是
(7)甲醛(HCHO)燃料电池的工作原理如下图所示。

①该电池工作时,b口通入的物质为
②该电池工作时,电子的流向为
③右侧电极的电极反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.填空。
(1)已知1g氢气完全燃烧生成液态水放出热量121.6kJ,则2mol氢气完全燃烧生成液态水放出的热量为_______ kJ。
II.下图是氢-氧燃料电池的示意图。则:
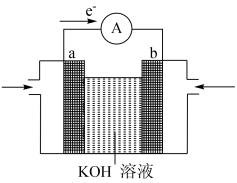
(2)溶液中K+移向_______ 电极(填“a”或“b”)。
(3)反应结束后溶液碱性_______ (填“增大”“减小”或“不变”)。
(4)b极通入气体为_______ ,a电极的反应式为_______ 。
(5)若把上述电解质溶液改为稀硫酸溶液,则正极的电极反应式为_______ 。
(1)已知1g氢气完全燃烧生成液态水放出热量121.6kJ,则2mol氢气完全燃烧生成液态水放出的热量为
II.下图是氢-氧燃料电池的示意图。则:

(2)溶液中K+移向
(3)反应结束后溶液碱性
(4)b极通入气体为
(5)若把上述电解质溶液改为稀硫酸溶液,则正极的电极反应式为
您最近一年使用:0次
【推荐3】(1)肼(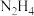 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为_____________________ 。
(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是_______ 填(“正”或“负”)极,写出该电池的负极反应式:_____________________ 。
(3)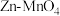 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是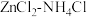 混合溶液。
混合溶液。
①该电池的负极材料是______ 。电池工作时,电子流向__________ 填(“正”或“负”)极。
②若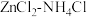 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是_______ 。
③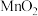 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的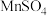 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是_____________________ 。若电路中通过4mol电子,标准状况下产生气体的物质的量为_________ 。
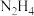 )-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为
)-空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为(2)科研人员新近开发一种由甲醇和氧气为燃料,强碱溶液作电解质溶液的新型手机电池,可供手机连续使用一个月。则通入甲醇的是
(3)
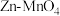 干电池应用广泛,电解质溶液是
干电池应用广泛,电解质溶液是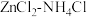 混合溶液。
混合溶液。①该电池的负极材料是
②若
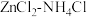 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速某电极的腐蚀,其主要原因是
,会加速某电极的腐蚀,其主要原因是③
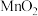 的生产方法之一是以石墨为电极,电解酸化的
的生产方法之一是以石墨为电极,电解酸化的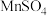 溶液。阳极的主要电极反应式是
溶液。阳极的主要电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在铜、锌原电池中,以稀硫酸为电解质溶液 如图
如图 ,则此原电池中锌电极上发生的是
,则此原电池中锌电极上发生的是_______ 反应 “氧化”或“还原”
“氧化”或“还原”  ,电极反应式为
,电极反应式为_______ ;铜为_______ 极,电极反应式是_______ ;若电路中有 电子通过时,负极质量会变化
电子通过时,负极质量会变化_______ 克;在内电路中, 向
向_______ 极定向移动。

 如图
如图 ,则此原电池中锌电极上发生的是
,则此原电池中锌电极上发生的是 “氧化”或“还原”
“氧化”或“还原”  ,电极反应式为
,电极反应式为 电子通过时,负极质量会变化
电子通过时,负极质量会变化 向
向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200 ℃左右供电。电池总反应为C2H5OH+3O2=2CO2+3H2O,如图是该电池的示意图,回答以下问题
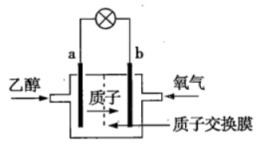
(1)该电池的正极为_________ (“a”或“b”),
(2)电池正极的电极反应为______________________________ ;负极的电极反应为_______________________________ 。
(3)电池工作时,1 mol乙醇被氧化时,有________ mol电子转移;
(4)电池工作一段时间后,a极附近溶液的pH________ (“增大”或“减小”)

(1)该电池的正极为
(2)电池正极的电极反应为
(3)电池工作时,1 mol乙醇被氧化时,有
(4)电池工作一段时间后,a极附近溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
(1)已知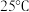 、
、 时,32g甲烷燃烧生成
时,32g甲烷燃烧生成 和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为
和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为___________ 。
Ⅱ.反应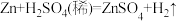 的能量变化如图所示。
的能量变化如图所示。___________ (填“吸热”或“放热”)反应。
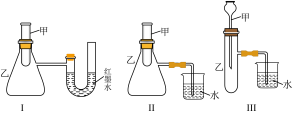
(3)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是___________ (填序号)
(5)请写出该电池的正极反应式___________
(6)若有1mol电子流过导线,则理论上在标准状况下,产生 的体积为
的体积为___________ L
(7)将稀 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是___________ (填“锌极”或“铜极”)。
(1)已知
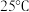 、
、 时,32g甲烷燃烧生成
时,32g甲烷燃烧生成 和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为
和液态水时放出1780.6kJ热量,则该条件下反应的热化学方程式为Ⅱ.反应
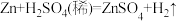 的能量变化如图所示。
的能量变化如图所示。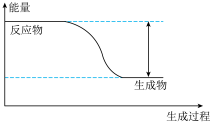
(3)如图三个装置中,不能证明“锌与稀硫酸反应是吸热反应还是放热反应”的是
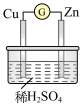
A.Cu极有 产生 产生 | B.锌作负极,发生还原反应 |
C. 向Zn极移动 向Zn极移动 | D.电子由Zn经导线流向Cu |
(6)若有1mol电子流过导线,则理论上在标准状况下,产生
 的体积为
的体积为(7)将稀
 换成
换成 溶液,电极质量增加的是
溶液,电极质量增加的是
您最近一年使用:0次



