书写下列方程式
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(2)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式___________ 。
(3)I2在KOH溶液中反应,产物之一是KIO3,该过程的离子反应方程式为___________ 。
(4)在碱性条件下,Cl2可将废水中的CN—氧化为无毒的CO2、N2,该过程的离子反应方程式为___________ 。
(5)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为___________ 。
(1)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式
(3)I2在KOH溶液中反应,产物之一是KIO3,该过程的离子反应方程式为
(4)在碱性条件下,Cl2可将废水中的CN—氧化为无毒的CO2、N2,该过程的离子反应方程式为
(5)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
更新时间:2021-09-14 09:05:16
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应在生产生活中有广泛的应用,回答下列问题。
(1)实验室中常用浓盐酸和二氧化猛混合加热制备氯气,下列反应中盐酸所体现的性质与该反应相同的是________
a.Zn+2HCl=ZnCl2+H2↑
b.KClO3+6HCl=KCl+3Cl2↑+3H2O
c.2HCl H2↑+Cl2↑
H2↑+Cl2↑
d.2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
(2)向硫酸酸化的高锰酸钾溶液中滴加H2O2溶液,高锰酸钾溶液褪色并有气泡冒出,该反应中氧化剂与还原剂的物质的量之比为______ ,若生成标准状况下3.36 L气体时转移的电子数为________ 。
(3)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________ 。
(1)实验室中常用浓盐酸和二氧化猛混合加热制备氯气,下列反应中盐酸所体现的性质与该反应相同的是
a.Zn+2HCl=ZnCl2+H2↑
b.KClO3+6HCl=KCl+3Cl2↑+3H2O
c.2HCl
 H2↑+Cl2↑
H2↑+Cl2↑d.2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
(2)向硫酸酸化的高锰酸钾溶液中滴加H2O2溶液,高锰酸钾溶液褪色并有气泡冒出,该反应中氧化剂与还原剂的物质的量之比为
(3)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化合物X是产量大、应用广的二元化合物,大量用作漂白剂、饮水处理剂、消毒剂等。年产量达300万吨的氯酸钠是生产X的原料,92%用于生产X-在酸性水溶液中用盐酸、二氧化硫或草酸还原。此外,将亚氯酸钠固体装柱,通入用空气稀释的氯气氧化,也可生产X。X有极性和顺磁性,不形成二聚体,在碱性溶液里可发生歧化反应。
(1)写出X的分子式__________ 和共轭π键( 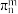 )
)___________
(2)分别写出上述用草酸还原和用氯气氧化生产X的反应方程式___________
(3)写出上述X歧化反应的化学方程式___________
(1)写出X的分子式
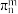 )
)(2)分别写出上述用草酸还原和用氯气氧化生产X的反应方程式
(3)写出上述X歧化反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质集合M中含有常见物质Na2O2、NaHCO3、Al、SO2、Fe、NH3、Na、Cl2,这些物质按照以下方法进行分类后如图所示,其中A组为单质,B组为化合物,请按照要求回答问题。
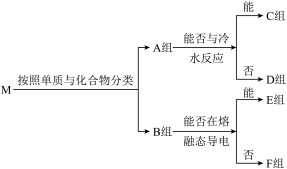
(1)该分类方法为_______ ,
(2)B组物质中属于非电解质的为_______ ,其中能作制冷剂的物质的电子式为_______ 。
(3)C组物质中有的能与水剧烈反应,该反应中氧化剂和还原剂物质的量之比为_______ 。
(4)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:_______ 。
(5)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:_______ 。
(6)在密闭容器中,将E组中的混合物加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为_______ ;

(1)该分类方法为
(2)B组物质中属于非电解质的为
(3)C组物质中有的能与水剧烈反应,该反应中氧化剂和还原剂物质的量之比为
(4)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:
(5)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:
(6)在密闭容器中,将E组中的混合物加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为
您最近一年使用:0次



