X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期?(填“是”或“否”)_______ ,理由是_______ ;
(2)Y是_______ ,Z是_______ ,W是_______ 。(填元素符号)
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1.写出该化合物的名称及化学式_______ 。
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期?(填“是”或“否”)
(2)Y是
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1.写出该化合物的名称及化学式
20-21高一·全国·课时练习 查看更多[1]
(已下线)人教必修第一册第4章第1节第2课时元素周期表(课后)
更新时间:2021-09-17 18:49:54
|
相似题推荐
【推荐1】根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】X是第四周期中未成对电子数最多的元素
(1)X是___________ (填元素符号)。
(2)它位于___________ 族,属于___________ 区。
(3)它的核外电子排布式是___________ ,价层电子的轨道表示式___________ 。
(4)它有___________ 个能层,___________ 个能级。
(5)价层电子排布式的特点是___________ 。
(1)X是
(2)它位于
(3)它的核外电子排布式是
(4)它有
(5)价层电子排布式的特点是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D为短周期元素,请根据下表信息回答问题。
(1)B在元素周期表的位置:___ ;B气态氢化物的电子式___ 。
(2)C的最高价氧化物分别与强酸、强碱反应的离子方程式为___ 、___ 。
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
(2)C的最高价氧化物分别与强酸、强碱反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】有三种物质AC2、B2C2、AD4,元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子的电子层结构与氩原子的相同,则:
(1)A、B、C、D的元素名称分别为_______ 、_______ 、_______ 、_______ 。
(2)AD4分子中含有的共价键类型为_____________ (填“σ键”或“π键”)。
(3)D的负一价阴离子的电子排布式为_______________ ,B2C2的电子式为__________ ,属______ (填“离子化合物”或“共价化合物”)。
(1)A、B、C、D的元素名称分别为
(2)AD4分子中含有的共价键类型为
(3)D的负一价阴离子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:________ (填具体元素符号,下同),原子结构示意图为________ 。元素⑩名称为________ 在周期表中的位置________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是________ ,碱性最强的化合物的电子式是:________ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:________________ ,该化合物属于________ (填“共价”或“离子”)化合物。
(4)表示①与⑦的化合物的电子式________ ,该化合物是由________ (填”极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是______________ 。
(6)元素③的氢化物的结构式为________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为_________________________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(6)元素③的氢化物的结构式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某元素的原子序数为29,试问:
(1)此元素原子的电子总数是_________ 个。
(2)它有________ 个电子层,有__________ 个能级。
(3)它的外围电子排布式是_______________ 。
(4)它属于第___________ 周期第_________ 族。
(5)它有________ 个未成对电子。
(1)此元素原子的电子总数是
(2)它有
(3)它的外围电子排布式是
(4)它属于第
(5)它有
您最近一年使用:0次
填空题
|
较易
(0.85)
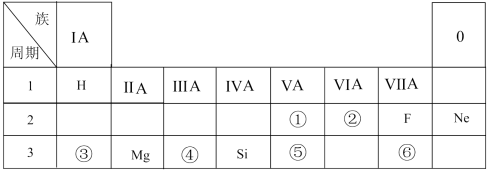
【推荐3】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:
(1)②表示的元素是______ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是______ (填元素符号),其非金属性较强的是 ______ (填元素符号),其最高正价氧化物水化物酸性较强的酸是 ______ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______ (填化学式)。③与⑥两种元素所形成化合物的电子式是 ______ 。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:______ 。
(1)②表示的元素是
(2)①与⑤两种元素相比较,原子半径较大的是
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次

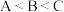 ,且都小于18,A元素的原子最外层电子数是次外层电子数的2倍;B元素的原子核外M层电子数是L层电子数的一半;C元素的原子次外层电子数比最外层电子数多1。回答下列问题:
,且都小于18,A元素的原子最外层电子数是次外层电子数的2倍;B元素的原子核外M层电子数是L层电子数的一半;C元素的原子次外层电子数比最外层电子数多1。回答下列问题:

