根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
更新时间:2022-09-15 21:00:58
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】甲元素原子的L电子层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
(1)甲的元素符号是____________ ;其轨道表示式为____________ 。
(2)乙元素原子的最外层电子排布式为____________ ,其在元素周期表中的位置是____________ 。
(3)甲属于____________ 区元素,乙属于____________ 区元素。
(1)甲的元素符号是
(2)乙元素原子的最外层电子排布式为
(3)甲属于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】今年为“国际化学元素周期表年”,元素周期表揭示了化学元素间的内在联系。
(1)图为氟元素在元素周期表中的部分信息和氟原子及镁原子的结构示意图。
写出图中①代表的元素符号_________ ,镁属于_________ (填“金属”或“非金属”)元素。
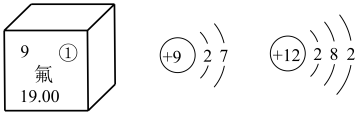
(2)由氟和镁两种元素组成化合物氟化镁的化学式为__________________
(3)A、B、C原子结构示意图中,与镁原子的化学性质最相似的是_________ (填序号)。
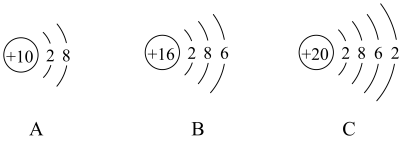
(4)已知原子的核外电子层数与元素所在周期表中周期的序数相同,则镁元素在元素周期表中排在第_______ 周期。
(1)图为氟元素在元素周期表中的部分信息和氟原子及镁原子的结构示意图。
写出图中①代表的元素符号

(2)由氟和镁两种元素组成化合物氟化镁的化学式为
(3)A、B、C原子结构示意图中,与镁原子的化学性质最相似的是

(4)已知原子的核外电子层数与元素所在周期表中周期的序数相同,则镁元素在元素周期表中排在第
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
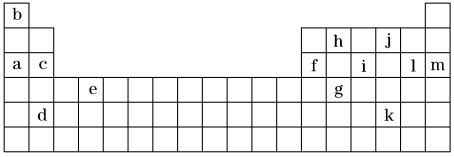
(1)下列___________ (填序号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k
③c、h、l ④d、e、f
(2)如给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:a.原子核对核外电子的吸引力,b.形成稳定结构的倾向。下表是一些气态电中性基态,原子失去核外不同电子所需的能量(kJ·mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:___________ 。
②表中X可能为以上13种元素中的___________ (填字母)元素,则该元素属于___________ 区。用元素符号表示X和j所能形成的化合物的化学式是___________ 。
③Y是周期表中第___________ 族元素。
④以上13种元素中,___________ (填字母)元素原子失去核外第一个电子需要的能量最多。

(1)下列
①a、c、h ②b、g、k
③c、h、l ④d、e、f
(2)如给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:a.原子核对核外电子的吸引力,b.形成稳定结构的倾向。下表是一些气态电中性基态,原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | — | 9 550 | 11 600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:
②表中X可能为以上13种元素中的
③Y是周期表中第
④以上13种元素中,
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】 是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
1.基态Mn原子的价电子轨道表示式为___________ ;其核外有___________ 种不同能量的电子。
2.氯酸钾熔融状态下的电离方程式为___________ ;双氧水的电子式为___________ 。
 是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。1.基态Mn原子的价电子轨道表示式为
2.氯酸钾熔融状态下的电离方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在___________ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是___________ 。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】合成氨有助于解决地球上粮食不足问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)我国科研人员研制出了“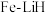 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。
①第三电离能
_______ 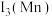 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
②比较 与
与 的半径大小关系:
的半径大小关系: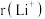
_______  (填“>”或“<”)。
(填“>”或“<”)。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将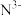 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
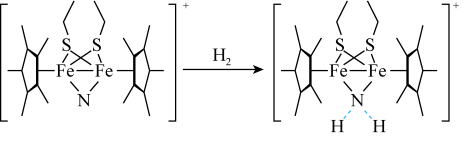
产物中 原于的杂化轨道类型为
原于的杂化轨道类型为_______ 。
(1)基态N原子中,能量最高的电子的电子云在空间有
(2)我国科研人员研制出了“
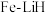 ”催化剂,使得合成氨温度和压强分别降到了350℃,
”催化剂,使得合成氨温度和压强分别降到了350℃, ,这是近年来合成氨反应研究中心的重要突破。
,这是近年来合成氨反应研究中心的重要突破。①第三电离能

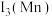 (填“>”或“<”),原因是
(填“>”或“<”),原因是②比较
 与
与 的半径大小关系:
的半径大小关系: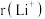
 (填“>”或“<”)。
(填“>”或“<”)。(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将
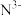 转化为NH2,反应过程如图所示:
转化为NH2,反应过程如图所示:
产物中
 原于的杂化轨道类型为
原于的杂化轨道类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D代表4种元素。请填空:
(1)A原子序数为24的元素原子中有___________ 个电子层,___________ 个能级,___________ 个未成对电子,位于元素周期表的___________ 区。
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:___________ 。
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为___________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应的化学方程式:___________ 。
(1)A原子序数为24的元素原子中有
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题
(1)基态二价铜离子的核外电子排布式为__________ 。已知高温下 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:__________________________ 。
(2)镍的基态原子的价电子的电子排布图(轨道表示式)为_____________________ 。
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为__________ ,铬原子的价电子排布式为____________________________ 。
(4)钴元素的常见价态为 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:________________ 。
(5)基态钒原子的价层电子排布式是________________ 。
(6)Mn的价电子排布式为____________ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用____________ 理论解释。
(1)基态二价铜离子的核外电子排布式为
 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:(2)镍的基态原子的价电子的电子排布图(轨道表示式)为
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态
 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为(4)钴元素的常见价态为
 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:(5)基态钒原子的价层电子排布式是
(6)Mn的价电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求回答下列各小题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,Fe成为阳离子时首先失去___________ 轨道电子。
(2)基态S原子电子占据最高能级的电子云轮廓图为___________ 形,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为___________ 。
(3)Zn原子核外电子排布式为___________ 。
(4)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
(5)Co基态原子核外电子排布式为___________ 。
(6)基态Ge原子的核外电子排布式为[Ar]___________ ,有___________ 个未成对电子。
(7)镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(8)写出基态As原子的核外电子排布式___________ 。
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)Zn原子核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
(5)Co基态原子核外电子排布式为
(6)基态Ge原子的核外电子排布式为[Ar]
(7)镍元素基态原子的电子排布式为
(8)写出基态As原子的核外电子排布式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1) 基态核外电子排布式为
基态核外电子排布式为________ 。
(2) 的空间构型为
的空间构型为________ (用文字描述); 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为________ (填元素符号)。
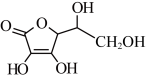
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为________ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(1)
 基态核外电子排布式为
基态核外电子排布式为(2)
 的空间构型为
的空间构型为 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用NH4Cl溶液浸出氧化锌矿石的过程中主要涉及反应2ZnO+4 +4Cl-=[Zn(NH3)4]2++ZnCl
+4Cl-=[Zn(NH3)4]2++ZnCl +2H2O。与
+2H2O。与 互为等电子体的阴离子为
互为等电子体的阴离子为___________ (写离子符号,写一种即可)。[Zn(NH3)4]2+的结构示意图为___________ 。
 +4Cl-=[Zn(NH3)4]2++ZnCl
+4Cl-=[Zn(NH3)4]2++ZnCl +2H2O。与
+2H2O。与 互为等电子体的阴离子为
互为等电子体的阴离子为
您最近一年使用:0次

 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。 中的配位键
中的配位键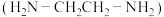 形成配离子:
形成配离子: