Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu2O。
(1) 基态核外电子排布式为
基态核外电子排布式为________ 。
(2) 的空间构型为
的空间构型为________ (用文字描述); 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为________ (填元素符号)。
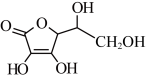
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为________ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(1)
 基态核外电子排布式为
基态核外电子排布式为(2)
 的空间构型为
的空间构型为 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为
更新时间:2024-04-16 11:28:59
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】有以下物质:①HF、②Cl2、③H2O、④N2、⑤C2H4、⑥C2H6、⑦H2、⑧H2O2和⑨HCN。
(1)只含有σ键的是___________ (填序号,下同);
(2)既含有σ键又含有π键的是__________ 。
(3)含有由两个原子的s轨道重叠形成σ键的是____________ 。
(4)写出以下分子或离子的空间构型:NH3:________ ,H2O:________ , SO2:________ ,BeCl2:________ ,CO2:_________ 。
(1)只含有σ键的是
(2)既含有σ键又含有π键的是
(3)含有由两个原子的s轨道重叠形成σ键的是
(4)写出以下分子或离子的空间构型:NH3:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】完成下列问题。
(1) 是有机合成中常用的还原剂。
是有机合成中常用的还原剂。 中,存在_______(填标号)。
中,存在_______(填标号)。
(2)气态三氧化硫以单分子形式存在,其中按轨道重叠方式分类共价键的类型有_______ 种。
(3)等电子体的结构相似、物理性质相近,称为等电子原理。如 和CO为等电子体。试回答:
和CO为等电子体。试回答:
①写出下面物质分子或离子的立体构型:

_______ ,
_______ 。
②由第二周期元素组成,与 互为等电子体的离子有
互为等电子体的离子有_______ 。
③ 的立体构型如图1所示,请再按照图1的表示方法在图2中表示
的立体构型如图1所示,请再按照图1的表示方法在图2中表示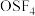 分子中O、S、F原子的空间位置
分子中O、S、F原子的空间位置_______ 。已知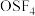 分子中O、S间为共价双键,S、F间为共价单键。(已知三键斥力>双键斥力>单键斥力)
分子中O、S间为共价双键,S、F间为共价单键。(已知三键斥力>双键斥力>单键斥力)
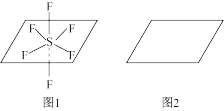
(4)氨气在水中的溶解度远大于甲烷,原因是_______ (答出三条)。
(1)
 是有机合成中常用的还原剂。
是有机合成中常用的还原剂。 中,存在_______(填标号)。
中,存在_______(填标号)。| A.离子键 | B.σ键 | C.π键 | D.氢键 |
(3)等电子体的结构相似、物理性质相近,称为等电子原理。如
 和CO为等电子体。试回答:
和CO为等电子体。试回答:①写出下面物质分子或离子的立体构型:


②由第二周期元素组成,与
 互为等电子体的离子有
互为等电子体的离子有③
 的立体构型如图1所示,请再按照图1的表示方法在图2中表示
的立体构型如图1所示,请再按照图1的表示方法在图2中表示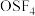 分子中O、S、F原子的空间位置
分子中O、S、F原子的空间位置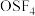 分子中O、S间为共价双键,S、F间为共价单键。(已知三键斥力>双键斥力>单键斥力)
分子中O、S间为共价双键,S、F间为共价单键。(已知三键斥力>双键斥力>单键斥力)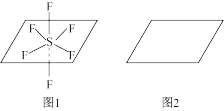
(4)氨气在水中的溶解度远大于甲烷,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】有A、B、C、D四种主族元素,原子序数依次增大,A元素原子 轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入
轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入 轨道后,
轨道后, 轨道为全充满状态。请回答下列问题:
轨道为全充满状态。请回答下列问题:
(1) 分子中含有
分子中含有______ 个π键,属于______ (填“极性”或“非极性”)分子。
(2)B的简单氢化物的空间结构为______ ,B原子采用______ 杂化。
(3)C元素的电负性______ (填“>”“<”或“=”)D元素的电负性,用一个化学方程式表示:______ 。
 轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入
轨道上有2个未成对电子。B元素原子的p轨道中有3个未成对电子,其简单氢化物在水中的溶解度在同族元素所形成的简单氢化物中最大。C的最高化合价和最低化合价的代数和为4,其最高价氧化物中含C的质量分数为40%,且其核内质子数等于中子数。D元素原子得一个电子填入 轨道后,
轨道后, 轨道为全充满状态。请回答下列问题:
轨道为全充满状态。请回答下列问题:(1)
 分子中含有
分子中含有(2)B的简单氢化物的空间结构为
(3)C元素的电负性
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】FeTiO3的结构如图所示,其中由O围成的__ (填“四面体空隙”或“八面体空隙”)被Fe占据,Ti的配位数为__ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
(1)请写出h元素的价电子排布图_____________________ ;
(2)ya3分子的电子式是_______ ,其分子的空间构型是_______ ,分子中y原子的杂化轨道类型是_________ , g2+可以与ya3以________ 键形成 [g (ya3)4]2+离子;
(3)请写出上述元素d3+的核外电子排布式____________________ ,实验室常用形成一种红色配离子的方法检验该离子,该反应的离子方程式为_______________________________________________ 。
(4)请比较b、e、j三种元素的第一电离能由大到小的顺序_____________ (写元素符号),其原因是_____________________________________________
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | [ | d | g | l | ||||||||||||
| [ | |||||||||||||||||
(2)ya3分子的电子式是
(3)请写出上述元素d3+的核外电子排布式
(4)请比较b、e、j三种元素的第一电离能由大到小的顺序
您最近一年使用:0次



