A、B、C、D代表4种元素。请填空:
(1)A原子序数为24的元素原子中有___________ 个电子层,___________ 个能级,___________ 个未成对电子,位于元素周期表的___________ 区。
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:___________ 。
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为___________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应的化学方程式:___________ 。
(1)A原子序数为24的元素原子中有
(2)B原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子的价电子排布图:
(3)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D元素基态原子的电子排布式为
更新时间:2024-01-11 18:48:03
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)某基态原子的价层电子的轨道表示式为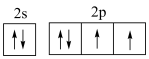
①s电子的电子云轮廓图是______________ 形
②有______________ 种空间运动状态不同的电子
③最外层有______________ 个电子
④有______________ 种能量不同的电子
(2)四种元素基态原子的电子排布式如下:①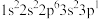 ;②
;② ;③
;③ ;④
;④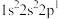
①第一电离能:①______________ ②(填“>”、“=”或“<”)
②电负性:③______________ ④(填“>”、“=”或“<”)
(1)某基态原子的价层电子的轨道表示式为

①s电子的电子云轮廓图是
②有
③最外层有
④有
(2)四种元素基态原子的电子排布式如下:①
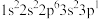 ;②
;② ;③
;③ ;④
;④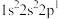
①第一电离能:①
②电负性:③
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】硅原子核外电子运动状态为___________ 种;基态Si原子,若其电子排布式表示为 违背了
违背了___________ 。
 违背了
违背了
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业制玻璃主要原料有石英、纯碱和石灰石.在玻璃窑中发生主要反应的化学方程式为:Na2CO3+SiO2 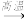 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2 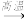 CaSiO3+CO2↑
CaSiO3+CO2↑
(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为________ ,则原料中SiO2、Na2CO3、CaCO3的物质的量之比为_________________________ 。
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式___________________ ,有_____________ 种不同类型的晶体(填数字)
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径___________ (填“大”或“小”),该元素与铝元素两者的最高价氧化物的水化物之间发生反应的离子方程式为__________________________ 。
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有________ 种不同运动状态的电子、________ 种不同能级的电子。
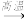 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2 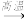 CaSiO3+CO2↑
CaSiO3+CO2↑(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是_______ 。
a.最易失去的电子能量最高
b.同一个电子层上的不同能级上的原子轨道,能量大小不同
c.p轨道电子能量一定高于s轨道电子能量
d.在离核最近区域内运动的电子能量最低
(2)比较下列多电子原子的原子轨道的能量高低。
①1s,3d:_______ ;②3s,3p,3d:_______ ;③2p,3p,4p:_______ ;④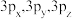 :
:_______ 。
(3)基态铝原子核外电子云有_______ 种不同的伸展方向,共有_______ 种不同能级的电子,有_______ 种不同运动状态的电子。
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是
a.最易失去的电子能量最高
b.同一个电子层上的不同能级上的原子轨道,能量大小不同
c.p轨道电子能量一定高于s轨道电子能量
d.在离核最近区域内运动的电子能量最低
(2)比较下列多电子原子的原子轨道的能量高低。
①1s,3d:
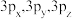 :
:(3)基态铝原子核外电子云有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知元素周期表中共有18个纵行,下图实线表示元素周期表的边界。按核外电子排布,可把元素周期表里的元素划分为 区、
区、 区、
区、 区、
区、 区等。除
区等。除 区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
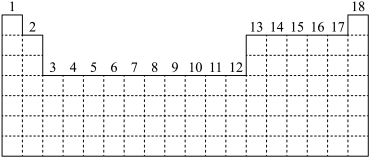
(1)请在上图中用实线画出 区、
区、 区、
区、 区、
区、 区的边界线,并分别用阴影
区的边界线,并分别用阴影 和
和 表示
表示 区和
区和 区
区________ 。
(2)有的同学受这种划分的启发,认为 区内第6、7纵行的部分元素可以排在另一区,你认为应排在
区内第6、7纵行的部分元素可以排在另一区,你认为应排在______ 区。
(3)请在上述元素周期表中用元素符号标出 轨道处于半充满状态的元素
轨道处于半充满状态的元素________ 。
 区、
区、 区、
区、 区、
区、 区等。除
区等。除 区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
(1)请在上图中用实线画出
 区、
区、 区、
区、 区、
区、 区的边界线,并分别用阴影
区的边界线,并分别用阴影 和
和 表示
表示 区和
区和 区
区(2)有的同学受这种划分的启发,认为
 区内第6、7纵行的部分元素可以排在另一区,你认为应排在
区内第6、7纵行的部分元素可以排在另一区,你认为应排在(3)请在上述元素周期表中用元素符号标出
 轨道处于半充满状态的元素
轨道处于半充满状态的元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)M电子层上有_______ 个能级,有_______ 个轨道。
(2)A元素的最高正化合价是+4价,A原子次外层上有2个电子,A原子的电子排布式是_______ 。
(3)B元素在气态氢化物中显-3价,气态氢化物极易溶于水,B原子的电子排布式是_______ 。
(4)E原子核外占有9个轨道,且只有1个未成对电子,E离子结构示意图是_______ 。
(5)F、G都是短周期元素,F2-与G3+的电子层结构相同,则F2-的电子排布式是_______ ,G元素的原子序数是_______ 。
(2)A元素的最高正化合价是+4价,A原子次外层上有2个电子,A原子的电子排布式是
(3)B元素在气态氢化物中显-3价,气态氢化物极易溶于水,B原子的电子排布式是
(4)E原子核外占有9个轨道,且只有1个未成对电子,E离子结构示意图是
(5)F、G都是短周期元素,F2-与G3+的电子层结构相同,则F2-的电子排布式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钛很多重要的化合物,如TiO2、TiCl4、[Ti(OH)2(H2O)4]Cl2。图1为TiO2催化下,O3降解CH3CHO的示意图。回答下列问题:
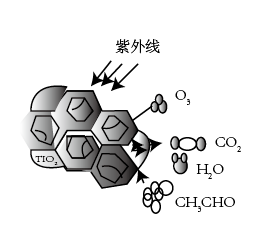
图1
(1)写出Ti元素在周期表中的位置___________ ,价电子排布式___________
(2)图1中反应方程式___________
(3)1molCH3CHO中含有的σ键的数目为___________ (设阿伏加德罗常数的值为NA)
(4)乙醛的沸点___________ (填“高于”或“低于”)乙醇的沸点,原因是___________ 。
(5)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如图2所示。

①基态Cl原子的核外电子占据的最高能级的电子云轮廓图为___________ 形。
②M中不含___________ (填代号)。
a.π键 b.离子键 c.σ键 d.非极性键

图1
(1)写出Ti元素在周期表中的位置
(2)图1中反应方程式
(3)1molCH3CHO中含有的σ键的数目为
(4)乙醛的沸点
(5)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如图2所示。

①基态Cl原子的核外电子占据的最高能级的电子云轮廓图为
②M中不含
a.π键 b.离子键 c.σ键 d.非极性键
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y。W 原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为 l: 1,Z原子核外电子中p电子数比Y原子多2个。
(1)X元素的单质与Z、Y 所形成的化合物反应,其化学方程式_______ 。
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为_____<_____(用分子式表示)。_________
(3) 这四种元素原子半径的大小为_______>_______ >_______ >_______ (填元素符号)。_____
(1)X元素的单质与Z、Y 所形成的化合物反应,其化学方程式
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为_____<_____(用分子式表示)。
(3) 这四种元素原子半径的大小为_______>_______ >_______ >_______ (填元素符号)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某元素的原子序数为29,试问:
(1)此元素原子的电子总数是_________ 个。
(2)它有________ 个电子层,有__________ 个能级。
(3)它的外围电子排布式是_______________ 。
(4)它属于第___________ 周期第_________ 族。
(5)它有________ 个未成对电子。
(1)此元素原子的电子总数是
(2)它有
(3)它的外围电子排布式是
(4)它属于第
(5)它有
您最近一年使用:0次
【推荐2】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的______ 区,其价电子排布式为_____ 。与Ti同周期的过渡元素中,未成对电子数最多的基态原子的外围电子的轨道表示式______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是______ 。
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次



