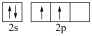
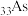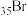X是第四周期中未成对电子数最多的元素
(1)X是___________ (填元素符号)。
(2)它位于___________ 族,属于___________ 区。
(3)它的核外电子排布式是___________ ,价层电子的轨道表示式___________ 。
(4)它有___________ 个能层,___________ 个能级。
(5)价层电子排布式的特点是___________ 。
(1)X是
(2)它位于
(3)它的核外电子排布式是
(4)它有
(5)价层电子排布式的特点是
更新时间:2021-12-03 09:07:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】香花石是1958年中国地质学家发现的第一种世界新矿物,其主要成分的化学式为Ca3Li2(BeSiO4)3F2。回答下列问题:
(1)质子数与中子数相等的Ca原子的符号为________ 。
(2)Si在元素周期表的位置为________ 。
(3)香花石的主要成分的组成元素中,原子半径最小的是________ (填元素符号),原子半径最大的是________ (填元素符号)。
(1)质子数与中子数相等的Ca原子的符号为
(2)Si在元素周期表的位置为
(3)香花石的主要成分的组成元素中,原子半径最小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知元素周期表中共有18纵行。如图所示实线表示元周期表的边界,按电子排布,可把元素周期表划分为s区、p区、d区、ds等,除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
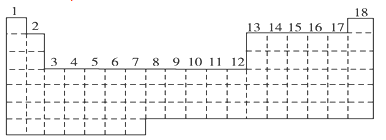
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区_____ 。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)_____ 。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:___________ 。
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:
(1)M元素原子的核外电子排布式为_______ 。
(2)M元素在元素周期表中的位置为_______ 。
(3)M的基态原子共有_______ 种不同能级的电子,该原子最外层电子数为_______ ,价层电子数为_______ 。
(4)某元素原子的基态电子排布式为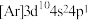 ,该元素处于元素周期表的第
,该元素处于元素周期表的第_______ 周期第_______ 族。试推测该元素处于元素周期表的_______ 区,该元素原子的价电子排布图为_______ 。
(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式_______ 。
 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:(1)M元素原子的核外电子排布式为
(2)M元素在元素周期表中的位置为
(3)M的基态原子共有
(4)某元素原子的基态电子排布式为
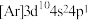 ,该元素处于元素周期表的第
,该元素处于元素周期表的第(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式
您最近一年使用:0次
【推荐1】N、P两种元素位于元素周期表第VA族。请回答下列问题:
(1)基态氮原子的电子排布式为________ ;基态氮原子的价层电子的轨道表示式为________ 。
(2)基态磷原子中,其占据的最高能层的符号是________ ;基态磷原子占据的最高能级共有________ 个原子轨道,其形状是________ 。
(3)电负性:N________ P(填>或<)。
(4)雷酸汞曾被用作起爆药,雷酸汞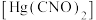 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为________ >________ >________ (填元素符号)。
(1)基态氮原子的电子排布式为
(2)基态磷原子中,其占据的最高能层的符号是
(3)电负性:N
(4)雷酸汞曾被用作起爆药,雷酸汞
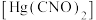 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在化学实验和科学研究中,水是一种常用的试剂。
(1)水分子中的氧原子在基态时的价电子排布式为:___________ 。
(2)水分子在特定条件下容易得到一个H+而形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是___________ 。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)在冰晶体中,每个水分子与相邻的4个水分子形成___________ 键,水分子间还存在___________ ,1mol H2O中含___________ mol氢键。
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位离子。请写出生成此配位离子的离子方程式:___________ 。
(1)水分子中的氧原子在基态时的价电子排布式为:
(2)水分子在特定条件下容易得到一个H+而形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)在冰晶体中,每个水分子与相邻的4个水分子形成
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位离子。请写出生成此配位离子的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】[Zn(CN)4]2–在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2–+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________ 。
(2)1 mol HCHO分子中含有σ键的数目为_________ mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是________ 。
(4)与H2O分子互为等电子体的阴离子为________ 。
(1)Zn2+基态核外电子排布式为
(2)1 mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化类型是
(4)与H2O分子互为等电子体的阴离子为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)元素Cu基态原子的价电子排布式为 ___________ ,价电子排布图为___________ 。
(2)基态Mg原子中,电子占据的最高能层符号为___________ ,占据该能层电子的电子云轮廓图形状为___________ 、核外电子的运动状态为___________ 种。
(3)N、O、F三种元素第一电离能由大到小顺序为___________ (用元素符号表示)
(2)基态Mg原子中,电子占据的最高能层符号为
(3)N、O、F三种元素第一电离能由大到小顺序为
您最近一年使用:0次
【推荐2】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B的基态原子中能量最高的电子,其电子云在空间有___ 个方向,原子轨道呈____ 形。
(2)某同学根据上述信息,推断C基态原子的核外电子排布图为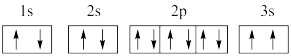 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____________________ 。
(3)G位于______ 族______ 区。
(4)检验F元素的实验方法是_________________ 。
(5)BA3中心原子杂化轨道类型为___________ ;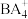 VSEPR模型为
VSEPR模型为___________ ;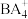 空间结构为
空间结构为_______________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1个 |
| C元素原子的第一至第四电离能分别是: I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)B的基态原子中能量最高的电子,其电子云在空间有
(2)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)G位于
(4)检验F元素的实验方法是
(5)BA3中心原子杂化轨道类型为
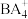 VSEPR模型为
VSEPR模型为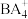 空间结构为
空间结构为
您最近一年使用:0次
【推荐1】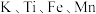 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钾在火焰上灼烧的紫光是一种_______ (填“吸收”或“发射”)光谱。
(2) 原子位于元素周期表中的
原子位于元素周期表中的_______ 区,基态 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为_______ 形,其价电子排布式为_______ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为_______ 。
(3)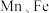 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第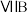 族。比较两元素的
族。比较两元素的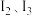 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是_______ 。
(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(5) 与
与 的半径大小关系为
的半径大小关系为
_______ (填“大于”或“小于”) 。
。
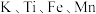 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:(1)钾在火焰上灼烧的紫光是一种
(2)
 原子位于元素周期表中的
原子位于元素周期表中的 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为(3)
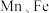 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:| 元素 |  |  | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
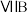 族。比较两元素的
族。比较两元素的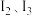 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(5)
 与
与 的半径大小关系为
的半径大小关系为
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为____________________ 。Fe与N相比,第一电离能较大的是_______________ 。
(2)丙酮( )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为_______________ 和_______________ 。
(3)C、N、O三种元素形成的氢化物沸点从高到低的顺序为:_____________ ,原因是________________ 。
(4)1molN2分子中含有σ键____________ mol,含π键______________ mol。
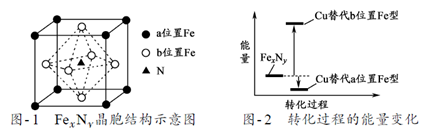
(5)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为___________ 。
(1)Fe3+基态核外电子排布式为
(2)丙酮(
 )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为(3)C、N、O三种元素形成的氢化物沸点从高到低的顺序为:
(4)1molN2分子中含有σ键
(5)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次

 :
: