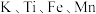 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:(1)钾在火焰上灼烧的紫光是一种
(2)
 原子位于元素周期表中的
原子位于元素周期表中的 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为(3)
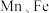 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:| 元素 |  |  | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
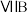 族。比较两元素的
族。比较两元素的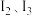 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(5)
 与
与 的半径大小关系为
的半径大小关系为
 。
。
更新时间:2024-02-13 10:27:08
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室加热液体时常加入沸石,其主要成分为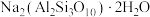 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:
(1)元素Si在周期表中的位置是_______ 。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式);Na与同周期非金属性最强的元素形成的化合物可做调味品,用电子式表示该化合物的形成过程_______ 。
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是_______ (填化学式)。
(4)Na所在周期的主族元素中,简单离子半径最小的是_______ (填离子符号)
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
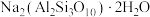 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:(1)元素Si在周期表中的位置是
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是
(4)Na所在周期的主族元素中,简单离子半径最小的是
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y。W 原子的最外层没有p电子,X原子核外s电子与p电子数之比为1:1,Y原子最外层s电子与p电子数之比为 l: 1,Z原子核外电子中p电子数比Y原子多2个。
(1)X元素的单质与Z、Y 所形成的化合物反应,其化学方程式_______ 。
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为_____<_____(用分子式表示)。_________
(3) 这四种元素原子半径的大小为_______>_______ >_______ >_______ (填元素符号)。_____
(1)X元素的单质与Z、Y 所形成的化合物反应,其化学方程式
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为_____<_____(用分子式表示)。
(3) 这四种元素原子半径的大小为_______>_______ >_______ >_______ (填元素符号)。
您最近一年使用:0次
【推荐3】锶(Sr)位于元素周期表的第5周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。
完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是___________ ,非金属性最强的是___________ ;
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式___________ ,该分子为___________ (选填“极性”、“非极性”)分子。
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号___________ ;写出锶原子的最外层电子排布式__________ 。
(4)下列关于锶及其化合物的叙述中,错误的是________ 。
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
(4)下列关于锶及其化合物的叙述中,错误的是
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列微粒的电子排布式和外围电子排布式:
(1)Fe___________ 、___________ 。
(2)Fe2+___________ 、___________ 。
(3)As___________ 、___________ 。
(4)Cu2+___________ 、___________ 。
(1)Fe
(2)Fe2+
(3)As
(4)Cu2+
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】PM2.5中的某些物质,易引发光化学烟雾污染,光化学烟雾中含有NOx、OCS、CH2=CH-CHO、HCOOH、以及光气等二次污染物。水污染程度可通过测定水体中铅、铬等重金属的含量判断。
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______ (用元素符号表示),CH2=CH-CHO分子醛基中碳原子杂化方式为____________ 。
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_________ ;光气(COCl2)各原子最外层都满足8电子稳定结构,则光气分子的空间构型为_________ (用文字描述);
(3)1molHCOOH中含σ键和π键数目之比为______________ 。
(4)基态Cr原子核外电子排布式是_______ ,配合物[Cr(NH3)4(H2O)2] Cl3中心离子的配体为_______ 。
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=______ (填数字)。若两个相邻面心的Kr原子的核间距为acm,用NA表示阿伏伽德罗常数,M表示Kr的相对原子质量。该晶体的密度计算式为______ g/cm3。
(1)C、N、O三种元素的第一电离能从大到小的顺序为
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
(3)1molHCOOH中含σ键和π键数目之比为
(4)基态Cr原子核外电子排布式是
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】铜元素的化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)CuSO4和Cu(NO3)2是自然界中重要的铜盐。
① CuSO4和Cu(NO3)2中阳离子的基态外围电子排布式为_______________ 。
② S、O、N三种元素的第一电离能由大到小为_____________ 。
③ CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是________ 。
(2)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:

① 配合物A中N原子的轨道杂化类型为__________ 。
② 1 mol配合物A含有σ键的数目为_____________ 。
(3)CuFeS2的晶胞如图1所示,CuFeS2的晶胞中每个Cu原子与__ 个S原子相连

(1)CuSO4和Cu(NO3)2是自然界中重要的铜盐。
① CuSO4和Cu(NO3)2中阳离子的基态外围电子排布式为
② S、O、N三种元素的第一电离能由大到小为
③ CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是
(2)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:

① 配合物A中N原子的轨道杂化类型为
② 1 mol配合物A含有σ键的数目为
(3)CuFeS2的晶胞如图1所示,CuFeS2的晶胞中每个Cu原子与

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)日光等白光经棱镜折射后产生的是___________ 光谱。原子光谱是___________ 光谱。
(2)吸收光谱是___________ 的电子跃迁为___________ 的电子产生的,此过程中电子___________ 能量;发射光谱是___________ 的电子跃迁为___________ 的电子产生的,此过程中电子___________ 能量。
(3)1861年德国人基尔霍夫(G.R Kirchhoff)和本生(R.W.Bunsen)研究锂云母的某谱时,发现在深红区有一新线从而发现了铷元素他们研究的是___________ 。
(4)含有钾元素的盐的焰色试验为___________ 色。许多金属盐都可以发生焰色试验其原因是___________ 。
(1)日光等白光经棱镜折射后产生的是
(2)吸收光谱是
(3)1861年德国人基尔霍夫(G.R Kirchhoff)和本生(R.W.Bunsen)研究锂云母的某谱时,发现在深红区有一新线从而发现了铷元素他们研究的是
(4)含有钾元素的盐的焰色试验为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】光谱分析
通过原子发射光谱或吸收光谱___________ 元素,称为光谱分析。
通过原子发射光谱或吸收光谱
您最近一年使用:0次
【推荐3】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的______ 区,其价电子排布式为_____ 。与Ti同周期的过渡元素中,未成对电子数最多的基态原子的外围电子的轨道表示式______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是______ 。
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
【推荐1】X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)Y2分子中存在的σ键和π键个数之比为___________ 。
(2)X—H键和Y—H键属于极性共价键,其中极性较强的是___________ (X、Y用元素符号表示)键。X的第一电离能比Y的___________ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:___________ 。
(4)W的基态原子的价电子排布式为___________ 。
(5)已知一种Y4分子结构如图所示:断裂1molY—Y键吸收167kJ的热量,生成1molY≡Y放出942kJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式:___________ 。

(1)Y2分子中存在的σ键和π键个数之比为
(2)X—H键和Y—H键属于极性共价键,其中极性较强的是
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:
(4)W的基态原子的价电子排布式为
(5)已知一种Y4分子结构如图所示:断裂1molY—Y键吸收167kJ的热量,生成1molY≡Y放出942kJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式:

您最近一年使用:0次
【推荐2】完成下列填空
(1)写出下列基态原子的核外电子排布式。
Li:___________ ;N:___________ ;Ti:___________ ;Cu___________ 。
(2)钒元素在元素周期表中的位置是___________ 。
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是___________ 。
(1)写出下列基态原子的核外电子排布式。
Li:
(2)钒元素在元素周期表中的位置是
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】由《物质结构与性质》第一、二章的知识回答下列问题:
(1)互为同分异构的两种物质分别为,a: 对羟基苯甲醛( ); b:邻羟基苯甲醛(
); b:邻羟基苯甲醛( ),则一般易形成分子间氢键的是
),则一般易形成分子间氢键的是___________ (填“a”或“b”),其沸点明显___________ (填“高于”或“低于”)另一同分异构体。
(2)已知Ti的第二电离能:I2(Ti)=1310 kJ·mol-1,K的第二电离能I2(K)=3051 kJ·mol-1,I2(Ti)≪I2(K),其原因为___________ 。
(3)Ni与Ca处于同一周期,且原子核外最外层电子数相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为___________ 。
(4)有下列物质:①HCHO ②O2 ③(NH4)2S ④P4 ⑤H2O2 ⑥MgSO4 ⑦CO2 ⑧C2H4,按要求填写相对应序号。
i.既含有极性键又含有非极性键的分子是___________ 。
ii.含极性键的离子化合物的是___________ 。
iii.①HCHO、⑤H2O2、⑦CO2 三种分子中,键角由大到小的顺序___________ 。
(1)互为同分异构的两种物质分别为,a: 对羟基苯甲醛(
 ); b:邻羟基苯甲醛(
); b:邻羟基苯甲醛( ),则一般易形成分子间氢键的是
),则一般易形成分子间氢键的是(2)已知Ti的第二电离能:I2(Ti)=1310 kJ·mol-1,K的第二电离能I2(K)=3051 kJ·mol-1,I2(Ti)≪I2(K),其原因为
(3)Ni与Ca处于同一周期,且原子核外最外层电子数相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(4)有下列物质:①HCHO ②O2 ③(NH4)2S ④P4 ⑤H2O2 ⑥MgSO4 ⑦CO2 ⑧C2H4,按要求填写相对应序号。
i.既含有极性键又含有非极性键的分子是
ii.含极性键的离子化合物的是
iii.①HCHO、⑤H2O2、⑦CO2 三种分子中,键角由大到小的顺序
您最近一年使用:0次



