已知 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:
(1)M元素原子的核外电子排布式为_______ 。
(2)M元素在元素周期表中的位置为_______ 。
(3)M的基态原子共有_______ 种不同能级的电子,该原子最外层电子数为_______ ,价层电子数为_______ 。
(4)某元素原子的基态电子排布式为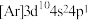 ,该元素处于元素周期表的第
,该元素处于元素周期表的第_______ 周期第_______ 族。试推测该元素处于元素周期表的_______ 区,该元素原子的价电子排布图为_______ 。
(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式_______ 。
 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:(1)M元素原子的核外电子排布式为
(2)M元素在元素周期表中的位置为
(3)M的基态原子共有
(4)某元素原子的基态电子排布式为
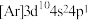 ,该元素处于元素周期表的第
,该元素处于元素周期表的第(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式
更新时间:2023-03-08 20:00:31
|
相似题推荐
【推荐1】1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于____ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素的中文名称,分别为“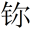 (nǐ)”“镆(mò)”“
(nǐ)”“镆(mò)”“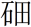 (tián)”“
(tián)”“ (ào)”,则下列说法正确的是
(ào)”,则下列说法正确的是___ (填字母序号)。
a.115号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___ ,该元素M能层上具有____ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___ F(填“>”“<”或“=”),理由是___ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素的中文名称,分别为“
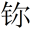 (nǐ)”“镆(mò)”“
(nǐ)”“镆(mò)”“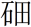 (tián)”“
(tián)”“ (ào)”,则下列说法正确的是
(ào)”,则下列说法正确的是a.115号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有人推测尚未合成的第114号元素有相当稳定的同位素,恰处在不稳定核素的“海洋”中浮起的一群较稳定核素的“岛屿”的中心。114号元素是第_______ 周期第_______ 族元素,它的可能氧化态_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】结合元素周期表,用化学用语回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。_______

(2)表中所列元素,属于短周期元素的有____ ,属于主族元素的有___ 种;i元素位于第_____ 周期第______ 族。
(3)元素f是第____ 周期____ 族元素,请在如图方框中按氮元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。______
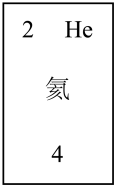
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是_______ (填标号)。
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。

(2)表中所列元素,属于短周期元素的有
(3)元素f是第

(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
您最近一年使用:0次
【推荐1】在下列空格中,填上适当的元素符号。
(1)在第3周期中,第一电离能最小的元素是_______ ,第一电离能最大的元素是_______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_______ 。
(3)在第4周期元素中,原子的4p轨道半充满的是_______ ,3d轨道半充满的_______ ,4s轨道半充满的是_______ ,外围电子中s电子数与d电子数相同的是_______ 。
(1)在第3周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)在第4周期元素中,原子的4p轨道半充满的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在1~18号元素中,符合下列要求的元素为(填写元素符号)
(1)原子L层上有3个电子的元素:_______
(2)原子M层电子数为L层电子数一半的元素:_______
(3)原子K层与M层上的电子数之和等于L层上的电子数的元素:_______
(4)原子最外层电子数为其内层电子数总和一半的元素:_______
(5)原子最外层电子数等于其电子层数的元素:_______
(6)次外层电子数为最外层电子数 的元素:
的元素:_______
(7)最外层只有1个电子的元素:_______
(8)原子最外层电子数是次外层电子数的2倍的元素:_______
(9)原子次外层电子数是最外层电子数的2倍的元素:____
(10)原子的K层和M层电子数相同的元素:_______
(1)原子L层上有3个电子的元素:
(2)原子M层电子数为L层电子数一半的元素:
(3)原子K层与M层上的电子数之和等于L层上的电子数的元素:
(4)原子最外层电子数为其内层电子数总和一半的元素:
(5)原子最外层电子数等于其电子层数的元素:
(6)次外层电子数为最外层电子数
 的元素:
的元素:(7)最外层只有1个电子的元素:
(8)原子最外层电子数是次外层电子数的2倍的元素:
(9)原子次外层电子数是最外层电子数的2倍的元素:
(10)原子的K层和M层电子数相同的元素:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)以基态硅原子为例,如果电子排布式写作ls22s22p63s13p3则违反了_______ 原理,如写作ls22s22p63s33p1则违反了_______ 原理;
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为_______ 、_______ ;
(3)在我们现今使用的元素周期表中,元素种类最多的族是_______ 族,共_______ 种元素;元素种类最多的周期是第_______ 周期,共_______ 种元素;
(4)熔点: F2_______ Cl2(填“<”或“=”“或>”,下同),沸点:HF_______ HCl,一定压强下HF和HCl的混合气体降温时_______ (填HF或HCl)先液化;
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:_______ (用元素符号按原子序数由小到大排列)。
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为
(3)在我们现今使用的元素周期表中,元素种类最多的族是
(4)熔点: F2
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)CH2=CH—C≡N分子中含有 ______ 个σ键,______ 个π键。
(2)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素名称是______ 。
(2)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素名称是
您最近一年使用:0次
【推荐2】按要求回答下列问题:
(1)研究发现,在 低压合成甲醇反应(
低压合成甲醇反应(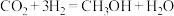 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为_______ 。在上述反应中,非金属元素的电负性最大的是_______ ,在周期表中Mn属于_______ 区元素。
(2)我国科学家成功合成了世界上首个五氮阴离子盐 。
。
①氮原子的价电子轨道表示式为_______ 。
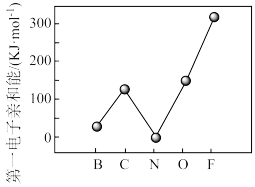
②元素的基态气志原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的变化趋势
)。第二周期部分元素的变化趋势 如图所示。氮元素的(
如图所示。氮元素的( )呈现异常的原因是
)呈现异常的原因是_______ 。
(3)已知As元素的相关信息如图所示,下列说法不正确的是_______。

(1)研究发现,在
 低压合成甲醇反应(
低压合成甲醇反应(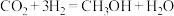 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为(2)我国科学家成功合成了世界上首个五氮阴离子盐
 。
。①氮原子的价电子轨道表示式为
②元素的基态气志原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的变化趋势
)。第二周期部分元素的变化趋势 如图所示。氮元素的(
如图所示。氮元素的( )呈现异常的原因是
)呈现异常的原因是
(3)已知As元素的相关信息如图所示,下列说法不正确的是_______。

| A.推测As能形成多种氧化物 |
B.热稳定性: 、 、 、HCl逐渐增强 、HCl逐渐增强 |
C.As的一种核素表示为, 中子数为40 中子数为40 |
| D.原子半径由大到小的顺序:As、Cl、Si |
您最近一年使用:0次
【推荐1】磷酸亚铁锂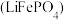 和锰酸锂
和锰酸锂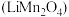 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性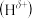 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性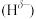 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: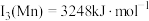 ,
,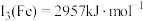 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
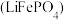 和锰酸锂
和锰酸锂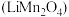 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性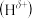 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性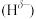 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
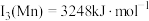 ,
,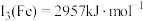 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近一年使用:0次
【推荐2】按要求回答下列问题:
(1)研究发现,在 低压合成甲醇反应(
低压合成甲醇反应(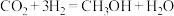 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为_______ 。在上述反应中,非金属元素的电负性最大的是_______ ,在周期表中Mn属于_______ 区元素。
(2)我国科学家成功合成了世界上首个五氮阴离子盐 。
。
①氮原子的价电子轨道表示式为_______ 。
②元素的基态气志原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的变化趋势
)。第二周期部分元素的变化趋势 如图所示。氮元素的(
如图所示。氮元素的( )呈现异常的原因是
)呈现异常的原因是_______ 。

(3)已知As元素的相关信息如图所示,下列说法不正确的是_______。

(1)研究发现,在
 低压合成甲醇反应(
低压合成甲醇反应(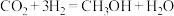 )中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为
)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布式为(2)我国科学家成功合成了世界上首个五氮阴离子盐
 。
。①氮原子的价电子轨道表示式为
②元素的基态气志原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的变化趋势
)。第二周期部分元素的变化趋势 如图所示。氮元素的(
如图所示。氮元素的( )呈现异常的原因是
)呈现异常的原因是
(3)已知As元素的相关信息如图所示,下列说法不正确的是_______。

| A.推测As能形成多种氧化物 |
B.热稳定性: 、 、 、HCl逐渐增强 、HCl逐渐增强 |
C.As的一种核素表示为, 中子数为40 中子数为40 |
| D.原子半径由大到小的顺序:As、Cl、Si |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:___________ ;B、N、H的电负性由大到小的顺序为___________ 。
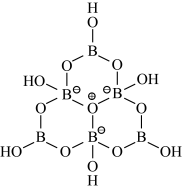
(2)科学家合成了一种含硼阴离子 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为___________ ,该结构中共有___________ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子___________ (填离子符号); 空间构型为
空间构型为___________ 。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子 空间构型为
空间构型为
您最近一年使用:0次

 环加成反应,
环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题: 核外电子排布式为
核外电子排布式为

