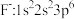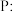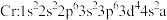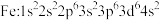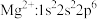点击化学的代表反应为铜催化的叠氨-炔基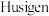 环加成反应,
环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:
(1)基态 核外电子排布式为
核外电子排布式为_______ ;基态O原子未成对电子有_______ 个。
(2)F、O、N、C的第一电离能从小到大的顺序是_______ 。
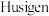 环加成反应,
环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:(1)基态
 核外电子排布式为
核外电子排布式为(2)F、O、N、C的第一电离能从小到大的顺序是
2023高三·全国·专题练习 查看更多[1]
(已下线)第四部分 物质结构与性质 热点1 原子结构与性质
更新时间:2023-03-15 13:00:58
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下图是s轨道、p轨道的原子轨道图,试回答下列问题:
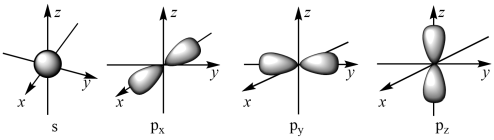
s能级的原子轨道呈______ 形,每个s能级有______ 个原子轨道;p能级的原子轨道呈______ 形,每个p能级有______ 个原子轨道。

s能级的原子轨道呈
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(2) 基态铝原子核外共有___________ 种不同能级的电子,有___________ 种不同运动状态的电子。
(2) 基态铝原子核外共有
您最近一年使用:0次
【推荐3】根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题。
(1)R原子的3p轨道上只有一个电子,则R原子是_______ ;Y原子的核电荷数为33,其电子排布式是_______ ,外围电子排布式是_______ 。
(2)写出Si、Ca2+、Cl-的电子排布式:
①Si:_______ ;
②Ca2+:_______ ;
③Cl-:_______ 。
(1)R原子的3p轨道上只有一个电子,则R原子是
(2)写出Si、Ca2+、Cl-的电子排布式:
①Si:
②Ca2+:
③Cl-:
您最近一年使用:0次
【推荐2】根据有关知识,回答下列问题。
(1)符号 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。
(2)铝原子核外电子云有__________ 种不同的伸展方向,有__________ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是__________ (填元素符号,下同),电负性最大的元素是__________ 。
(4)Be的第一电离能大于B的第一电离能,这是因为__________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:__________ 。
(6)锰元素位于第四周期第ⅦB族,请写出基础 的价层电子排布式
的价层电子排布式__________ 。
(1)符号
 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C. 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)锰元素位于第四周期第ⅦB族,请写出基础
 的价层电子排布式
的价层电子排布式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铁、铝、铜、硫、氮、磷、砷都是日常生活中常见的元素,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)Cu+的基态价电子排布图_______ ;Cu(NH3)4SO4中N、S、O三种元素的第一电离能由大到小的顺序为_______ (元素符号表示)。
(2)SO 中心原子的杂化方式为
中心原子的杂化方式为_______ ,SO 的立体构型为
的立体构型为_______ 。
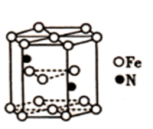
(3)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为_______ 。
(1)Cu+的基态价电子排布图
(2)SO
 中心原子的杂化方式为
中心原子的杂化方式为 的立体构型为
的立体构型为(3)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】N、O、S的第一电离能(I1)大小为(I1N)>(I1O)>(I1S),原因是______________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】丁二酮肟可用于镍的检验和测定,其结构式如图:
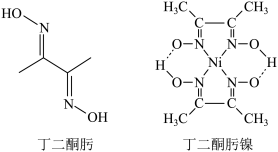
(1)Ni元素基态原子电子排布式为____ ,价电子排布图为:____ ,其中未成对电子数为:____ 。C、N、O第一电离能由大到小的顺序是____ 。
(2)1mol丁二酮肟含有的σ键数目是____ ,已知CN-与N2互为等电子体。推算HCN分子中σ和π键数目之比为:____ 。
(3)与氮原子同族的P的氢化物,它的空间立体构型是:____ ,它是含有____ 键的____ 分子。
(4)CO 的杂化方式是:
的杂化方式是:____ ,它的空间构型是:____ 。
(5)丁二酮肟镍分子内含有的作用力有____ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力

(1)Ni元素基态原子电子排布式为
(2)1mol丁二酮肟含有的σ键数目是
(3)与氮原子同族的P的氢化物,它的空间立体构型是:
(4)CO
 的杂化方式是:
的杂化方式是:(5)丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
您最近一年使用:0次