在下列空格中,填上适当的元素符号。
(1)在第3周期中,第一电离能最小的元素是_______ ,第一电离能最大的元素是_______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_______ 。
(3)在第4周期元素中,原子的4p轨道半充满的是_______ ,3d轨道半充满的_______ ,4s轨道半充满的是_______ ,外围电子中s电子数与d电子数相同的是_______ 。
(1)在第3周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)在第4周期元素中,原子的4p轨道半充满的是
20-21高二·全国·课时练习 查看更多[3]
更新时间:2022-11-25 11:44:37
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】电子排布的轨道表示式(电子排布图)
8O的轨道表示式如图:
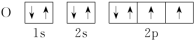
例:根据上面回答下列问题:
(1)简并轨道:_______ 相同的原子轨道。
(2)电子对:同一个原子轨道中,自旋方向_______ 的一对电子。
(3)单电子:_______ 轨道中若只有一个电子,则该电子称为单电子。
(4)自旋平行:_______ 的单电子称为自旋平行。
(5)在氧原子中,有_______ 对电子对,有_______ 个单电子。
(6)在氧原子中,有_______ 种空间运动状态,有_______ 种运动状态不同的电子。
8O的轨道表示式如图:

例:根据上面回答下列问题:
(1)简并轨道:
(2)电子对:同一个原子轨道中,自旋方向
(3)单电子:
(4)自旋平行:
(5)在氧原子中,有
(6)在氧原子中,有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)以基态硅原子为例,如果电子排布式写作ls22s22p63s13p3则违反了_______ 原理,如写作ls22s22p63s33p1则违反了_______ 原理;
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为_______ 、_______ ;
(3)在我们现今使用的元素周期表中,元素种类最多的族是_______ 族,共_______ 种元素;元素种类最多的周期是第_______ 周期,共_______ 种元素;
(4)熔点: F2_______ Cl2(填“<”或“=”“或>”,下同),沸点:HF_______ HCl,一定压强下HF和HCl的混合气体降温时_______ (填HF或HCl)先液化;
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:_______ (用元素符号按原子序数由小到大排列)。
(2)已知H、C、Si三种元素的电负性依次为2.1、2.5、1.8,则CH4、SiH4中C、Si的化合价依次为
(3)在我们现今使用的元素周期表中,元素种类最多的族是
(4)熔点: F2
(5)前三周期元素中,基态原子中未成对电子数与其所在周期序数相同的元素:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据如表所示:
(1)Mn元素原子的电子排布式为___________ 。比较两元素的I2、I3可知:气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是___________ 。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是___________ 。
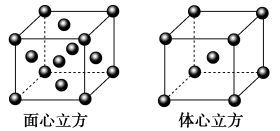
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为___________ 。
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1) 中配体分子
中配体分子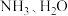 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。
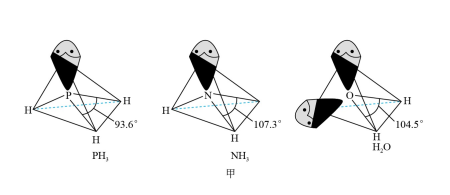
 中P的杂化类型是
中P的杂化类型是________ 。 的沸点比
的沸点比 的
的________ ,原因是________ 。 的键角小于
的键角小于 的,分析原因:
的,分析原因:________ 。
(2)磷酸根离子的空间构型为________ ,其中P的价层电子对数为________ 、杂化轨道类型为________ 。
(3) 分子中氮原子的轨道杂化类型是
分子中氮原子的轨道杂化类型是________ ;C、N、O元素的第一电离能由大到小的顺序为________ 。
(4)乙二胺 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是________ 、________ 。
(5) 中,电负性最高的元素是
中,电负性最高的元素是________ ;P的________ 杂化轨道与O的2p轨道形成________ 键。
(6) 的空间构型为
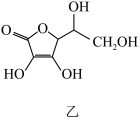
的空间构型为________ (用文字描述);抗坏血酸的分子结构如图乙所示,分子中碳原子的轨道杂化类型为________ ;推测抗坏血酸在水中的溶解性:________ (填“难溶于水”或“易溶于水”)。
(1)
 中配体分子
中配体分子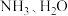 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。
 中P的杂化类型是
中P的杂化类型是 的沸点比
的沸点比 的
的 的键角小于
的键角小于 的,分析原因:
的,分析原因:(2)磷酸根离子的空间构型为
(3)
 分子中氮原子的轨道杂化类型是
分子中氮原子的轨道杂化类型是(4)乙二胺
 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是(5)
 中,电负性最高的元素是
中,电负性最高的元素是(6)
 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】翡翠的主要成分为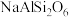 ,还含有其他多种金属阳离子,其中
,还含有其他多种金属阳离子,其中 的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
(1)基态 最外电子层的电子排布图(轨道表示式)为
最外电子层的电子排布图(轨道表示式)为___________ 。
(2)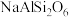 所含元素中,第一电离能最小的是
所含元素中,第一电离能最小的是___________ (填元素符号,下同);电负性最大的是___________ 。
(3)配合物 中的配体是
中的配体是___________ , 的沸点比
的沸点比 的高了许多,主要原因是
的高了许多,主要原因是___________
(4)已知某 的结构如图所示。
的结构如图所示。


___________ ,粒子内部的键角
___________  (填“>”“ <”或“=”)。
(填“>”“ <”或“=”)。
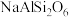 ,还含有其他多种金属阳离子,其中
,还含有其他多种金属阳离子,其中 的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一(1)基态
 最外电子层的电子排布图(轨道表示式)为
最外电子层的电子排布图(轨道表示式)为(2)
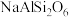 所含元素中,第一电离能最小的是
所含元素中,第一电离能最小的是(3)配合物
 中的配体是
中的配体是 的沸点比
的沸点比 的高了许多,主要原因是
的高了许多,主要原因是(4)已知某
 的结构如图所示。
的结构如图所示。


 (填“>”“ <”或“=”)。
(填“>”“ <”或“=”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大。C是周期表中电负性最大的元素。基态E原子的核外电子有7种空间运动状态。基态F原子有3个未成对电子。按要求回答下列问题:
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式___________ 。
(2)基态原子第一电离能大小介于E和F之间的元素有___________ 。(用元素符号表示)
(3)氨硼烷(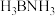 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为___________ (用元素符号表示)。
(4)磷酸盐在微生物作用下可转化为 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为___________ 。
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式
(2)基态原子第一电离能大小介于E和F之间的元素有
(3)氨硼烷(
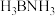 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为(4)磷酸盐在微生物作用下可转化为
 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p的原子结构示意图为___________________ 。
(2)o、p两元素的部分电离能数据如下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_________________________________________________________ 。
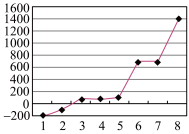
(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是___________________ (填图1中的序号)。
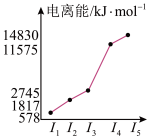
(4)表中所列的某主族元素的电离能情况如图所示,则该元素是___________________ (填元素符号)。
(5)基态钒原子的价电子排布图为___________________ 。
(6)写出单电子数最多的原子的电子排布式:__________________________________________ 。
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
(1)元素p的原子结构示意图为
(2)o、p两元素的部分电离能数据如下表:
元素 元素电离能/  | o | p |
| 717 | 759 |
| 1509 | 1561 |
| 3248 | 2957 |
比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图所示,则该元素是

(5)基态钒原子的价电子排布图为
(6)写出单电子数最多的原子的电子排布式:
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
A.[Ne]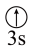 | B.[Ne]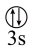 | C.[Ne]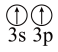 | D.[Ne]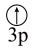 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Zn2+、三乙撑二胺和对苯二甲酸根离子可形成晶体M,其晶胞示意图如图。
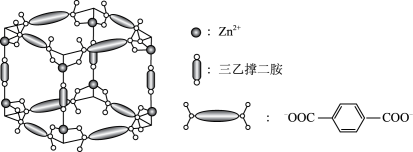
(1)Zn2+的价层电子排布式是_____ 。
(2)C、N、O的电负性从大到小 的顺序是_____ ;C、N、O的第一电离能从大到小 的顺序是_____ 。
(3)三乙撑二胺(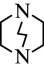 )与
)与 能形成配位键的原因是
能形成配位键的原因是_____ 。
(4)下列事实可用“水分子间存在氢键”解释的是_____ (填字母序号 )。
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(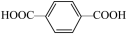 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为_____ ,羧基上碳原子的杂化方式为____ ,对苯二甲酸中最多有_____ 个原子共平面。

(1)Zn2+的价层电子排布式是
(2)C、N、O的电负性
(3)三乙撑二胺(
 )与
)与 能形成配位键的原因是
能形成配位键的原因是(4)下列事实可用“水分子间存在氢键”解释的是
a.常压下,4℃时水的密度最大
b.水的沸点比硫化氢的沸点高160℃
c.水的热稳定性比硫化氢强
(5)对苯二甲酸(
 )中苯环上的碳原子的杂化方式为
)中苯环上的碳原子的杂化方式为
您最近一年使用:0次




