A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大。C是周期表中电负性最大的元素。基态E原子的核外电子有7种空间运动状态。基态F原子有3个未成对电子。按要求回答下列问题:
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式___________ 。
(2)基态原子第一电离能大小介于E和F之间的元素有___________ 。(用元素符号表示)
(3)氨硼烷(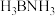 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为___________ (用元素符号表示)。
(4)磷酸盐在微生物作用下可转化为 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为___________ 。
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式
(2)基态原子第一电离能大小介于E和F之间的元素有
(3)氨硼烷(
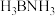 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为(4)磷酸盐在微生物作用下可转化为
 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为
更新时间:2024-03-04 16:11:59
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】科学家从化肥厂生产的(NH4)2SO4中检出组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子,N4分子不能被植物吸收。
请回答下列问题:
(1)N4和N2的关系正确的是______________ (填序号)
(2)N4H4(SO4)2______________ (填“能”或“不能”)和草木灰混合施用:
(3)已知白磷、NH4+、N4H44+的空间构型均为四面体, 的结构式为
的结构式为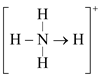 (
(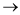 表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
表示共用电子对由N原子单方面提供),白磷(P4)的结构式为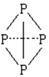
请画出 的结构式
的结构式____________________________________ ;
(4)已知液氨中存在着平衡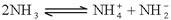 。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:
。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:_____________________________________________ ;
(5)含有一定量(NH4)2SO4和NH3·H2O的水溶液称为“缓冲溶液”,在此溶液中加入少量的强碱或强酸时,溶液的pH几乎不变,这可由下列离子方程式来说明。
加酸时: NH3·H2O+H+=NH4++H2O
加碱时: NH4++OH-= NH3·H2O
由于(NH4)2SO4和NH3·H2O的大量存在,加少量酸或碱时,溶液中C(H+)与C(OH-)基本保持不变;
含有一定量NaH2PO4和Na2HPO4的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或强碱时发生的离子反应方程式:
加酸时_____________________________________________ ;
加碱时_____________________________________________ 。
请回答下列问题:
(1)N4和N2的关系正确的是
| A.同种单质 | B.同位素 | C.同分异构体 | D.同素异形体 |
(2)N4H4(SO4)2
(3)已知白磷、NH4+、N4H44+的空间构型均为四面体,
 的结构式为
的结构式为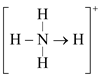 (
(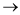 表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
表示共用电子对由N原子单方面提供),白磷(P4)的结构式为
请画出
 的结构式
的结构式(4)已知液氨中存在着平衡
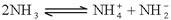 。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:
。科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式:(5)含有一定量(NH4)2SO4和NH3·H2O的水溶液称为“缓冲溶液”,在此溶液中加入少量的强碱或强酸时,溶液的pH几乎不变,这可由下列离子方程式来说明。
加酸时: NH3·H2O+H+=NH4++H2O
加碱时: NH4++OH-= NH3·H2O
由于(NH4)2SO4和NH3·H2O的大量存在,加少量酸或碱时,溶液中C(H+)与C(OH-)基本保持不变;
含有一定量NaH2PO4和Na2HPO4的溶液,也具有缓冲作用,写出此溶液中加入少量强酸或强碱时发生的离子反应方程式:
加酸时
加碱时
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)X和W的元素符号分别为____ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式__________ ,工业合成Y的氢化物的化学方程式为________________ 。
(3) X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是________ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为__________________________ 。
(4)写出铜和Y的最高价氧化物的水化物的稀溶液反应的离子方程式:______________ 。
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式:__________________________ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(1)X和W的元素符号分别为
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3) X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
(4)写出铜和Y的最高价氧化物的水化物的稀溶液反应的离子方程式:
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为-96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)铬(24号元素)基态原子的电子排布式为____ 。
(2)CH3COCH3分子中含有____ 个π键,含有____ 个σ键。
(3)固态氯化铬酰属于____ 晶体,丙酮中碳原子的杂化方式为____ ,二硫化碳属于____ (填“极性”或“非极性”)分子,分子中含有____ (填“极性”或“非极性”)键。
(1)铬(24号元素)基态原子的电子排布式为
(2)CH3COCH3分子中含有
(3)固态氯化铬酰属于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe3+离子中未成对的电子数为_____ 。
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I1(Li)> I1(Na),原因是__ ,Li、Be、B三元素的第一电离能I1(Be)、 I1(B)、 I1(Li)之间的大小关系是__ 。
(3)磷酸根离子的空间构型为__ ,其中P的价层电子对数为__ 、杂化轨道类型为__ 。
(1)基态Fe3+离子中未成对的电子数为
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I1(Li)> I1(Na),原因是
(3)磷酸根离子的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
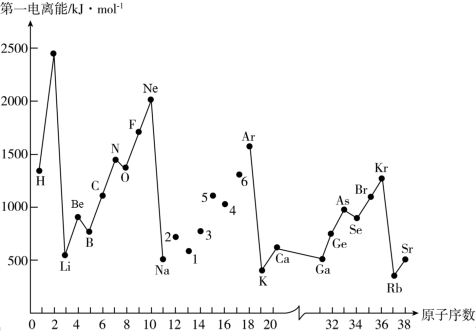
请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象______ 。
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是_______ ;
(3)图中5号元素在周期表中的位置是_________ ;
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是_______ 。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)

请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)图中5号元素在周期表中的位置是
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】第三代半导体中,碳化硅(SiC)和氮化镓(GaN)是核心半导体。它们具有更宽的禁带宽度、更高的导热率、更高的抗辐射能力、更大的电子饱和漂移速率等特性。
(1)基态Ga原子的价电子排布式为____ 。
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为____ 。
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3 GaN+3HCl。
GaN+3HCl。
①GaCl3的熔点为77.9℃,其晶体类型为____ ,它在高温时会形成双聚分子(GaCl3)2,该双聚分子的结构式为____ 。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是____ 。
②上述反应涉及的元素中,电负性最小的是____ (填元素符号,下同),第一电离能最大的是____ 。
(1)基态Ga原子的价电子排布式为
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3
 GaN+3HCl。
GaN+3HCl。①GaCl3的熔点为77.9℃,其晶体类型为
②上述反应涉及的元素中,电负性最小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)O、F、Cl电负性由大到小的顺序为________ ;OF2分子的空间构型为_______ ;OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O,原因是________ 。
(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价层电子轨道表示式为___________ ;第二周期的元素中,第一电离能介于B和N之间的元素有___________ 种。
(2)PH3分子的空间结构为___________ ,其中存在的共价键类型为___________ ,PH3的沸点___________ (填“高于”或“低于”)NH3,原因是___________ 。
(3)雌黄的分子式为As2S3,其分子结构如图所示: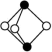 ,As原子的杂化类型为
,As原子的杂化类型为___________ 。
(4)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。 的空间结构为
的空间结构为___________ ; [Cu(NH3)4]SO4·H2O固体中含有的化学键有___________ (填字母)。
A.离子键 B.共价键 C.氢键 D.金属键
(1)基态氮原子的价层电子轨道表示式为
(2)PH3分子的空间结构为
(3)雌黄的分子式为As2S3,其分子结构如图所示:
 ,As原子的杂化类型为
,As原子的杂化类型为(4)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。
 的空间结构为
的空间结构为A.离子键 B.共价键 C.氢键 D.金属键
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】完成下列小题
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间结构是___________ ,中心原子的杂化方式为___________ 。
(2)根据价层电子对互斥模型,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(3)ZnCO3中,阴离子空间结构为___________ ,C原子的杂化方式为___________ 。
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间结构是
(2)根据价层电子对互斥模型,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)ZnCO3中,阴离子空间结构为
您最近一年使用:0次

 价层电子的轨道表示式
价层电子的轨道表示式 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)

