中国古代四大发明之一——黑火药,它的爆炸反应为2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
(1)除S外,上列元素的电负性从大到小依次为________ 。
(2)在生成物中,A的晶体类型为________ ,含极性共价键的分子的中心原子轨道杂化类型为________ 。
(3)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为________ 。
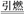 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)(1)除S外,上列元素的电负性从大到小依次为
(2)在生成物中,A的晶体类型为
(3)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
更新时间:2018/02/10 22:59:58
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)下列关于CH4和CO2的说法正确的是________ (填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(2)Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有________ mol σ键。
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
①“可燃冰”中分子间存在的2种作用力是______________________ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是______________________________ 。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(2)Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
| 分子 参数 | 分子直径/nm | 分子与H2O的结合能 E/kJ·mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |

①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_________ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_________ ,能量最低的是_________ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p c.1s22s22p63s13p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的_________ 区,最高能层电子的电子云轮廓形状为_________ ,其价电子排布式为_________ 。与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子的轨道表示式_________ 。
(4)下列各组多电子原子的能级能量比较不正确的是_________。
①2p=3p ②4s>2s ③4p>4f ④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p c.1s22s22p63s13p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)下列各组多电子原子的能级能量比较不正确的是_________。
①2p=3p ②4s>2s ③4p>4f ④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价层电子轨道表示式为___________ ;第二周期的元素中,第一电离能介于B和N之间的元素有___________ 种。
(2)PH3分子的空间结构为___________ ,其中存在的共价键类型为___________ ,PH3的沸点___________ (填“高于”或“低于”)NH3,原因是___________ 。
(3)雌黄的分子式为As2S3,其分子结构如图所示: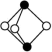 ,As原子的杂化类型为
,As原子的杂化类型为___________ 。
(4)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。 的空间结构为
的空间结构为___________ ; [Cu(NH3)4]SO4·H2O固体中含有的化学键有___________ (填字母)。
A.离子键 B.共价键 C.氢键 D.金属键
(1)基态氮原子的价层电子轨道表示式为
(2)PH3分子的空间结构为
(3)雌黄的分子式为As2S3,其分子结构如图所示:
 ,As原子的杂化类型为
,As原子的杂化类型为(4)向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。
 的空间结构为
的空间结构为A.离子键 B.共价键 C.氢键 D.金属键
您最近半年使用:0次
【推荐1】用符号“>”或“<”表示下列各项关系。
(1)第一电离能:Na__________ Mg,Mg _______ Ca。
(2)电负性:O________ F,F ________ Cl。
(3)能量高低:ns________ (n+1)s,ns ________ np。
(1)第一电离能:Na
(2)电负性:O
(3)能量高低:ns
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据信息回答下列问题:不同元素的原子在分子内吸引键合电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子间的电负性差值小于1.7通常形成共价键。下表是某些元素的电负性值:
(1)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围:___________ 。
(2)请归纳元素的电负性和金属性、非金属性的关系是___________ 。
(3)推测AlF3、AlCl3、AlBr3是离子化合物还是共价化合物:AlF3___________ ,AlCl3___________ , AlBr3___________ 。
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
(2)请归纳元素的电负性和金属性、非金属性的关系是
(3)推测AlF3、AlCl3、AlBr3是离子化合物还是共价化合物:AlF3
您最近半年使用:0次
【推荐3】请填空:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为___________ 。
(2)B元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,B的元素号为___________ ,其正二价离子的电子排布式为___________ 。
(3)C元素的原子最外层电子排布式为nsnnpn+1,则C的电子排布图为___________ 。
(4)在元素周期表中,电负性最大的元素是___________ ,第三周期p轨道半充满的元素是___________ 。
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为
(2)B元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,B的元素号为
(3)C元素的原子最外层电子排布式为nsnnpn+1,则C的电子排布图为
(4)在元素周期表中,电负性最大的元素是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下列有机化合物中,都有多个官能团:
A.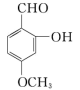 B.
B. C.
C. D.
D. E.CH2=CHCOOCH3
E.CH2=CHCOOCH3
(1)可以看作醇的是___________ (填写字母,下同)。
(2)可以看作酚的是___________ 。
(3)可以看作羧酸的是___________ 。
(4)可以看作酯的是___________ 。
(5)E中σ键和π键个数比为___________ 。
A.
 B.
B. C.
C. D.
D. E.CH2=CHCOOCH3
E.CH2=CHCOOCH3(1)可以看作醇的是
(2)可以看作酚的是
(3)可以看作羧酸的是
(4)可以看作酯的是
(5)E中σ键和π键个数比为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】在下列7种物质中: ① N2 ② CO2 ③ CH2Cl2 ④ C2H4 ⑤ CaCl2 ⑥ Na2O2,只含有非极性键的分子是_______ ,既含离子键又含共价键的化合物是_________ ,只存在σ键的分子是_______ ,只存在1个π键的分子是________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】关于化学键和分子间作用力的理论是关于物质结构的基本理论。
(1)N、P、As 电负性由大到小的顺序为___________ 。
(2)用“>”或“<”填空:
(3)MgCl2在工业上应用广泛,可由 MgO 制备。MgO 的熔点比 BaO 的熔点___________ (填“高” 或“低”)。
(4)HCHO 分子的立体构型为___________ 形,它与 H2加成后,加成产物的熔、沸点比 CH4的熔、沸点高,其主要原因是___________ (须指明加成产物是何物质) 。
(5)已知 H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键的夹角均为96o52′。
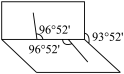
①H2O2分子是含有_______ 键和_______ 键的________ (填“极性”或“非极性”)分子。
②H2O2难溶于 CS2,简要说明理由:___________ 。
(1)N、P、As 电负性由大到小的顺序为
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |
(4)HCHO 分子的立体构型为
(5)已知 H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键的夹角均为96o52′。

①H2O2分子是含有
②H2O2难溶于 CS2,简要说明理由:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为2CH3OH+O2 2
2 +2H2O。
+2H2O。
(1)H2O的中心原子上的孤电子对数为____ 。
(2)HCHO分子内σ键与π键个数之比为____ ,HCHO的空间结构为____ 。
(3)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为____ 和____ 。
(4)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为____ 。
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:___ 。
 2
2 +2H2O。
+2H2O。(1)H2O的中心原子上的孤电子对数为
(2)HCHO分子内σ键与π键个数之比为
(3)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为
(4)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O==NaN3+NaOH+NH3,3NaNH2+NaNO3==NaN3+3NaOH+NH3↑。
回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是________ ,第一电离能最小的元素是_______ 。
(2)基态氮原子的L层电子排布图为_________________ 。
(3)与N3-互为等电子体的分子为_________ (写出一种)。依据价层电子对互斥理论,NO3-的空间构型是______________ ,其中心原子杂化类型是__________ 。
(4)叠氮化钠中不含有 的化学键类型有_____________ 。
A.离子键 B.极性共价键 C.σ键 D.π键
回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是
(2)基态氮原子的L层电子排布图为
(3)与N3-互为等电子体的分子为
(4)叠氮化钠中
A.离子键 B.极性共价键 C.σ键 D.π键
您最近半年使用:0次

 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是

