Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据如表所示:
(1)Mn元素原子的电子排布式为___________ 。比较两元素的I2、I3可知:气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是___________ 。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是___________ 。
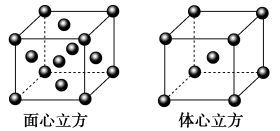
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为___________ 。
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为

更新时间:2021-05-28 07:51:44
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___ (填标号)。
A. [Ne]3s1 B. [Ne]3s2 C. [Ne]3s13p1 D. [Ne]3p1
(2)Li2O是离子晶体,其晶格能可通过如图的Born-Haber循环计算得到。Li原子的第一电离能为___ kJ·mol-1,O=O键键能为__ kJ·mol-1。

(3)NH4H2PO4中,电负性最高的元素是__ 。
A. [Ne]3s1 B. [Ne]3s2 C. [Ne]3s13p1 D. [Ne]3p1
(2)Li2O是离子晶体,其晶格能可通过如图的Born-Haber循环计算得到。Li原子的第一电离能为

(3)NH4H2PO4中,电负性最高的元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
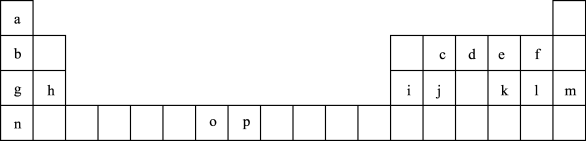
(1)基态o原子的价层电子排布图为_______ ;基态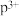 的最外层电子排布式为
的最外层电子排布式为_______ 。
(2)n的原子结构示意图为_______ ;基态j原子的核外电子填充时最高能级符号为_______ 。
(3)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为_______ (用元素符号表示),第一电离能由大到小排序为_______ (用元素符号表示)。

(1)基态o原子的价层电子排布图为
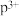 的最外层电子排布式为
的最外层电子排布式为(2)n的原子结构示意图为
(3)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】钴的一种配位聚合物的化学式为{[Co(bte)2(H2O)2](NO3)2}n。
(1)Co2+基态核外电子排布式为___________ 。
(2)NO 的空间结构为
的空间结构为___________ 。
(3)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是___________ 和___________ (填元素符号)。
②C、H、N的电负性从大到小顺序为___________ 。
③bte分子中碳原子轨道杂化类型为___________ 和___________ 。
④1mol bte分子中含 键的数目为
键的数目为___________ mol。
(1)Co2+基态核外电子排布式为
(2)NO
 的空间结构为
的空间结构为(3)bte的分子式为C6H8N6,其结构简式如图所示。

①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是
②C、H、N的电负性从大到小顺序为
③bte分子中碳原子轨道杂化类型为
④1mol bte分子中含
 键的数目为
键的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)以下微粒:①N2H5②CH4③OH-④NH4+
⑤Fe(CO)3⑥Fe(SCN)3⑦H3O+⑧[Ag(NH3)2]OH,含配位键的是:________ 。
(2)在配合物[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是____ ,画出配合物离子[Cu(NH3)4]2+中的配位键:___ 。
⑤Fe(CO)3⑥Fe(SCN)3⑦H3O+⑧[Ag(NH3)2]OH,含配位键的是:
(2)在配合物[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在化学实验和科学研究中,水是一种常用的试剂。
(1)水分子中的氧原子在基态时的价电子排布式为:___________ 。
(2)水分子在特定条件下容易得到一个H+而形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是___________ 。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)在冰晶体中,每个水分子与相邻的4个水分子形成___________ 键,水分子间还存在___________ ,1mol H2O中含___________ mol氢键。
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位离子。请写出生成此配位离子的离子方程式:___________ 。
(1)水分子中的氧原子在基态时的价电子排布式为:
(2)水分子在特定条件下容易得到一个H+而形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)在冰晶体中,每个水分子与相邻的4个水分子形成
(4)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位离子。请写出生成此配位离子的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据晶体结构知识,回答下列问题:
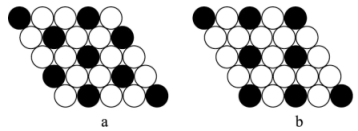
(1)如图所示为二维平面晶体示意图,所表示的化学式为AX3的是_______ 。(填字母标号)
(2)Al的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
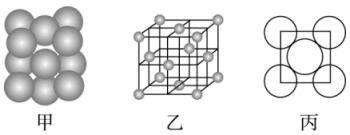
若已知Al的原子半径为d,NA表示阿伏加德罗常数,Al的相对原子质量为M,则:
①晶胞中Al原子的配位数为_______ 。
②该晶体的密度为_______ (用字母表示)。
(3)下图为氟化钙晶胞,试回答下列问题:
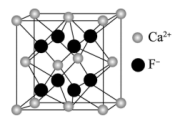
每个F-周围有_______ 个Ca2+与之紧邻,每个F-周围与其距离最近的F-的数目是_______ 。
(4)已知晶体硼结构单元是由硼原子组成的正二十面体(如图),其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。通过观察图形及推算,此晶体结构单元由_______ 个硼原子构成。
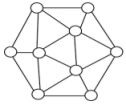
(1)如图所示为二维平面晶体示意图,所表示的化学式为AX3的是

(2)Al的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。

若已知Al的原子半径为d,NA表示阿伏加德罗常数,Al的相对原子质量为M,则:
①晶胞中Al原子的配位数为
②该晶体的密度为
(3)下图为氟化钙晶胞,试回答下列问题:

每个F-周围有
(4)已知晶体硼结构单元是由硼原子组成的正二十面体(如图),其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。通过观察图形及推算,此晶体结构单元由

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】锑酸亚铁晶胞如图所示,其晶胞参数分别为a nm、b nm、c nm,α=β=γ=90°,则:

(1)锑酸亚铁的化学式为_______ 。
(2)晶体的密度为_______ g·cm-3(设NA为阿伏加德罗常数的值)。

(1)锑酸亚铁的化学式为
(2)晶体的密度为
您最近一年使用:0次