硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:___________ ;B、N、H的电负性由大到小的顺序为___________ 。
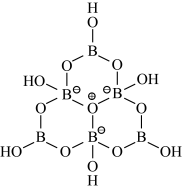
(2)科学家合成了一种含硼阴离子 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为___________ ,该结构中共有___________ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子___________ (填离子符号); 空间构型为
空间构型为___________ 。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子 空间构型为
空间构型为
更新时间:2023-06-10 17:41:23
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】V的价电子排布图___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】C、O、S、 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
(1) 元素在元素周期表的位置是
元素在元素周期表的位置是_______ ,基态 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是_______ ,基态 原子的简化电子排布式为
原子的简化电子排布式为_______ 。
(2)基态S原子的价层电子轨道表示式为_______ , 属于
属于_______ 分子(填“极性”或“非极性”)。
(3) 的键角
的键角_______  的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是_______
(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。 比
比 的离子半径小,原因是
的离子半径小,原因是_______ 。
 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:(1)
 元素在元素周期表的位置是
元素在元素周期表的位置是 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是 原子的简化电子排布式为
原子的简化电子排布式为(2)基态S原子的价层电子轨道表示式为
 属于
属于(3)
 的键角
的键角 的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是 比
比 的离子半径小,原因是
的离子半径小,原因是
您最近一年使用:0次
【推荐1】I.雄黄( )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
(1)基态硫原子核外电子的运动轨道数有_______ 种;有___________ 种能量不同的电子;
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)S和As比较,电负性较大的是___________
(4)As元素的第一电离能___________ Se元素的第一电离能(填“大于”“小于”或“等于”),原因是_______________________________ 。
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是________ ,属于两性化合物,证明这一结论的有关离子方程式为__________________________ 、________________ 。
(6)若已知反应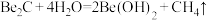 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______________________ 。
(7)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是________________ 。用电子式表示 的形成过程:
的形成过程:__________
 )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:(1)基态硫原子核外电子的运动轨道数有
(2)基态砷原子的价层电子的轨道表示式为
(3)S和As比较,电负性较大的是
(4)As元素的第一电离能
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是
(6)若已知反应
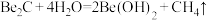 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(7)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮化硅(Si3N4)陶瓷可代替金属制造发动机的耐热部件。工业上用气相沉淀法制备氨化硅: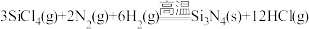 。请回答:
。请回答:
(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si___________ H(选填“<”或“>”)。
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是___________ 。
(3)氮化硅(Si3N4)的晶体类型为___________
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
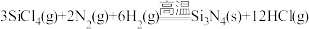 。请回答:
。请回答:(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是
(3)氮化硅(Si3N4)的晶体类型为
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
| A.是一种活泼的金属元素 |
| B.其电负性大于硫 |
| C.其单质可作为半导体材料 |
| D.其气态氢化物的稳定性低于硅的气态氢化物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)SO 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为___________ ; 的空间构型为
的空间构型为___________ (用文字描述)。
(2)与O3分子互为等电子体的一种阴离子为___________ (填化学式)。
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为(2)与O3分子互为等电子体的一种阴离子为
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
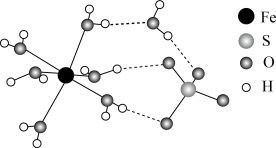
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】元素X和Y属于同一主族。负二价的元素X和氢形成的化合物在通常状况下是一种液体,其中X的质量分数约为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)写出基态Y原子的电子排布式:___________ 。
(2)在X和Y两种元素形成的化合物中:
①X的质量分数为50%的化合物的化学式为___________ ;该分子的中心原子发生___________ 杂化,分子构型为___________ 。
②X的质量分数为60%的化合物的化学式为___________ ;该分子的中心原子发生___________ 杂化,分子构型为___________ 。
(3)由元素X、Y和氢三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式___________ 、___________ ,两种酸的阴离子分别为___________ 和___________ ,其立体构型分别为___________ 和___________ 。
(4)在由氢元素与X元素形成的化合物中,含有非极性键的是___________ (写分子式),分子构型为V形的是___________ (写分子式)。
(1)写出基态Y原子的电子排布式:
(2)在X和Y两种元素形成的化合物中:
①X的质量分数为50%的化合物的化学式为
②X的质量分数为60%的化合物的化学式为
(3)由元素X、Y和氢三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式
(4)在由氢元素与X元素形成的化合物中,含有非极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1) 分子的中心原子的杂化类型
分子的中心原子的杂化类型___________ 。
(2) 分子中共价键的类型分别是_______。
分子中共价键的类型分别是_______。
(1)
 分子的中心原子的杂化类型
分子的中心原子的杂化类型(2)
 分子中共价键的类型分别是_______。
分子中共价键的类型分别是_______。A. 键、非极性健 键、非极性健 | B. 键、极性键 键、极性键 |
C. 键、非极性键 键、非极性键 | D. 键、极性键 键、极性键 |
您最近一年使用:0次
【推荐2】回答下列问题:
(1) 基态原子核外电子排布式为
基态原子核外电子排布式为_______ ,基态 原子核外占据最高能层电子的电子云轮廓图形状为
原子核外占据最高能层电子的电子云轮廓图形状为_______ ;基态F原子的价电子轨道表达式为_______ 。
(2)硝酸锰是工业制备中常用的催化剂, 的
的 空间构型为
空间构型为_______ ;写出锰的基态原子的价电子排布式_______ ;
(3)O的第一电离能_______ (填“大于”或“小于”)N的第一电离能,原因为_______ 。
(4)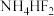 的组成元素的电负性由大到小的顺序为
的组成元素的电负性由大到小的顺序为_______ 。(用元素符号表示);其中N原子的杂化方式为_______ ; 能形成分子缔合体
能形成分子缔合体 的原因为
的原因为_______ 。
(1)
 基态原子核外电子排布式为
基态原子核外电子排布式为 原子核外占据最高能层电子的电子云轮廓图形状为
原子核外占据最高能层电子的电子云轮廓图形状为(2)硝酸锰是工业制备中常用的催化剂,
 的
的 空间构型为
空间构型为(3)O的第一电离能
(4)
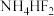 的组成元素的电负性由大到小的顺序为
的组成元素的电负性由大到小的顺序为 能形成分子缔合体
能形成分子缔合体 的原因为
的原因为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题。
(1) 中的化学键属于
中的化学键属于___________ (填“σ”或“π”)键。
(2) 分子中,中心原子上的σ键电子对数为
分子中,中心原子上的σ键电子对数为___________ ,孤电子对数为___________ ,价层电子对数为___________ ,中心原子的杂化方式为___________ ,VSEPR模型为___________ ,分子的空间结构为___________ 。
(3)下列分子中若有手性分子,请用“*”标出其手性碳原子;若无手性分子,此小题不必作答。
(1)
 中的化学键属于
中的化学键属于(2)
 分子中,中心原子上的σ键电子对数为
分子中,中心原子上的σ键电子对数为(3)下列分子中若有手性分子,请用“*”标出其手性碳原子;若无手性分子,此小题不必作答。

您最近一年使用:0次

 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(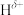 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(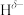 ),电负性大小顺序是
),电负性大小顺序是

