N、P两种元素位于元素周期表第VA族。请回答下列问题:
(1)基态氮原子的电子排布式为________ ;基态氮原子的价层电子的轨道表示式为________ 。
(2)基态磷原子中,其占据的最高能层的符号是________ ;基态磷原子占据的最高能级共有________ 个原子轨道,其形状是________ 。
(3)电负性:N________ P(填>或<)。
(4)雷酸汞曾被用作起爆药,雷酸汞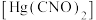 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为________ >________ >________ (填元素符号)。
(1)基态氮原子的电子排布式为
(2)基态磷原子中,其占据的最高能层的符号是
(3)电负性:N
(4)雷酸汞曾被用作起爆药,雷酸汞
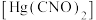 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为
更新时间:2023-02-15 06:28:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在氧化硅表面生长高质量六方氮化硼薄膜。回答下面问题:
(1)写出硼的元素符号______ ,其在元素周期表的位置为______ 。
(2)基态O原子的核外电子空间运动状态有______ 种,第二周期主族元素中,第一电离能比O元素大的有______ 种,电负性比O元素大的有______ 。
(3)写出基态Si原子的电子排布式______ ,其单电子数有______ 个。已知H的电负性大于Si,则在硅烷( )中H元素的化合价是
)中H元素的化合价是______ ,中心原子Si的杂化类型是______ 。硅烷分子的空间构型是______ 。
(4)将铬(Cr)原子填充在 ,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
,空隙中,形成常用的催化剂。元素Cr在周期表中的位置______ ,属于______ 区,其基态原子的价层电子排布式为______ 。
(1)写出硼的元素符号
(2)基态O原子的核外电子空间运动状态有
(3)写出基态Si原子的电子排布式
 )中H元素的化合价是
)中H元素的化合价是(4)将铬(Cr)原子填充在
 ,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
,空隙中,形成常用的催化剂。元素Cr在周期表中的位置
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】甲苯是重要的有机溶剂及有机合成原料。回答下列问题:
(1)溶解下列物质不能用甲苯作溶剂的是_____(填标号)。
(2) 甲苯通过原子轨道“头碰头”的方式重叠形成的共价键数目是
甲苯通过原子轨道“头碰头”的方式重叠形成的共价键数目是_____  ,下图表示甲基中碳氢键成键方式的是
,下图表示甲基中碳氢键成键方式的是_____ (填标号)。 溶液氧化生成苯甲酸。
溶液氧化生成苯甲酸。
①Mn元素位于周期表_____ 区,Mn原子的价电子排布式是_____ 。
①写出甲苯生成TNT的反应方程式_____ ,TNT中所含元素的电负性由大到小的顺序是_____ (写元素符号)。
②甲苯比苯更容易发生硝化反应的原因是_____ 。
(1)溶解下列物质不能用甲苯作溶剂的是_____(填标号)。
| A.乙醇 | B.氯仿 | C.纯碱 | D.冰醋酸 |
 甲苯通过原子轨道“头碰头”的方式重叠形成的共价键数目是
甲苯通过原子轨道“头碰头”的方式重叠形成的共价键数目是 ,下图表示甲基中碳氢键成键方式的是
,下图表示甲基中碳氢键成键方式的是A. B.
B. C.
C. D.
D.
 溶液氧化生成苯甲酸。
溶液氧化生成苯甲酸。①Mn元素位于周期表
(2)水杨醛( )是苯甲酸的同分异构体。水杨醛的沸点
)是苯甲酸的同分异构体。水杨醛的沸点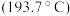 低于苯甲酸的沸点
低于苯甲酸的沸点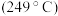 ,原因是
,原因是
①写出甲苯生成TNT的反应方程式
②甲苯比苯更容易发生硝化反应的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号:B:___________ C:___________ D:___________
(2)用元素符号表示A2B2的电子式为___________ 。
(3)E元素在元素周期表的位置为:___________ ,属于___________ 区,它有___________ 个能层。
(4)D原子核外电子排布式为___________ , 离子价层电子轨道表示式为
离子价层电子轨道表示式为___________ , 价层电子排布式的特点是
价层电子排布式的特点是___________ 。
(5)检验某溶液中是否含有 ,通常所用的试剂是
,通常所用的试剂是___________ 和___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有17个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示A2B2的电子式为
(3)E元素在元素周期表的位置为:
(4)D原子核外电子排布式为
 离子价层电子轨道表示式为
离子价层电子轨道表示式为 价层电子排布式的特点是
价层电子排布式的特点是(5)检验某溶液中是否含有
 ,通常所用的试剂是
,通常所用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】磷酸氯喹(结构如图所示)是由氢、碳、氮、氯、磷、氧元素组成的有机物,在细胞水平上能有效抑制新型冠状病毒的感染,我国印发的《新型冠状病毒肺炎诊疗方案(试行第七版)》中明确规定了其用量。
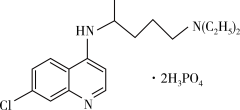
(1)碳、硅、储为同一主族元素,则基态硅原子核外有____ 种运动状态的电子,基态锗原子的最外层电子的轨道表示式为_____ 。
(2)氮原子价层电子的轨道表示式为_____ 。
(3)基态Cl原子中,核外电子占据最高能层的符号是____ 。
(4)氧元素基态原子核外K层电子的自旋状态_____ (填“相同”或“相反”)。

(1)碳、硅、储为同一主族元素,则基态硅原子核外有
(2)氮原子价层电子的轨道表示式为
(3)基态Cl原子中,核外电子占据最高能层的符号是
(4)氧元素基态原子核外K层电子的自旋状态
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________
(2)Cu2+基态核外电子排布式为___________
(3)Zn原子核外电子排布式为___________
(4)氮原子价层电子的轨道表达式(电子排布图)为___________
(5)Co基态原子核外电子排布式为___________
(1)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为
(2)Cu2+基态核外电子排布式为
(3)Zn原子核外电子排布式为
(4)氮原子价层电子的轨道表达式(电子排布图)为
(5)Co基态原子核外电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。请回答以下问题:
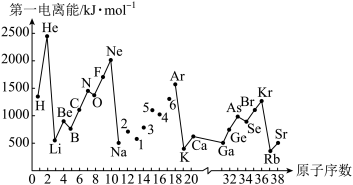
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象____ 。
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律____ 。
(3)图中5号元素在周期表中的位置是____ 、电子排布____ 。
(4)图中N元素比O元素第一电离能高的原因是____ 。
(5)C、H元素形成的化合物分子中共有14个电子,该分子中____ 个σ键,____ 个π键,中心原子杂化模式____ ,分子空间构型____ 。

(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律
(3)图中5号元素在周期表中的位置是
(4)图中N元素比O元素第一电离能高的原因是
(5)C、H元素形成的化合物分子中共有14个电子,该分子中
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
(1)写出下列元素的符号:B_____ 、C_____ 。
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是____ ,电负性最大的元素是____ 。
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在____ 区。
(4)写出A的核外电子排布式_____ 。
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的价电子排布式3d64s2。回答下列问题:(1)写出下列元素的符号:B
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(3)已知元素周期表可按电子排布分为s区、p区等,则E元素在
(4)写出A的核外电子排布式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)元素C、N、O、K的电负性从大到小依次为______ 。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为______ 。
(3)下图是周期表中短周期的一部分,A的单质是空气中含量最多的物质,其中第一电离能最小的元素是______ (填“A”“B”“C”或“D”)。

(4)氮化硼(BN)是一种重要的功能陶瓷材料。基态B原子的电子排布式为______ ;B和N相比,电负性较大的是______ ,BN中B元素的化合价为______ 。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)下图是周期表中短周期的一部分,A的单质是空气中含量最多的物质,其中第一电离能最小的元素是

(4)氮化硼(BN)是一种重要的功能陶瓷材料。基态B原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___ ;氮元素的E1呈现异常的原因是__ 。

(2)C、H、O三种元素的电负性由小到大的顺序为___ 。
(3)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是__ 。

(2)C、H、O三种元素的电负性由小到大的顺序为
(3)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】第三代半导体中,碳化硅(SiC)和氮化镓(GaN)是核心半导体。它们具有更宽的禁带宽度、更高的导热率、更高的抗辐射能力、更大的电子饱和漂移速率等特性。
(1)基态Ga原子的价电子排布式为____ 。
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为____ 。
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3 GaN+3HCl。
GaN+3HCl。
①GaCl3的熔点为77.9℃,其晶体类型为____ ,它在高温时会形成双聚分子(GaCl3)2,该双聚分子的结构式为____ 。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是____ 。
②上述反应涉及的元素中,电负性最小的是____ (填元素符号,下同),第一电离能最大的是____ 。
(1)基态Ga原子的价电子排布式为
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3
 GaN+3HCl。
GaN+3HCl。①GaCl3的熔点为77.9℃,其晶体类型为
②上述反应涉及的元素中,电负性最小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是某些短周期元素的电负性(x)值:
(1)根据上表试推测,元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为___________ 。
(2)已知: 。
。
①若 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测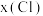 的范围是
的范围是___________ (填表中数值);
② 水解的化学反应方程式是
水解的化学反应方程式是___________ 。
(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析, 属于
属于___________ (填“离子化合物”或“共价化合物”),可设计实验证明,如测定___________ 。
| 元素符号 | Li | Be | N | O | F | Na | Mg | Al | P | S |
| x值 | 1.0 | 1.5 | 3.0 | a | 4.0 | 0.9 | 1.2 | 1.5 | 2.1 | 2.5 |
(2)已知:
 。
。①若
 最初水解产物是
最初水解产物是 和HClO,根据
和HClO,根据 的化合价推测
的化合价推测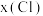 的范围是
的范围是②
 水解的化学反应方程式是
水解的化学反应方程式是(3)一般认为:如果两个成键元素间的电负性差值大于1.7,它们之间通常形成离子键,小于1.7通常形成共价键,结合问题(2)①进行分析,
 属于
属于
您最近一年使用:0次



