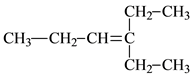第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。请回答以下问题:
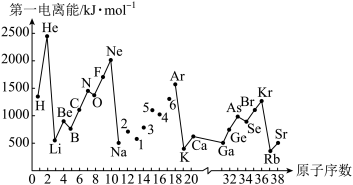
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象____ 。
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律____ 。
(3)图中5号元素在周期表中的位置是____ 、电子排布____ 。
(4)图中N元素比O元素第一电离能高的原因是____ 。
(5)C、H元素形成的化合物分子中共有14个电子,该分子中____ 个σ键,____ 个π键,中心原子杂化模式____ ,分子空间构型____ 。

(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图分析可知,同一主族元素原子第一电离能I1变化规律
(3)图中5号元素在周期表中的位置是
(4)图中N元素比O元素第一电离能高的原因是
(5)C、H元素形成的化合物分子中共有14个电子,该分子中
更新时间:2022-09-18 22:12:23
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为___________ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是___________ (填选项字母)。
A.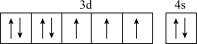
B.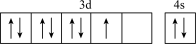
C.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为___________ (用元素符号表示),原因为___________ 。
(3)钛元素位于元素周期表___________ 区;基态钛原子中,最外层电子的电子云轮廓图为___________ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.

B.

C.

D.

(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
您最近一年使用:0次
【推荐2】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式___ 。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有___ 和___ 。
(3)黄血盐中N原子的杂化方式为____ ;C、N、O的第一电离能由大到小的排序为___ ,电负性由大到小的排序为___ 。
(1)写出基态Fe3+的核外电子排布式
(2)K4[Fe(CN)6]中的作用力除共价键外,还有
(3)黄血盐中N原子的杂化方式为
您最近一年使用:0次
【推荐3】CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。CO进入血液后有如下平衡: 。
。
(1)C、N、O三种元素,第一电离能由大到小的顺序为___________ 。
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是___________ 。
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:___________ 。
 。
。(1)C、N、O三种元素,第一电离能由大到小的顺序为
(2)在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是
(3)高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
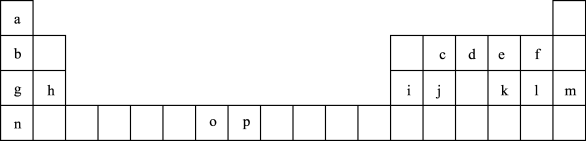
(1)基态o原子的价层电子排布图为_______ ;基态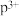 的最外层电子排布式为
的最外层电子排布式为_______ 。
(2)n的原子结构示意图为_______ ;基态j原子的核外电子填充时最高能级符号为_______ 。
(3)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为_______ (用元素符号表示),第一电离能由大到小排序为_______ (用元素符号表示)。

(1)基态o原子的价层电子排布图为
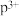 的最外层电子排布式为
的最外层电子排布式为(2)n的原子结构示意图为
(3)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为
您最近一年使用:0次
【推荐2】丁二酮肟(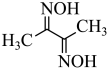 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:
(1)Ni在元素周期表中的位置为___________ 。
(2)基态氧原子的核外电子的空间运动状态有___________ 种。
(3)丁二酮肟( )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ;与氮同周期的硼在成键时,能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:___________ ,该过程形成的原子光谱为___________ (填“吸收”或“发射”)光谱。
(4)与Ni同周期的铜、锌两种元素位于元素周期表的___________ 区,两元素的第一电离能( )、第二电离能(
)、第二电离能( )数据如表所示:
)数据如表所示:
铜的 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是___________ 。
 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:(1)Ni在元素周期表中的位置为
(2)基态氧原子的核外电子的空间运动状态有
(3)丁二酮肟(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为(4)与Ni同周期的铜、锌两种元素位于元素周期表的
 )、第二电离能(
)、第二电离能( )数据如表所示:
)数据如表所示:电离能/( ) ) |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为2CH3OH+O2 2
2 +2H2O。
+2H2O。
(1)H2O的中心原子上的孤电子对数为____ 。
(2)HCHO分子内σ键与π键个数之比为____ ,HCHO的空间结构为____ 。
(3)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为____ 和____ 。
(4)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为____ 。
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:___ 。
 2
2 +2H2O。
+2H2O。(1)H2O的中心原子上的孤电子对数为
(2)HCHO分子内σ键与π键个数之比为
(3)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为
(4)甲醇氧化生成HCHO时,会产生CO、CO2、CH3OCH3等副产物。相同条件下,CO2的沸点比O2的高,主要原因为
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:
您最近一年使用:0次
【推荐2】CuSCN是一种生物防腐涂料,可用CuSO4、NaSCN、Na2SO3作原料,并用乙二醇或DMF作分散剂进行制备。
(1) Cu+基态核外电子排布式为____________ 。
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为____________ ;Na2SO3中SO32-的空间构型为____________ (用文字描述)。
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为____________________ 。
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为____________ ;1 mol DMF分子中含有σ键的数目为____________ 。
(1) Cu+基态核外电子排布式为
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为
您最近一年使用:0次