氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
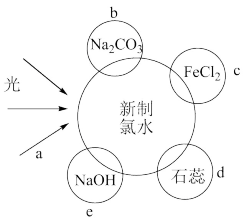
(1)氯水中含有的粒子有H2O、Cl2、___________ 、H+、Cl-、___________ 、OH-七种。
(2)久置的氯水变为___________ ,原因是___________ (用化学反应方程式表示);实验室保存饱和氯水的方法是___________ 。
(3)b过程中的离子方程式是___________ 。
(4)e过程中所发生的主要反应的化学方程式为___________ 。
(5)能证明氯水具有漂白性的是___________ (填“a”、“b”、“c”或“d”)。

(1)氯水中含有的粒子有H2O、Cl2、
(2)久置的氯水变为
(3)b过程中的离子方程式是
(4)e过程中所发生的主要反应的化学方程式为
(5)能证明氯水具有漂白性的是
20-21高一上·广东东莞·期中 查看更多[4]
广东省东莞市光明中学2020-2021学年高一上学期期中考试化学试题(已下线)3.1.2 氯气的性质与应用-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)专题四 氯及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)【定心卷】2.2.1 氯气的性质随堂练习-人教版2023-2024学年必修第一册
更新时间:2021-09-19 23:43:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是_______ (填序号,下同),主要成分属于盐类的是_______ ,相互间能发生反应的是_______ 。
(2)食盐不慎洒落在天然气的火焰上,可观察到_______ 。
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是_______ 。
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的_______ (填物质名称),将该反应的离子方程式补充完整:
ClO- + CO2 + H2O =_______ + _____
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为_______ 。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,可观察到
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的
ClO- + CO2 + H2O =
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精、含氯消毒剂、过氧乙酸等可有效灭活病毒。回答下列问题:
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为_______ 。
②氯水经光照后酸性增强,用化学方程表示其原因:_______ 。
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为_______ 。
②它的消毒原理是_______ (用化学方程式表示)。
③由以上反应证明 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸_______ 。
④工业生产漂白粉的化学方程式为_______ 。
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为_______ 。
(4)将 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为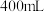 。试计算:
。试计算:
①原混合物中 的质量为
的质量为_______  。
。
②所得溶液的物质的量浓度为_______  。
。
(1)Cl2是最早用于饮用水消毒的物质,主要是利用Cl2溶于水生成的次氯酸灭活病毒。
①Cl2与水反应的化学方程式为
②氯水经光照后酸性增强,用化学方程表示其原因:
(2)漂白液、漂白粉和漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境消毒剂。
①漂白液的有效成分为
②它的消毒原理是
③由以上反应证明
 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸④工业生产漂白粉的化学方程式为
(3)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8gNa2O2中阴离子的物质的量为
(4)将
 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为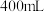 。试计算:
。试计算:①原混合物中
 的质量为
的质量为 。
。②所得溶液的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4 CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作
CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作___________ (填“氧化剂”或“还原剂”)。
(2)SO2能够使品红溶液褪色,体现了二氧化硫具有___________ 性。
(3)为了探究HClO的漂白性,某同学设计了如下的实验。
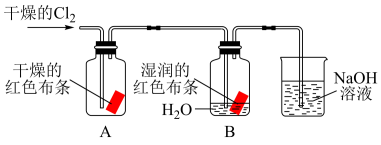
通入Cl2后,集气瓶A中的现象是___________ ,集气瓶B中湿润的红色布条的现象可得出的结论是___________ ,最后的NaOH装置中发生的主要化学方程式是___________ 。
(1)红热木炭与浓H2SO4反应的化学方程式是C+2H2SO4
 CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作
CO2↑+2SO2↑+2H2O,该反应中浓硫酸的作用是作(2)SO2能够使品红溶液褪色,体现了二氧化硫具有
(3)为了探究HClO的漂白性,某同学设计了如下的实验。

通入Cl2后,集气瓶A中的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。下列分别为钠和氯及 其化合物的“价-类”二维图,请回答下列问题:
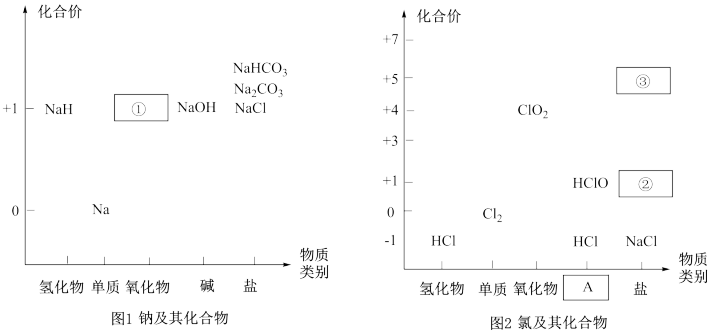
(1)填写二维图中缺失的化学式:①___________ 、②___________ 。
(2)物质③常用于实验室制取O2,则③的化学式是___________ 。
(3)从物质类别角度看,HClO 属于___________ ,一般能与下列___________ (填字母序号)类别 物质发生反应;
a.金属单质b.非金属单质c.酸性氧化物d.碱性氧化物e.酸f.碱g.盐
从化合价角度看,Cl2具有___________ 填“还原性”或“氧化性”或“既有氧化性又有还原性”), 已知 Cl2与H2O 反应,该反应的 离子方程式为___________ 。
(4)氢化钠(NaH)可在野外用作生氢剂,NaH 用作生氢剂时的化学反应原理为:NaH+H2O=NaOH+H2↑,NaH 做___________ (填“氧化剂”或“还原剂”)。
(5)二氧化氯(ClO2)是一种新型自来水消毒剂,用 ClO2代替 Cl2对饮用水进行消毒可避免产生对人体有害的有机氯化 合物。ClO2能杀死水中的病菌,起到消毒的作用,是因为 ClO2具有___________ (填“强还原性”或“强氧化性”)。

(1)填写二维图中缺失的化学式:①
(2)物质③常用于实验室制取O2,则③的化学式是
(3)从物质类别角度看,HClO 属于
a.金属单质b.非金属单质c.酸性氧化物d.碱性氧化物e.酸f.碱g.盐
从化合价角度看,Cl2具有
(4)氢化钠(NaH)可在野外用作生氢剂,NaH 用作生氢剂时的化学反应原理为:NaH+H2O=NaOH+H2↑,NaH 做
(5)二氧化氯(ClO2)是一种新型自来水消毒剂,用 ClO2代替 Cl2对饮用水进行消毒可避免产生对人体有害的有机氯化 合物。ClO2能杀死水中的病菌,起到消毒的作用,是因为 ClO2具有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气是氯碱工业的主要产品之一,是一种常用的消毒刹,其消毒原理是与水反应生成了次氯酸,次氯酸的强氧化性能杀死水中的病菌。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
(1)氯气与水反应的离子方程式为______________________________ 。
(2)将氯气通入淀粉 溶液中,溶液变蓝,写出反应的离子方程式
溶液中,溶液变蓝,写出反应的离子方程式____________________ ;继续通入氯气,蓝色消失,原因是: ,该反应体现了氯气的
,该反应体现了氯气的__________ 性。
(3)泳池用含氯物质消毒时,需要保证一定量的余氯,若水中的余氯以次氯酸形式存在,再加入 进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与
进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与 发生反应生成盐酸的化学方程式
发生反应生成盐酸的化学方程式____________________ 。
(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为_________________________ 。
(5)二氧化氯( )是国际上公认为安全、.无毒的绿色消毒剂。工业上制取
)是国际上公认为安全、.无毒的绿色消毒剂。工业上制取 的化学方程式如下:
的化学方程式如下: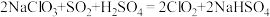 。按要求回答下列问题:
。按要求回答下列问题:
①该反应的离子方程式为____________________ 。
②另一种制备 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 与
与 的物质的量之比为
的物质的量之比为 ,则每生成
,则每生成 ,转移
,转移_________ 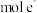 。
。
(1)氯气与水反应的离子方程式为
(2)将氯气通入淀粉
 溶液中,溶液变蓝,写出反应的离子方程式
溶液中,溶液变蓝,写出反应的离子方程式 ,该反应体现了氯气的
,该反应体现了氯气的(3)泳池用含氯物质消毒时,需要保证一定量的余氯,若水中的余氯以次氯酸形式存在,再加入
 进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与
进行消毒反而会导致藻类生长,池水变绿。写出次氯酸与 发生反应生成盐酸的化学方程式
发生反应生成盐酸的化学方程式(4)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为
(5)二氧化氯(
 )是国际上公认为安全、.无毒的绿色消毒剂。工业上制取
)是国际上公认为安全、.无毒的绿色消毒剂。工业上制取 的化学方程式如下:
的化学方程式如下: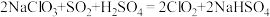 。按要求回答下列问题:
。按要求回答下列问题:①该反应的离子方程式为
②另一种制备
 的方法是用
的方法是用 与盐酸反应,同时有
与盐酸反应,同时有 生成,产物中
生成,产物中 与
与 的物质的量之比为
的物质的量之比为 ,则每生成
,则每生成 ,转移
,转移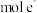 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是___________ (填写序号)。
(2)写出物质⑤在水中反应的离子方程式:___________ 。
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为___________ L,反应转移电子数为___________ (用NA表示),Na2O2中阴、阳离子个数比为___________ 。
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:___________ 。
现有以下物质:①石墨;②铝;③乙醇;④氨气;⑤液氯;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氢氧化钠固体。
(1)属于电解质的是
(2)写出物质⑤在水中反应的离子方程式:
(3)40.5g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,体积为11.2LCO2与足量Na2O2反应,生成气体的体积为
(5)已知P2O5为酸性氧化物,可与水反应生成磷酸(H3PO4),写出P2O5与足量NaOH溶液反应的离子方程式:
您最近一年使用:0次
【推荐1】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_______________________________ 。
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为____________ mol;产生“气泡”的化学方程式为__________________ 。
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是_____________________ (用离子方程式表示)。工业上是将氯气通入30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1 000 kg该溶液需消耗氯气的质量为________ kg(保留整数)。
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
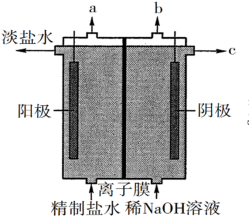
(1)氯气是制备系列含氯化合物的主要原料,可采用如图所示的装置来制取。装置中的离子膜只允许Na+离子通过,已知阳极发生氧化反应,则a口逸出的气体的分子式为_______ 。
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,请写出氯气与水反应生成HClO的离子方程式_______ 。
(3)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,5ClO +4H+=4ClO2+Cl-+2H2O,每生成1 mol ClO2消耗NaClO2的量为
+4H+=4ClO2+Cl-+2H2O,每生成1 mol ClO2消耗NaClO2的量为_______ mol;产生“气泡”的化学方程式为_______ 。
(4)“84消毒液”的有效成分为_______ ,不可与酸性清洁剂混用的原因是(用离子方程式表示)_______ 。
(5)工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为_______ kg(保留整数)。
(1)氯气是制备系列含氯化合物的主要原料,可采用如图所示的装置来制取。装置中的离子膜只允许Na+离子通过,已知阳极发生氧化反应,则a口逸出的气体的分子式为

(2)次氯酸为一元弱酸,具有漂白和杀菌作用,请写出氯气与水反应生成HClO的离子方程式
(3)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,5ClO
 +4H+=4ClO2+Cl-+2H2O,每生成1 mol ClO2消耗NaClO2的量为
+4H+=4ClO2+Cl-+2H2O,每生成1 mol ClO2消耗NaClO2的量为(4)“84消毒液”的有效成分为
(5)工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为
您最近一年使用:0次



