月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________ 。
(2)Na的原子结构示意图为______ 。
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为______ 。
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为_________ 、_________ (写化学式)。
(1)3He是高效核能原料,其原子核内中子数为
(2)Na的原子结构示意图为
(3)MgCl2在工业上应用广泛,可由MgO制备。
①月球上某矿石经处理得到的MgO中含有少量SiO2,用NaOH溶液除去SiO2的化学方程式为
②MgO与炭粉和氯气在一定条件下反应可制备MgCl2,尾气中的氯气可用足量冷的NaOH溶液完全吸收,则生成的盐为
更新时间:2018-03-13 09:20:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下(氯化过程中少量Ca(ClO)2分解为CaCl2和O2):
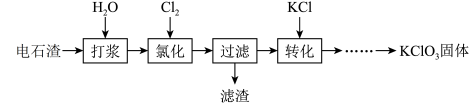
(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为__________________________________________________ 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________ (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为__________ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]________ 1∶5(填“>”、“<”或“=”)。

(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯是海水中含量最丰富的元素,氯的单质及其化合物在生成、生活领域应用广泛。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为_____________ (用离子方程式表示)。
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式_______ 。
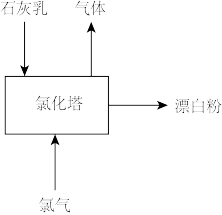
(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为_______ 。实际生产中,将石灰乳(含有3%~6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是_______ 。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成
 ,写出制备二氧化氯的离子方程式
,写出制备二氧化氯的离子方程式(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。生产漂白粉反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
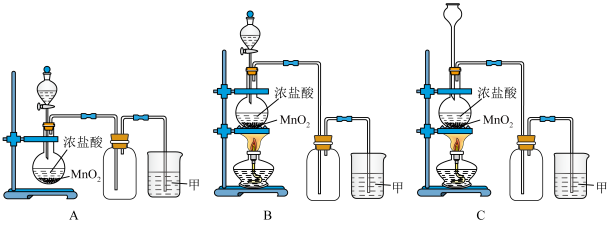
(1)A、B、C三套装置中,应选用的装置是___________ (选填“A”、“B”、“C”)。
(2)写出制取氯气的化学方程式___________ 。
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式___________ 。
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是___________ (用化学方程式说明)
(5)实验室也可用 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:___________ 。若反应中有5mol电子转移,被氧化HCl的的物质的量为___________ 。

(1)A、B、C三套装置中,应选用的装置是
(2)写出制取氯气的化学方程式
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是
(5)实验室也可用
 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如何用所提供的试剂和方法除去各混合物粉末中的杂质(括号内为杂质)?将所选答案的编号填入表中相应的空格内。(如果不需补加试剂,则对应答案栏可空着)可供选择的试剂:A.盐酸 B.NaOH溶液 C.O2 D.H2O E.CO2可供选择的操作:①分液 ②加热 ③高温灼烧 ④过滤 ⑤结晶
| 序号 | 粉末状混合物 | 所加试剂 | 主要操作 |
| (1) | SiO2(CaCO3) | ||
| (2) | CaCO3(SiO2) | ||
| (3) | NaCl(SiO2) | ||
| (4) | SiO2(Fe2O3) | ||
| (5) | SiO2(H2SiO3) | ||
| (6) | SiO2(Na2SO4) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列说法是否正确(正确的打“√”,不正确的打“×”),若不正确请说明理由。
(1)SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物___________ ,理由 ___________
(2)某气体通入品红溶液后,品红溶液褪色,则该气体一定是SO2___________ ,理由 ___________
(3)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性___________ ,理由 ___________
(4)王水是浓盐酸和浓硝酸体积比为3∶1的混合物,能溶解金和铂___________ ,理由______
(1)SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物
(2)某气体通入品红溶液后,品红溶液褪色,则该气体一定是SO2
(3)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性
(4)王水是浓盐酸和浓硝酸体积比为3∶1的混合物,能溶解金和铂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】天宫二号空间实验室已于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________ ,该物质的属于_______ 氧化物 ,实验室中不能用玻璃塞试剂瓶盛KOH溶液,原因是_________________________________ (用离子方程式表示)。
(2)联氨(N2H4,无色液体)可用作火箭燃料,其电子式为____________ 。
(3)太阳能电池帆板是“天宫二号”空间运行的动力湃泉。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光认太阳能电池,该电池的核心材料是___________ ,其能量转化方式为____________________ 。
(4)下面是一个还原过程的反应式:NO3﹣+4H++3e﹣→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生.
①写出并配平该氧化还原反应的方程式:_________________________________
②反应中若产生0.2mol气体,则转移电子的物质的量是___ mol.
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)联氨(N2H4,无色液体)可用作火箭燃料,其电子式为
(3)太阳能电池帆板是“天宫二号”空间运行的动力湃泉。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光认太阳能电池,该电池的核心材料是
(4)下面是一个还原过程的反应式:NO3﹣+4H++3e﹣→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生.
①写出并配平该氧化还原反应的方程式:
②反应中若产生0.2mol气体,则转移电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Na、Fe、Al是中学化学常见的金属元素。回答下列问题:
(1)焰色反应的实验中,Na元素燃烧时的焰色为_______ 色,观察K元素燃烧时的焰色需要透过_______ 。
(2)碘元素的一种核素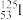 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为_______ ,中子数为_______ ,质量数为_______ ,核外电子数为_______ 。(对应数值125和53)
(1)焰色反应的实验中,Na元素燃烧时的焰色为
(2)碘元素的一种核素
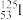 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】判断正误:
1.任何原子或离子的组成中都含有质子_________
2.元素原子的多样性是由构成原子的质子和中子数目引起的_________
3.元素的化学性质主要取决于元素原子的最外层电子数_________
4.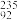 U和
U和 U是同位素,核反应属于化学变化
U是同位素,核反应属于化学变化_________
5.2H+核外电子数为2_________
6.两种粒子,若核外电子排布完全相同,则其化学性质一定相同_________
7.一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子_________
8.核聚变如 H+
H+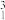 H→
H→ He+
He+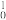 n,因为有新微粒生成,所以该变化是化学变化
n,因为有新微粒生成,所以该变化是化学变化_________
9. Cl与
Cl与 Cl得电子能力几乎相同
Cl得电子能力几乎相同_________
10.一种核素只有一种质量数_________
11.最外层电子数为8的粒子一定是稀有气体元素原子_________
12.核外电子排布相同的微粒化学性质也相同_________
13.40K和40Ca原子中的质子数和中子数都相等_________
14.某元素的原子最外层只有一个电子,则它一定是金属元素_________
15.同位素的不同核素的物理、化学性质完全相同_________
16.当原子形成简单离子后,其最外层上的电子数可超过8个_________
17.原子最外层上的电子数少于4个时,电子数越多,还原性越强_________
18.原子核外电子中,最外层上的电子能量最高_________
19.当最外层上的电子数变为4个时即达稳定结构_________
20.若两种不同的核素具有相同的中子数,则二者一定不属于同种元素___________
1.任何原子或离子的组成中都含有质子
2.元素原子的多样性是由构成原子的质子和中子数目引起的
3.元素的化学性质主要取决于元素原子的最外层电子数
4.
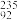 U和
U和 U是同位素,核反应属于化学变化
U是同位素,核反应属于化学变化5.2H+核外电子数为2
6.两种粒子,若核外电子排布完全相同,则其化学性质一定相同
7.一种元素可以有多种核素,也可能只有一种核素,有多少种核素就有多少种原子
8.核聚变如
 H+
H+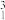 H→
H→ He+
He+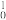 n,因为有新微粒生成,所以该变化是化学变化
n,因为有新微粒生成,所以该变化是化学变化9.
 Cl与
Cl与 Cl得电子能力几乎相同
Cl得电子能力几乎相同10.一种核素只有一种质量数
11.最外层电子数为8的粒子一定是稀有气体元素原子
12.核外电子排布相同的微粒化学性质也相同
13.40K和40Ca原子中的质子数和中子数都相等
14.某元素的原子最外层只有一个电子,则它一定是金属元素
15.同位素的不同核素的物理、化学性质完全相同
16.当原子形成简单离子后,其最外层上的电子数可超过8个
17.原子最外层上的电子数少于4个时,电子数越多,还原性越强
18.原子核外电子中,最外层上的电子能量最高
19.当最外层上的电子数变为4个时即达稳定结构
20.若两种不同的核素具有相同的中子数,则二者一定不属于同种元素
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)按 X(X为元素符号)格式写出含有8个质子、10个中子的原子的化学符号:
X(X为元素符号)格式写出含有8个质子、10个中子的原子的化学符号:_________ 。
(2)根据下列微粒回答问题: H、
H、 H、
H、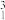 H、14C、14N、16O、35Cl2、37Cl2。
H、14C、14N、16O、35Cl2、37Cl2。
①以上8种微粒共有________ 种核素,共________ 种元素。
②互为同位素的是________ 。
③质量数相等的是________ 和________ ,中子数相等的是________ 和________ 。
(3)相同物质的量的14CO2与S18O2的质量之比为________ ;电子数之比为________ 。
 X(X为元素符号)格式写出含有8个质子、10个中子的原子的化学符号:
X(X为元素符号)格式写出含有8个质子、10个中子的原子的化学符号:(2)根据下列微粒回答问题:
 H、
H、 H、
H、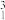 H、14C、14N、16O、35Cl2、37Cl2。
H、14C、14N、16O、35Cl2、37Cl2。①以上8种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的14CO2与S18O2的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)用A质子数,B中子数,C核外电子数,D最外层电子数,用序号回答下列问题。
①原子种类由______ 决定;
②元素种类由______ 决定;
③元素的化合价由______ 决定。
(2)2.0g由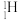 和
和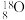 构成的水
构成的水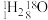 ,该水分子的物质的量为
,该水分子的物质的量为______ ,含中子数为______ 。
(3)核内中子数为N的 ,质量数为A,则该离子的核外电子数为
,质量数为A,则该离子的核外电子数为______ 。
①原子种类由
②元素种类由
③元素的化合价由
(2)2.0g由
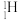 和
和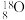 构成的水
构成的水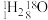 ,该水分子的物质的量为
,该水分子的物质的量为(3)核内中子数为N的
 ,质量数为A,则该离子的核外电子数为
,质量数为A,则该离子的核外电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将某文献资料上记载的相对原子质量数据摘录如下:
试完成下列问题:
(1)34.969是表示___________ ;
(2)35.453是表示___________ ;
(3)35是表示___________ ;
(4)35.485是表示___________ ;
(5)24.23%是表示___________ ;
(6)列出求算35.453的算式___________ ;
(7)列出求算35.485的算式___________ 。
| 35Cl | 34.969 | 75.77% | 35Cl | 35 | 75.77% |
| 37Cl | 36.966 | 24.23% | 37Cl | 37 | 24.23% |
| 平均 | 35.453 | 平均 | 35.485 | ||
试完成下列问题:
(1)34.969是表示
(2)35.453是表示
(3)35是表示
(4)35.485是表示
(5)24.23%是表示
(6)列出求算35.453的算式
(7)列出求算35.485的算式
您最近一年使用:0次



