以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下(氯化过程中少量Ca(ClO)2分解为CaCl2和O2):
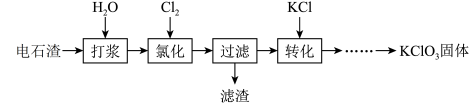
(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为__________________________________________________ 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________ (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为__________ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]________ 1∶5(填“>”、“<”或“=”)。

(1)氯化过程控制电石渣过量、在75 ℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2。
①生成Ca(ClO)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。请回答:
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] :n[CaCl2]
更新时间:2019-03-28 10:47:05
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某些化学反应可用下式表示:A+B→C+D+H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:________________________________________________________________________ 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是____________________ 。
(3)若A为Na2O2,B为硫酸,则C和D的化学式是________________ 。
(4)若A、C均含有铝元素。
①当B是盐酸时,C是__________________ 。
②当B是NaOH时,C是________________ 。
(5)若A为单质,B为第2周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式:________________________________________________ (写出两个反应)。
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是
(3)若A为Na2O2,B为硫酸,则C和D的化学式是
(4)若A、C均含有铝元素。
①当B是盐酸时,C是
②当B是NaOH时,C是
(5)若A为单质,B为第2周期某种元素的最高价氧化物的水化物,请写出符合上式的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__ ,自然界中存在的54Fe和56Fe,它们互称为___ 。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__ 。通常证明某溶液中含Fe2+的化学方法是___ 。
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__ 相同。处于同一列的N和P位于元素周期表的__ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_ ,其气态氢化物的结构式为__ 。
②与硅元素处于同一周期,两性金属元素是__ ,并写出其在元素周期表中的位置:第__ 周期,__ 族,该元素的最高价氧化物对应水化物的电离方程式为__ 。
③第三周期半径最大的金属元素__ ,该元素形成氢氧化物的电子式_ ,检验物质中是否含有该元素的方法是:__ 。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__ (写化学式)。该元素与硫元素相比,非金属性较强的元素是__ (填元素符号),请写出证明该结论的一个实验事实:__ 。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___ 。

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__ 族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__ 。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②与硅元素处于同一周期,两性金属元素是
③第三周期半径最大的金属元素
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究化学反应速率和限度对促进生产具有重要的意义。
(1)某同学为探究锌与盐酸反应,取同质量、同体积的锌片,同浓度盐酸做了下列实验:
实验一:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如下图所示:

实验二:在盐酸中滴入几滴CuSO4溶液,发现生成氢气速率明显比实验一要快。
①在上图中t1~t2速率变化的主要原因是_______ ;t2~t3速率变化的主要原因是_______ 。
②用离子程式表示实验二反应速率加快原因_______ 。
(2)工业有一种方法是利用CO2制取甲醇,CO2(g)+3H2(g) CH3OH(g)+H2O(g)在体积为1L的密闭容器中,充入1molCO2和3molH2,在一定条件下发生反应,测得X和Y两种物质物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)在体积为1L的密闭容器中,充入1molCO2和3molH2,在一定条件下发生反应,测得X和Y两种物质物质的量随时间变化如图。请回答:

①X代表的物质的化学式为_______ 。
②从反应开始到平衡,氢气的平均反应速率:v(H2) =_______ ,CO2的转化率α(CO2) =_______ 。
③能够说明该反应已达到平衡的是_______ 。
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3molH2的同时生成1molCH3OH
E.有2个C=O键断裂的同时,有3个H-H键生成
(1)某同学为探究锌与盐酸反应,取同质量、同体积的锌片,同浓度盐酸做了下列实验:
实验一:把纯锌片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如下图所示:

实验二:在盐酸中滴入几滴CuSO4溶液,发现生成氢气速率明显比实验一要快。
①在上图中t1~t2速率变化的主要原因是
②用离子程式表示实验二反应速率加快原因
(2)工业有一种方法是利用CO2制取甲醇,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)在体积为1L的密闭容器中,充入1molCO2和3molH2,在一定条件下发生反应,测得X和Y两种物质物质的量随时间变化如图。请回答:
CH3OH(g)+H2O(g)在体积为1L的密闭容器中,充入1molCO2和3molH2,在一定条件下发生反应,测得X和Y两种物质物质的量随时间变化如图。请回答:
①X代表的物质的化学式为
②从反应开始到平衡,氢气的平均反应速率:v(H2) =
③能够说明该反应已达到平衡的是
A.恒温、恒容时,容器内的压强不再变化
B.恒温、恒容时,容器内混合气体的密度不再变化
C.一定条件下,CO2、H2和CH3OH的浓度不再变化
D.一定条件下,单位时间内消耗3molH2的同时生成1molCH3OH
E.有2个C=O键断裂的同时,有3个H-H键生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列方程式的书写
(1) 溶液显碱性的离子方程式
溶液显碱性的离子方程式_______
(2)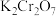 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式_______
(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式_______
(4)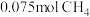 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
(1)
 溶液显碱性的离子方程式
溶液显碱性的离子方程式(2)
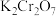 溶液中存在的化学平衡的离子方程式
溶液中存在的化学平衡的离子方程式(3)硫代硫酸钠溶液与稀硫酸反应的化学方程式
(4)
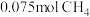 在常温常压下完全燃烧放出66kJ的热量,写出
在常温常压下完全燃烧放出66kJ的热量,写出 燃烧热的热化学方程式
燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有室温下浓度均为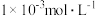 的几种溶液:①盐酸、②硫酸、③醋酸、④氨水、⑤
的几种溶液:①盐酸、②硫酸、③醋酸、④氨水、⑤ 溶液。回答下列问题:
溶液。回答下列问题:
(1)上述5种溶液中,水电离出的 最小的是
最小的是___________ 。(填序号,下同)
(2)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为___________ ,最终产生 总量的关系为
总量的关系为___________ 。
(3)现有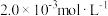 的
的 溶液,调节溶液
溶液,调节溶液 ,测得25℃时平衡体系中
,测得25℃时平衡体系中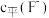 、
、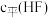 与溶液
与溶液 的关系如图所示:
的关系如图所示:
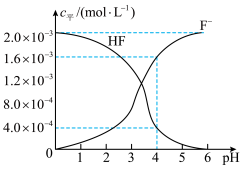
25℃时, 的电离平衡常数
的电离平衡常数
___________ 。
(4)在一定温度下,用水缓慢稀释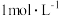 氨水的过程中,溶液中随着水量的增加,
氨水的过程中,溶液中随着水量的增加,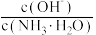
___________ (填“增大“减小”或“不变”,下同),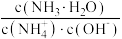
___________ 。
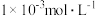 的几种溶液:①盐酸、②硫酸、③醋酸、④氨水、⑤
的几种溶液:①盐酸、②硫酸、③醋酸、④氨水、⑤ 溶液。回答下列问题:
溶液。回答下列问题:(1)上述5种溶液中,水电离出的
 最小的是
最小的是(2)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为
 总量的关系为
总量的关系为(3)现有
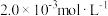 的
的 溶液,调节溶液
溶液,调节溶液 ,测得25℃时平衡体系中
,测得25℃时平衡体系中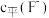 、
、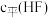 与溶液
与溶液 的关系如图所示:
的关系如图所示:
25℃时,
 的电离平衡常数
的电离平衡常数
(4)在一定温度下,用水缓慢稀释
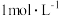 氨水的过程中,溶液中随着水量的增加,
氨水的过程中,溶液中随着水量的增加,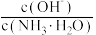
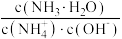
您最近一年使用:0次



