如何用所提供的试剂和方法除去各混合物粉末中的杂质(括号内为杂质)?将所选答案的编号填入表中相应的空格内。(如果不需补加试剂,则对应答案栏可空着)可供选择的试剂:A.盐酸 B.NaOH溶液 C.O2 D.H2O E.CO2可供选择的操作:①分液 ②加热 ③高温灼烧 ④过滤 ⑤结晶
| 序号 | 粉末状混合物 | 所加试剂 | 主要操作 |
| (1) | SiO2(CaCO3) | ||
| (2) | CaCO3(SiO2) | ||
| (3) | NaCl(SiO2) | ||
| (4) | SiO2(Fe2O3) | ||
| (5) | SiO2(H2SiO3) | ||
| (6) | SiO2(Na2SO4) |
2016高一·全国·课时练习 查看更多[5]
(已下线)同步君 必修1 第4章 第1节 二氧化硅和硅酸高中化学人教版 必修1 第四章 非金属及其化合物 1.无机非金属材料的主角——硅 二氧化硅和硅酸(已下线)2018年11月14日——《每日一题》人教必修1-二氧化硅的性质(已下线)2019年11月13日 《每日一题》化学人教版(必修1)——二氧化硅的性质湖南省株洲市第二中学2022-2023学年高一下学期第一次月考化学试题
更新时间:2017-11-27 16:00:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】月球含有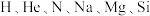 等元素,是人类未来的资源宝库。
等元素,是人类未来的资源宝库。
(1)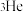 是高效核能原料,其原子核内中子数为
是高效核能原料,其原子核内中子数为_______ 。
(2) 的原子结构示意图为
的原子结构示意图为_______ , 在氧气中完全燃烧所得产物的电子式为
在氧气中完全燃烧所得产物的电子式为_______ 。
(3) 在工业上应用广泛,可由
在工业上应用广泛,可由 制备。
制备。
①月球上某矿石经处理得到的 中含有少量
中含有少量 ,除去
,除去 的离子方程式为
的离子方程式为_______ 。
② 与炭粉和氯气在一定条件下反应可制备
与炭粉和氯气在一定条件下反应可制备 。若尾气可用足量
。若尾气可用足量 溶液完全吸收,则生成的盐为
溶液完全吸收,则生成的盐为_______ (写化学式)。
(4)月球土壤中含有丰富的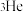 ,从月球土壤中提炼
,从月球土壤中提炼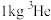 ,同时可得
,同时可得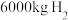 和
和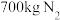 。以所得
。以所得 和
和 为原料经一系列反应最多可生产碳酸氢铵
为原料经一系列反应最多可生产碳酸氢铵_______  。
。
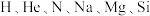 等元素,是人类未来的资源宝库。
等元素,是人类未来的资源宝库。(1)
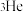 是高效核能原料,其原子核内中子数为
是高效核能原料,其原子核内中子数为(2)
 的原子结构示意图为
的原子结构示意图为 在氧气中完全燃烧所得产物的电子式为
在氧气中完全燃烧所得产物的电子式为(3)
 在工业上应用广泛,可由
在工业上应用广泛,可由 制备。
制备。①月球上某矿石经处理得到的
 中含有少量
中含有少量 ,除去
,除去 的离子方程式为
的离子方程式为②
 与炭粉和氯气在一定条件下反应可制备
与炭粉和氯气在一定条件下反应可制备 。若尾气可用足量
。若尾气可用足量 溶液完全吸收,则生成的盐为
溶液完全吸收,则生成的盐为(4)月球土壤中含有丰富的
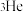 ,从月球土壤中提炼
,从月球土壤中提炼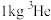 ,同时可得
,同时可得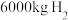 和
和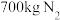 。以所得
。以所得 和
和 为原料经一系列反应最多可生产碳酸氢铵
为原料经一系列反应最多可生产碳酸氢铵 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)普通玻璃又称为钠玻璃,试写出生产普通玻璃过程中发生反应的一个化学方程式:____________ 。
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):_________ ;玻璃试剂瓶不能盛放氢氟酸的原因是(用化学方程式表示):______________________________________ 。
(3)有一种特殊玻璃为钾玻璃,其热膨胀系数较小,较难熔化,较难受化学药品的侵蚀,可用于制作一般的化学仪器。现以石英砂、苛性钾、熟石灰为原料,熔制钾玻璃,质量比为75:28:37(假定这些原料不含杂质),试用氧化物的形式表示该钾玻璃的组成____________________________ 。
(4)下列叙述正确的是_________________________ 。
①SO2、NO、NO2都是形成酸雨的因素,都能和水反应生成酸
②NH3、H2S均不能用浓硫酸干燥
③水晶的主要成分是SiO2
④SiO2与CO2都属于酸性氧化物,都不能与酸反应
⑤实验室可用NaOH溶液处理Cl2和SO2废气
⑥NO只能用排水集气法收集,不能用排空气法收集;而NO2只能用排空气法收集,不能用排水集气法
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):
(3)有一种特殊玻璃为钾玻璃,其热膨胀系数较小,较难熔化,较难受化学药品的侵蚀,可用于制作一般的化学仪器。现以石英砂、苛性钾、熟石灰为原料,熔制钾玻璃,质量比为75:28:37(假定这些原料不含杂质),试用氧化物的形式表示该钾玻璃的组成
(4)下列叙述正确的是
①SO2、NO、NO2都是形成酸雨的因素,都能和水反应生成酸
②NH3、H2S均不能用浓硫酸干燥
③水晶的主要成分是SiO2
④SiO2与CO2都属于酸性氧化物,都不能与酸反应
⑤实验室可用NaOH溶液处理Cl2和SO2废气
⑥NO只能用排水集气法收集,不能用排空气法收集;而NO2只能用排空气法收集,不能用排水集气法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】非金属元素在化工生产中扮演着重要角色。其中硅是无机非金属材料的重要组成元素;在众多的化工原料和产品中,都能见到氮元素的踪迹。
I.回答下列问题:
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是______ (填序号)。
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:_______ 。
②熔化烧碱应选用的坩埚为______ (填字母)。
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
II.某化学小组模拟工业生产制取HNO3,设计了如图所示装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置E中主要反应的化学方程式为_______ 。
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式______ 。
(5)装置C中浓硫酸的主要作用是______ 。
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:
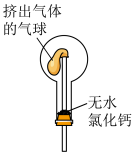
①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是______ 。由此,该同学得出结论:不能用CaCl2代替碱石灰。
I.回答下列问题:
(1)硅酸盐具有特殊的性质与应用,回答下列问题:硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃 ②陶瓷 ③水晶 ④硅芯片 ⑤光导纤维 ⑥水泥 ⑦砖瓦
(2)SiO2是一种酸性氧化物。
①用化学方程式表示盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:
②熔化烧碱应选用的坩埚为
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
II.某化学小组模拟工业生产制取HNO3,设计了如图所示装置,其中a为一个可持续鼓入空气的橡皮球。

(3)装置E中主要反应的化学方程式为
(4)F装置用浓NaOH溶液吸收NO2,生成物之一是NaNO2,请写出该反应的离子方程式
(5)装置C中浓硫酸的主要作用是
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证,实验步骤如图:

①用烧瓶收集满干燥的氨气,立即塞如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.某校化学一兴趣小组在社会实践活动中,考察了当地某工厂的废水(无色)处理流程,并取该厂未经处理的废水样品进行实验分析。

已知: 固体难溶于硝酸。
固体难溶于硝酸。
(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈_______ (填“酸性”或“碱性”),说明废水中含有较大量的_______ (填离子符号),建议该厂用_______ (填化学式)处理废水。
(2)另取少量废水,滴加适量 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是_______ ,其离子反应方程式为_______ 。
(3)已知该工厂废水中除含有以上离子外,还含有较多的 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是_______ ;随试剂的滴加,试管中出现的现象是_______ ,该反应的离子方程式为_______ 。
Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的_______
(5)向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。

已知:
 固体难溶于硝酸。
固体难溶于硝酸。(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈
(2)另取少量废水,滴加适量
 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是(3)已知该工厂废水中除含有以上离子外,还含有较多的
 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的
(5)向
 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2020 年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出新制氯水中,具有氧化性的含氯微粒有_______ ;
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4 +16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑+8H2O,15.8 g KMnO4能和_______ mol HCl发生上述反应、产生的Cl2在标准状况下的体积为_______ L;
③实验室还可以利用如下反应制取氯气:KClO3 + 6HCl(浓) = KCl + 3Cl2↑ + 3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为_______ mol;
(2)常温下,氯气与消石灰浊液反应得漂白精,Ca(ClO)2是漂白精的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入漂白精在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:_______ ;
(3)根据如图的溶解度曲线,回答下列问题。
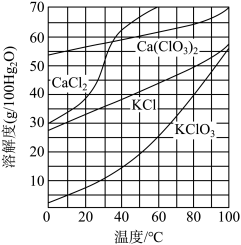
①向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出,若溶液中KClO3的含量为100 g·L-1,从该溶液中得到KClO3固体的方法是_______ 。
② KClO3与SO2在强酸性条件下可反应制得ClO2,SO2被氧化为SO ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(1)①写出新制氯水中,具有氧化性的含氯微粒有
②已知KMnO4与浓盐酸反应的化学方程式如下,该反应也可以用来制取氯气:2KMnO4 +16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑+8H2O,15.8 g KMnO4能和
③实验室还可以利用如下反应制取氯气:KClO3 + 6HCl(浓) = KCl + 3Cl2↑ + 3H2O。若制取标准状况下6.72 L氯气,反应过程中转移电子的物质的量为
(2)常温下,氯气与消石灰浊液反应得漂白精,Ca(ClO)2是漂白精的有效成分,在此次抗击新冠病毒中发挥了重要作用 ,浸泡衣物时加入漂白精在空气中放置一段时间漂白效果更好,原因用化学方程式表示为:
(3)根据如图的溶解度曲线,回答下列问题。

①向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出,若溶液中KClO3的含量为100 g·L-1,从该溶液中得到KClO3固体的方法是
② KClO3与SO2在强酸性条件下可反应制得ClO2,SO2被氧化为SO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】以硅藻土(主要成分为SiO2,含有少量的Fe2O3、 Al2O3) 为载体的V2O5-K2SO4常用作接触法制硫酸的催化剂。以下是一种废钒催化剂综合回收利用的工艺路线。
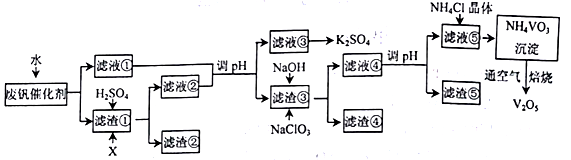
已知: 废钒催化剂中钒元素主要以VOSO4和V2O5形式存在;
V2O5是两性氧化物,不溶于水,溶于酸生成VO2+,溶于碱生成VO3-;
VOSO4是强电解质,溶于水电离出VO2+。
回答下列问题:
(1)VOSO4中V 元素的化合价为___________ 。
(2)滤渣①酸溶后加入的最佳试剂X 为_________ 。
a.NaClO b.Na2SO3c.K2SO3d.K2S
(3)从滤液③中得到产品K2SO4的操作为_________ 。滤渣③除含有V2O2(OH)4,还含有_________ 。
(4)若滤液⑤中c(VO3-)=0.1mol·L-1,为使钒元素的沉淀率达到98%,至少应调节c(NH4+)为_________ [Ksp(NH4VO3)=1.6×10-3]。
(5)“焙烧”时通入足量的空气,反应后的尾气可以直接排放。该反应的化学方程式为____________ 。
(6) V2O5纯度测定原理: 称取V2O5产品ag,先加入硫酸将V2O5转化为VO2+,再加入V1 mLc1mol·L-1(NH4) 2Fe(SO4) 2溶液将VO2+转 化为VO2+,最 后 用c2mol·L-1KMnO4 溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液V2mL。假设杂质不参与反应,实验测得某V2O5产品的纯度为91%,则理论上加入(NH4)2Fe(SO4)2溶液的体积V1至少_________ mL (用相关字母表示)。

已知: 废钒催化剂中钒元素主要以VOSO4和V2O5形式存在;
V2O5是两性氧化物,不溶于水,溶于酸生成VO2+,溶于碱生成VO3-;
VOSO4是强电解质,溶于水电离出VO2+。
回答下列问题:
(1)VOSO4中V 元素的化合价为
(2)滤渣①酸溶后加入的最佳试剂X 为
a.NaClO b.Na2SO3c.K2SO3d.K2S
(3)从滤液③中得到产品K2SO4的操作为
(4)若滤液⑤中c(VO3-)=0.1mol·L-1,为使钒元素的沉淀率达到98%,至少应调节c(NH4+)为
(5)“焙烧”时通入足量的空气,反应后的尾气可以直接排放。该反应的化学方程式为
(6) V2O5纯度测定原理: 称取V2O5产品ag,先加入硫酸将V2O5转化为VO2+,再加入V1 mLc1mol·L-1(NH4) 2Fe(SO4) 2溶液将VO2+转 化为VO2+,最 后 用c2mol·L-1KMnO4 溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液V2mL。假设杂质不参与反应,实验测得某V2O5产品的纯度为91%,则理论上加入(NH4)2Fe(SO4)2溶液的体积V1至少
您最近一年使用:0次



