天宫二号空间实验室已于2016年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是___________ ,该物质的属于_______ 氧化物 ,实验室中不能用玻璃塞试剂瓶盛KOH溶液,原因是_________________________________ (用离子方程式表示)。
(2)联氨(N2H4,无色液体)可用作火箭燃料,其电子式为____________ 。
(3)太阳能电池帆板是“天宫二号”空间运行的动力湃泉。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光认太阳能电池,该电池的核心材料是___________ ,其能量转化方式为____________________ 。
(4)下面是一个还原过程的反应式:NO3﹣+4H++3e﹣→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生.
①写出并配平该氧化还原反应的方程式:_________________________________
②反应中若产生0.2mol气体,则转移电子的物质的量是___ mol.
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是
(2)联氨(N2H4,无色液体)可用作火箭燃料,其电子式为
(3)太阳能电池帆板是“天宫二号”空间运行的动力湃泉。其性能直接影响到“天宫二号”的运行寿命和可靠性。天宫二号使用的光认太阳能电池,该电池的核心材料是
(4)下面是一个还原过程的反应式:NO3﹣+4H++3e﹣→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生.
①写出并配平该氧化还原反应的方程式:
②反应中若产生0.2mol气体,则转移电子的物质的量是
更新时间:2019/09/18 16:59:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】 (1)1971年美国的斯图杰尔和阿佩里曼在0℃ 以下将氟气从细冰末上通过,成功地合成了一直认为不存在的氟的含氧酸——次氟酸。
①写出次氟酸的结构并标出各元素的化合价__________________ ;
②次氟酸刹那间被热水分解得到既可表现氧化性(对NaI)又可表现还原性(对KMnO4)的溶液,写出次氟酸分解反应的化学方程式:____________________________ 。
(2) 氰(CN)2的化学性质与卤素(X2)很相似称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。氰的氧化性比溴弱、比碘强。
①HCN分子中含有4个共价键,写出HCN的结构式:_______ ;
②下列有关方程式不正确的是____________ 。
A.(CN)2+2NaOH===NaCN+NaCNO+H2O
B.MnO2+4HCN===Mn(CN)2+(CN)2+2H2O
C.I2+2KCN===2KI+(CN)2
D.向NaBr(aq)和KCN(aq)中加入少量Cl2:Cl2+2NaBr===2NaCl+Br2
①写出次氟酸的结构并标出各元素的化合价
②次氟酸刹那间被热水分解得到既可表现氧化性(对NaI)又可表现还原性(对KMnO4)的溶液,写出次氟酸分解反应的化学方程式:
(2) 氰(CN)2的化学性质与卤素(X2)很相似称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。氰的氧化性比溴弱、比碘强。
①HCN分子中含有4个共价键,写出HCN的结构式:
②下列有关方程式不正确的是
A.(CN)2+2NaOH===NaCN+NaCNO+H2O
B.MnO2+4HCN===Mn(CN)2+(CN)2+2H2O
C.I2+2KCN===2KI+(CN)2
D.向NaBr(aq)和KCN(aq)中加入少量Cl2:Cl2+2NaBr===2NaCl+Br2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分别写出乙醇的电子式、结构式、结构简式_____________ ,_____________ ,_____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室加热液体时,常加入沸石、其主要成分为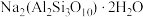 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:
(1)指出 元素在周期表中的位置
元素在周期表中的位置_______ 。
(2)沸石中的元素可形成多种化合物; 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式),化合物乙中存在的化学键类型为_______ 。
(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是_______ (填化学式)。
(4)已知硅酸(H2SiO3)为白色胶状沉淀。
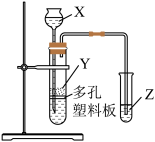
实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为_______ 、_______ 、_______ (填序号)。但有同学认为该实验所得现象无法充分证明C、Si的非金属性强弱,如何改进?_______ 。
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
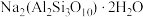 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:(1)指出
 元素在周期表中的位置
元素在周期表中的位置(2)沸石中的元素可形成多种化合物;
 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是
(4)已知硅酸(H2SiO3)为白色胶状沉淀。

实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列物质:① 溶液;②铁;③稀硫酸;④二氧化碳;⑤
溶液;②铁;③稀硫酸;④二氧化碳;⑤ 固体;⑥熔融
固体;⑥熔融 ;⑦
;⑦ 胶体;⑧蔗糖溶液。
胶体;⑧蔗糖溶液。
(1)将上述物质的序号填写在表格的空白处:
(2)某学习小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。
[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示:
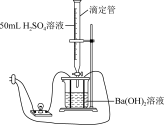
[实验过程与记录]
(3)写出下列情况发生反应的离子方程式:向 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性___________ ,继续滴加 溶液
溶液___________ 。
(4) 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
①请将湿法制备高铁酸钠的离子方程式配平:______
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________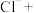 ___________
___________ 。
。
②干法制备高铁酸钠的化学方程式: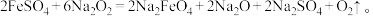 该反应中的氧化产物是
该反应中的氧化产物是___________ (填化学式)。生成 ,转移电子数目为
,转移电子数目为___________ 。
 溶液;②铁;③稀硫酸;④二氧化碳;⑤
溶液;②铁;③稀硫酸;④二氧化碳;⑤ 固体;⑥熔融
固体;⑥熔融 ;⑦
;⑦ 胶体;⑧蔗糖溶液。
胶体;⑧蔗糖溶液。(1)将上述物质的序号填写在表格的空白处:
| 分类标准 | 能导电的纯净物 | 电解质 |
| 属于该类的物质 |
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示:

[实验过程与记录]
| 实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入 的 的 溶液,逐滴滴加 溶液,逐滴滴加 的 的 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 | ① | ② 溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性 溶液
溶液(4)
 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:①请将湿法制备高铁酸钠的离子方程式配平:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________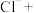 ___________
___________ 。
。②干法制备高铁酸钠的化学方程式:
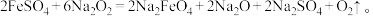 该反应中的氧化产物是
该反应中的氧化产物是 ,转移电子数目为
,转移电子数目为
您最近一年使用:0次
【推荐2】已知:(1)实验室制取Cl2的方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,其中MnO2发生了
MnCl2+Cl2↑+2H2O,其中MnO2发生了__ 反应,是__ 剂;每4分子氯化氢中只有___ 分子发生了___ 反应,盐酸是___ 剂。
(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,请在上式中用单线桥法表示出不同元素的原子间得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2跟HCl反应也能制得氯气,其化学方程式:4HCl+O2 2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是
2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是__ ;比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为___ 。
 MnCl2+Cl2↑+2H2O,其中MnO2发生了
MnCl2+Cl2↑+2H2O,其中MnO2发生了(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,请在上式中用单线桥法表示出不同元素的原子间得失电子的情况。
(3)用CuCl2作催化剂,在450℃时用空气中的O2跟HCl反应也能制得氯气,其化学方程式:4HCl+O2
 2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是
2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)工业上常以氨气为原料制备硝酸,其中有一步非常重要的反应为
4NH3+5O2 4NO+6H2O,该反应的氧化剂为
4NO+6H2O,该反应的氧化剂为______ ,还原剂为______ 。用单线桥法表示该氧化还原反应电子转移的方向和数目____________________________________ 。
若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为__________________ (写出含n、V的表达式)。
(2)某一反应体系中有反应物和生成物共5种物质:S、 H2S、HNO3、NO、H2O。已知硝酸是一种反应物,该反应中还原产物是________ ;若反应中转移了0.3mol电子,则氧化产物的质量是_____ g。
(3)按要求填空:
①除去碳酸氢钠溶液中的碳酸钠______________________ (用离子方程式表示原理);
②除去碳酸钠溶液中的碳酸氢钠,应加试剂为________________ ;
③用氢氧化钡除去明矾溶液中的硫酸根__________________ (用离子方程式表示原理)。
4NH3+5O2
 4NO+6H2O,该反应的氧化剂为
4NO+6H2O,该反应的氧化剂为若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏伽德罗常数(NA)可表示为
(2)某一反应体系中有反应物和生成物共5种物质:S、 H2S、HNO3、NO、H2O。已知硝酸是一种反应物,该反应中还原产物是
(3)按要求填空:
①除去碳酸氢钠溶液中的碳酸钠
②除去碳酸钠溶液中的碳酸氢钠,应加试剂为
③用氢氧化钡除去明矾溶液中的硫酸根
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】无机非金属材料与人类社会的发展与进步息息相关,硅元素更是无机非金属材料的主角,地壳质量的90%以上是二氧化硅和硅酸盐。回答下列问题:
(1)烧制普通玻璃的原料是纯碱、石灰石和石英砂,它们在玻璃窑中发生化学变化生成CaSiO3和Na2SiO3的化学方程式为___________ 、___________ 。
(2)工业上可利用水玻璃和盐酸反应制备硅酸凝胶后,进一步脱水处理可得到硅胶,请设计实验验证水玻璃与盐酸反应产生少量硅酸时,形成的分散系属于胶体:___________ (写出实验操作、现象和结论)。
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=___________ 。
(4)高纯度单晶硅可以按下列方法制备:
SiO2 Si(粗)
Si(粗) SiHCl3
SiHCl3 高纯度单晶硅
高纯度单晶硅
①写出SiO2转化为Si(粗)的化学方程式:___________ 。
②SiHCl3被H2还原为Si(纯)的基本反应类型为___________ 。
③写出高纯度单晶硅在信息技术或新能源技术等领域的应用:___________ (任写一种)。
(5)SiO2属于___________ 氧化物,试用任一离子方程式说明___________ 。
(6)向盐酸中逐滴滴加制得的硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在5~100nm的SiO2·nH2O粒子。该分散系属于___________ (选填“溶液”“浊液”或“胶体”),可以通过___________ 来鉴别。
(7)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是___________ (填序号)。
①玻璃②石英玻璃③陶瓷④硅芯片⑤砖瓦⑥水泥⑦光导纤维
(8)0.1mol 与0.05mol
与0.05mol 在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体___________ L。
(9)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[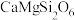 ]和橄榄石[
]和橄榄石[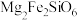 ])等,则辉石[
])等,则辉石[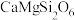 ]的氧化物形式可表示为
]的氧化物形式可表示为___________ ,斜长石[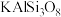 ]
]___________ (填“难”或“易”)溶于水,1mol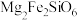 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl___________ mol。
(1)烧制普通玻璃的原料是纯碱、石灰石和石英砂,它们在玻璃窑中发生化学变化生成CaSiO3和Na2SiO3的化学方程式为
(2)工业上可利用水玻璃和盐酸反应制备硅酸凝胶后,进一步脱水处理可得到硅胶,请设计实验验证水玻璃与盐酸反应产生少量硅酸时,形成的分散系属于胶体:
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=
(4)高纯度单晶硅可以按下列方法制备:
SiO2
 Si(粗)
Si(粗) SiHCl3
SiHCl3 高纯度单晶硅
高纯度单晶硅①写出SiO2转化为Si(粗)的化学方程式:
②SiHCl3被H2还原为Si(纯)的基本反应类型为
③写出高纯度单晶硅在信息技术或新能源技术等领域的应用:
(5)SiO2属于
(6)向盐酸中逐滴滴加制得的硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在5~100nm的SiO2·nH2O粒子。该分散系属于
(7)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是
①玻璃②石英玻璃③陶瓷④硅芯片⑤砖瓦⑥水泥⑦光导纤维
(8)0.1mol
 与0.05mol
与0.05mol 在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体(9)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[
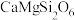 ]和橄榄石[
]和橄榄石[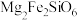 ])等,则辉石[
])等,则辉石[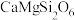 ]的氧化物形式可表示为
]的氧化物形式可表示为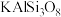 ]
]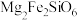 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
I.下列物品或设施:
①陶瓷餐具;②门窗玻璃;③水晶镜片;④硅太阳能电池;⑤光导纤维;⑥手机芯片。
(1)直接使用了硅单质的是(用序号填空)_______
II.在学习了硫的转化后,某学生绘制了如图转化关系。
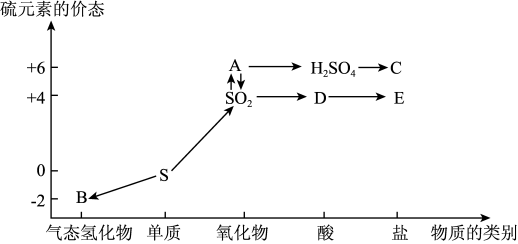
(2)写出简单气态氢化物B的结构式:_______ 。
(3)写出 转化为A的化学方程式:
转化为A的化学方程式:_______ 。
(4)下列五种有色溶液与 作用均能褪色
作用均能褪色
①品红溶液;②酸性 溶液;③溴水;④滴有酚酞的NaOH溶液;⑤淀粉-碘溶液
溶液;③溴水;④滴有酚酞的NaOH溶液;⑤淀粉-碘溶液
体现了 还原性的是(用序号填空)
还原性的是(用序号填空)_______ 。写出 通入酸性
通入酸性 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(5)工业生产中利用氨水吸收 和
和 ,原理如图所示:
,原理如图所示:
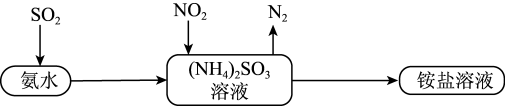
 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______ 。
(6)硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生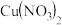 以外,还产生了NO与
以外,还产生了NO与 两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):反应产生的混合气体中,产生NO气体的体积为
两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):反应产生的混合气体中,产生NO气体的体积为_______ L(标准状况下测定)。
I.下列物品或设施:
①陶瓷餐具;②门窗玻璃;③水晶镜片;④硅太阳能电池;⑤光导纤维;⑥手机芯片。
(1)直接使用了硅单质的是(用序号填空)
II.在学习了硫的转化后,某学生绘制了如图转化关系。

(2)写出简单气态氢化物B的结构式:
(3)写出
 转化为A的化学方程式:
转化为A的化学方程式:(4)下列五种有色溶液与
 作用均能褪色
作用均能褪色①品红溶液;②酸性
 溶液;③溴水;④滴有酚酞的NaOH溶液;⑤淀粉-碘溶液
溶液;③溴水;④滴有酚酞的NaOH溶液;⑤淀粉-碘溶液体现了
 还原性的是(用序号填空)
还原性的是(用序号填空) 通入酸性
通入酸性 溶液反应的离子方程式:
溶液反应的离子方程式:(5)工业生产中利用氨水吸收
 和
和 ,原理如图所示:
,原理如图所示:
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生
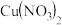 以外,还产生了NO与
以外,还产生了NO与 两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):反应产生的混合气体中,产生NO气体的体积为
两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):反应产生的混合气体中,产生NO气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学与生产、生活密切相关,回答下列问题。
(1)工业生产过程中氨在分离器中进行分离,分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的___________ 的性质。
(2)工业上用氨氧化制取硝酸的流程如下:___________ 。
②如果没有“尾气处理装置”,可能产生的环境问题是___________ 。
③实验室中硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因___________ 。
(3)下列物品或设施:①陶瓷餐具 ②砖瓦 ③混凝土桥墩 ④门窗玻璃 ⑤水晶镜片 ⑥石英钟 ⑦水晶项链 ⑧硅太阳能电池 ⑨石英光导纤维 ⑩计算机芯片
含有硅单质的是___________ (填序号),含有硅酸盐的是___________ (填序号)
(4)火力发电厂烟气中的二氧化硫等气体会造成一系列的环境和生态问题。为实现绿色环保、废物利用等目的,现探究控制和治理二氧化硫的有效途径。
碘、水吸收二氧化硫,具体流程如图所示。已知:HI易挥发。___________ 。
②碘、水吸收二氧化硫的总反应方程式为___________ 。
(1)工业生产过程中氨在分离器中进行分离,分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(2)工业上用氨氧化制取硝酸的流程如下:
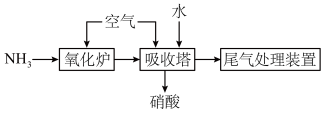
②如果没有“尾气处理装置”,可能产生的环境问题是
③实验室中硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因
(3)下列物品或设施:①陶瓷餐具 ②砖瓦 ③混凝土桥墩 ④门窗玻璃 ⑤水晶镜片 ⑥石英钟 ⑦水晶项链 ⑧硅太阳能电池 ⑨石英光导纤维 ⑩计算机芯片
含有硅单质的是
(4)火力发电厂烟气中的二氧化硫等气体会造成一系列的环境和生态问题。为实现绿色环保、废物利用等目的,现探究控制和治理二氧化硫的有效途径。
碘、水吸收二氧化硫,具体流程如图所示。已知:HI易挥发。
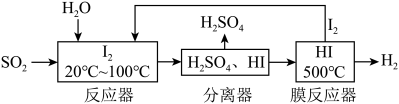
②碘、水吸收二氧化硫的总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】高纯二氧化硅可用来制造光纤。某蛇纹石的成分见下表:
通过下图流程可由蛇纹石制备较纯净的二氧化硅。

(1)蛇纹石中涉及的可溶性金属氧化物有____________ (写化学式)。
(2)步骤①中涉及SiO2反应的离子方程式为________________ 。
(3)滤渣A 的成分有______________________ (填化学式)。
(4)步骤②中洗涤沉淀的方法是_____________________ 。
(5)步骤③反应的化学方程式为______________________ ;实验室进行步骤③需要用到的仪器有坩埚、泥三角、酒精灯、玻璃棒、和________________ 。
组分 | SiO2 | MgO | Na2O | K2O | Fe2O3 |
质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.8 |

(1)蛇纹石中涉及的可溶性金属氧化物有
(2)步骤①中涉及SiO2反应的离子方程式为
(3)滤渣A 的成分有
(4)步骤②中洗涤沉淀的方法是
(5)步骤③反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 以上。
以上。
(1)下列物质不属于硅酸盐产品的是_______。
(2)埋在地下的光导纤维如果裸露在碱性土壤中,会导致断路,用离子方程式说明原因_______ ;工艺师常用_______  填物质名称
填物质名称 来雕刻玻璃。
来雕刻玻璃。
(3)工业上常利用反应 制备硅单质,该反应能否说明C的氧化性强于Si?
制备硅单质,该反应能否说明C的氧化性强于Si?_______  说明理由
说明理由 。
。
(4)有一Si、Al的混合固体,欲从中分离出Si,应如何操作?_______ 。
 以上。
以上。(1)下列物质不属于硅酸盐产品的是_______。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
 填物质名称
填物质名称 来雕刻玻璃。
来雕刻玻璃。(3)工业上常利用反应
 制备硅单质,该反应能否说明C的氧化性强于Si?
制备硅单质,该反应能否说明C的氧化性强于Si? 说明理由
说明理由 。
。(4)有一Si、Al的混合固体,欲从中分离出Si,应如何操作?
您最近一年使用:0次



