日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
更新时间:2023-12-05 12:59:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:

(1)写出下列元素符号:①_________ ,⑥_________ ,⑦_______ 。
(2)画出原子的结构示意图:④__________ ,⑧____________ 。
(3)在①~12元素中,金属性最强的元素是______ ,非金属性最强的元素是____ ,最不活泼的元素是_____ 。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是___ (填序号),跟它同周期原子半径最小的元素是__ (填序号),它们可以形成____ (填离子或共价)化合物,用电子式表示其形成过程:____ 。(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:_____

(1)写出下列元素符号:①
(2)画出原子的结构示意图:④
(3)在①~12元素中,金属性最强的元素是
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】核外电子排布的表示方法
| 原子的结构示意图 | 离子结构示意图 | |
 | Na+ | Cl- |
| 核内质子数 | 阳离子:核外电子数 | 阴离子:核外电子数 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】科学家发现:具有2、8、20、28、50、82、114、126等数目的质子或中子的原子核具有特别的稳定性,并将这些偶数称为“幻数”,而具有双幻数的 He、
He、 Ni、
Ni、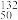 Sn、
Sn、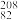 Pb等尤为稳定。根据此信息回答下列问题:
Pb等尤为稳定。根据此信息回答下列问题:
(1)写出上述第三种质子数为“幻数”的元素符号____ ,其元素原子的结构示意图为____ 。
(2)已知氧有三种同位素。 O、
O、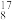 O、
O、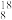 O,根据“幻数”规律,氧的同位素中原子核最稳定的是
O,根据“幻数”规律,氧的同位素中原子核最稳定的是____ 。
(3)根据现有元素周期律推算,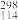 R在元素周期表的位置为
R在元素周期表的位置为____ ,核稳定性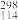 R
R____ 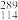 R(填“>”、“<”或“=”)。
R(填“>”、“<”或“=”)。
 He、
He、 Ni、
Ni、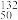 Sn、
Sn、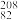 Pb等尤为稳定。根据此信息回答下列问题:
Pb等尤为稳定。根据此信息回答下列问题:(1)写出上述第三种质子数为“幻数”的元素符号
(2)已知氧有三种同位素。
 O、
O、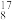 O、
O、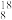 O,根据“幻数”规律,氧的同位素中原子核最稳定的是
O,根据“幻数”规律,氧的同位素中原子核最稳定的是(3)根据现有元素周期律推算,
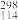 R在元素周期表的位置为
R在元素周期表的位置为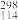 R
R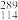 R(填“>”、“<”或“=”)。
R(填“>”、“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】过氧化氢(H2O2)又叫双氧水,其水溶液可用于制备工业上的漂白剂,特殊环境里燃料燃烧的助燃剂,医疗上的消毒剂,实验室里的制氧剂等。过氧化氢分子中的1个过氧原子团“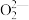 ”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。
”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。
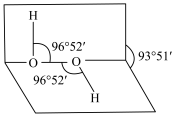

(1)写出过氧化氢分子的电子式:___________ 。
(2)下列关于过氧化氢的说法中正确的是___________ (填序号)。
①分子中有极性键
②分子中有非极性键
③氧原子的轨道发生了sp2杂化
④O—O共价键是p-p σ键
⑤分子是非极性分子
(3)过氧化氢难溶于二硫化碳,主要原因是___________ ;过氧化氢易溶于水,主要原因是___________ 。
 ”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。
”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。

(1)写出过氧化氢分子的电子式:
(2)下列关于过氧化氢的说法中正确的是
①分子中有极性键
②分子中有非极性键
③氧原子的轨道发生了sp2杂化
④O—O共价键是p-p σ键
⑤分子是非极性分子
(3)过氧化氢难溶于二硫化碳,主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程____________ 。
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是________ 。
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是_________________________ 。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl +S +SO2。组装该电池必须在无水、无氧的条件下进行,原因是____________________ (用化学方程式表示)。
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl +S +SO2。组装该电池必须在无水、无氧的条件下进行,原因是
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
| A.从上到下,单质密度依次增大 | B.从上到下,单质熔沸点依次升高 |
| C.从上到下,原子半径依次增大 | D.单质都可以与水反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题:
(1)请写出氯仿的电子式:_______ 。
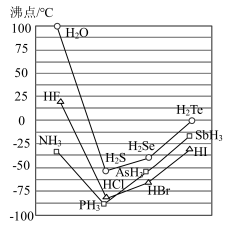
(2)请用一个离子方程式说明 使溴水褪色的原因
使溴水褪色的原因_______ 。
(3)下图中,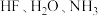 沸点反常的原因是
沸点反常的原因是_______ 。
(1)请写出氯仿的电子式:
(2)请用一个离子方程式说明
 使溴水褪色的原因
使溴水褪色的原因(3)下图中,
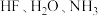 沸点反常的原因是
沸点反常的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用符号A:质子数,B:中子数,C:核外电子数,D:最外层电子数,E:电子层数,填写下列各空。
(1)原子种类由_____ 决定。
(2)元素的种类由_____ 决定
(3)元素的化合价主要由____ 决定
(4)核电荷数由_____ 决定。
(1)原子种类由
(2)元素的种类由
(3)元素的化合价主要由
(4)核电荷数由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(6) 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目
(6)
 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列8种化学符号: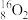 、
、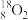 、
、 、
、 、
、 、
、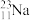 、
、 、
、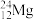 。
。
(1)表示核素的符号共___________ 种。
(2)互为同位素的是___________ 。
(3)质量相同的H216O和D216O所含中子数之比为___________ 。
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:___________ 。
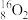 、
、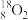 、
、 、
、 、
、 、
、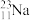 、
、 、
、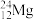 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)1 mol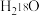 与1 mol
与1 mol 中子数之比为
中子数之比为_______ 。
(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为R2-时,含有电子的物质的量是_______ 。
(1)1 mol
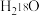 与1 mol
与1 mol 中子数之比为
中子数之比为(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为R2-时,含有电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。
(1)27Al是地壳中最丰富的金属元素,其原子含有中子数为_______ ,与26Al互为_______ 。
(2)用化学符号表示:铝离子的结构示意图_______ ,硅原子的电子式_______ 。
(3)Al与Al3+两种微粒结构上相同的是_______(填选项字母)。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si,计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。核外能量最高的电子位于_______ (填电子层符号)层。
(5)A、B、C、D四种微粒都含10个电子,若A++B- C+D↑,则A+和B-分别是
C+D↑,则A+和B-分别是_______ 、______ 。除C、D外,再写出2个含10个电子的分子_______ 、______ 。
(6)10g10Be所含的中子数与质子数之差为_______ 个。
(1)27Al是地壳中最丰富的金属元素,其原子含有中子数为
(2)用化学符号表示:铝离子的结构示意图
(3)Al与Al3+两种微粒结构上相同的是_______(填选项字母)。
| A.质子数 | B.中子数 | C.电子层数 | D.最外层电子数 |
(5)A、B、C、D四种微粒都含10个电子,若A++B-
 C+D↑,则A+和B-分别是
C+D↑,则A+和B-分别是(6)10g10Be所含的中子数与质子数之差为
您最近一年使用:0次

 X表示原子:
X表示原子:

