下列8种化学符号: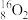 、
、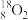 、
、 、
、 、
、 、
、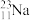 、
、 、
、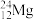 。
。
(1)表示核素的符号共___________ 种。
(2)互为同位素的是___________ 。
(3)质量相同的H216O和D216O所含中子数之比为___________ 。
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:___________ 。
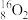 、
、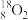 、
、 、
、 、
、 、
、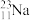 、
、 、
、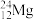 。
。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
(4)根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试着写出Be与NaOH溶液反应生成Na2[Be(OH)4]的离子方程式:
更新时间:2023-12-09 13:23:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】牙膏是常见的日用化学品。
(1)下表列出了两种牙膏中的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
(2)请根据用途推测并说明二氧化硅在水中的溶解性______ (“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。
①甲同学设计了一种在实验室中制备碳酸钙的实验方案(如下所示),请写出下述方案中有关反应的化学方程式______ 、______ 、______ 。

②乙同学设计的实验方案为:

乙同学的实验方案与甲同学的相比,有哪些优点__________ ?请写出乙同学的方案中有关反应的离子方程式_________ 、______ 。
(1)下表列出了两种牙膏中的摩擦剂,请写出它们所属的物质类别(填“酸”“碱”“盐”或“氧化物”)。
| 摩擦剂 | 碳酸钙 | 二氧化硅 |
| 物质类别 |
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。
①甲同学设计了一种在实验室中制备碳酸钙的实验方案(如下所示),请写出下述方案中有关反应的化学方程式

②乙同学设计的实验方案为:

乙同学的实验方案与甲同学的相比,有哪些优点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】四氧化三铁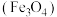 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。
(2)① 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式___________ 。
②验证反应后溶液中含有 的最恰当的试剂是
的最恰当的试剂是___________ 。
A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D. 溶液
溶液
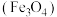 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。

| A.该“运输车”中四氧化三铁和二氧化硅都属于氧化物 |
| B.四氧化三铁起到“磁性导航仪”的作用 |
| C.该“运输车”属于混合物 |
| D.该“运输车”分散于水中所得的分散系属于胶体 |
 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式②验证反应后溶液中含有
 的最恰当的试剂是
的最恰当的试剂是A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D.
 溶液
溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有三组物质①MgO、Na2O、CO2、CuO ②HCl、H2O、H2SO4、HNO3 ③NaOH、Na2CO3、KOH、Cu(OH)2中,均有一种物质的类别与其他三种不同,这三种物质分别用A、B、C表示,则
(1)三种物质依次是(填化学式):A_________ ;B_________ ;C_________ 。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应________ (“是”或“不是”)氧化还原反应。写出该反应的化学方程式:___________________________
(3)写出物质A与足量氢氧化钠溶液反应的离子方程式_______________________ 。
(1)三种物质依次是(填化学式):A
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应
(3)写出物质A与足量氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】由短周期主族元素组成的化合物(如图所示)是一种优质还原剂,能将铜、镍等金属盐还原,其中元素W、X、Y、Z的原子序数依次增大,且总和为35,Z元素最高价氧化物对应水化物的摩尔质量为98g/mol。试回答下列问题:

(1)请写出元素符号:Z_______ 。
(2)X与Y形成的阴阳离子个数比为1:2的化合物的电子式_______ 。
(3)X、Y、Z的原子半径排序_______ (从小到大排序)。
(4)若元素X可组成相对分子质量为32、34、36三种单质X2,此三种气体分子的物质的量之比为9:6:1,X元素有_______ 种核素,中子数较少的核素的原子个数百分含量是_______ 。

(1)请写出元素符号:Z
(2)X与Y形成的阴阳离子个数比为1:2的化合物的电子式
(3)X、Y、Z的原子半径排序
(4)若元素X可组成相对分子质量为32、34、36三种单质X2,此三种气体分子的物质的量之比为9:6:1,X元素有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.现有下列基本粒子:1H、2H、3H、1H+、230Th、232Th、24Na、24Mg、O2、O3、14N、14C,请回答下列问题:
(1)这些粒子分属________ 种元素,有________ 种不同的核素。互为同素异形体的粒子为__________ 。
(2)质量数相等的粒子为____________________________ (可写多组)。
(3)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为__________ ;可得相对分子质量不同的二氧化碳分子种数为______ 。
Ⅱ.现有下列10中物质:①CaCl2 ②NH4Cl ③K2O2 ④Ba(OH)2 ⑤N2 ⑥HBr ⑦AlCl3⑧MgO⑨HNO3⑩CH4。试用以上编号填空:
(1)只有非极性键的是___________________ 。
(2)既有离子键又有极性键的是____________________ 。
(3)属于共价化合物的是__________________ 。
(1)这些粒子分属
(2)质量数相等的粒子为
(3)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为
Ⅱ.现有下列10中物质:①CaCl2 ②NH4Cl ③K2O2 ④Ba(OH)2 ⑤N2 ⑥HBr ⑦AlCl3⑧MgO⑨HNO3⑩CH4。试用以上编号填空:
(1)只有非极性键的是
(2)既有离子键又有极性键的是
(3)属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)写出表示含有8个质子,10个中子的原子的化学符号:__________ 。
(2)根据下列微粒回答问题: 、
、 、
、 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。
①以上8种微粒共有________ 种核素,共_________ 种元素。
②互为同位素的是________________ 。
③质量数相等的是_________ 和_________ ,中子数相等的是_______ 和_________ 。
(3)相同物质的量的14CO2与S18O2的质量之比为_________ ;中子数之比为_______ ;电子数之比为________ 。
(4)铷和另一种碱金属形成的合金7.8 g与足量的水反应后,产生0.2 g氢气,则此合金中另一碱金属可能是:________________ 。(铷的相对原子量取85.5)
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标况下的体积之比为________ 。
(2)根据下列微粒回答问题:
 、
、 、
、 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。①以上8种微粒共有
②互为同位素的是
③质量数相等的是
(3)相同物质的量的14CO2与S18O2的质量之比为
(4)铷和另一种碱金属形成的合金7.8 g与足量的水反应后,产生0.2 g氢气,则此合金中另一碱金属可能是:
(5)质量相同的H2O和D2O与足量钠反应,放出的气体在标况下的体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】请用符号表示下列核素或同位素。
(1)质子数为 ,中子数为
,中子数为 的
的 原子:
原子:______ 。
(2)质子数和中子数都为9的氟原子:______ 。
(3)中子数为2的氢原子:______ 。
(4)中子数分别为8、9、10的氧原子:______ 。
(5)质量数分别为35、37的氯原子:______ 。
(1)质子数为
 ,中子数为
,中子数为 的
的 原子:
原子:(2)质子数和中子数都为9的氟原子:
(3)中子数为2的氢原子:
(4)中子数分别为8、9、10的氧原子:
(5)质量数分别为35、37的氯原子:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在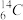 、
、 、
、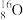 、
、 、
、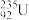 、
、 中
中
(1)____________ 和_____________ 互为同位素;
(2)___________ 和______________ 的质量数相等,但不能互称为同位素;
(3)___________ 和______________ 的中子数相等,但质子数不相等,所以不是同一种元素;
(4)以上所列共有_____________ 种元素;
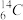 、
、 、
、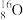 、
、 、
、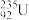 、
、 中
中(1)
(2)
(3)
(4)以上所列共有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.用 表示原子:
表示原子:
(1)中性原子的中子数:N=___________ 。
(2)中性分子中子数:12C16O2分子中,N=___________ 。
(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为___________ mol。
Ⅱ.有①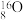 、
、 、
、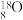 ②H2、D2、T2③红磷、白磷④
②H2、D2、T2③红磷、白磷④ 、
、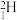 、
、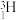 四组微粒或物质,回答下列问题:
四组微粒或物质,回答下列问题:
(1)互为同位素的是___________ (填编号,下同)。
(2)互为同素异形体的是___________ 。
 表示原子:
表示原子:(1)中性原子的中子数:N=
(2)中性分子中子数:12C16O2分子中,N=
(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为
Ⅱ.有①
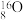 、
、 、
、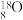 ②H2、D2、T2③红磷、白磷④
②H2、D2、T2③红磷、白磷④ 、
、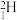 、
、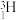 四组微粒或物质,回答下列问题:
四组微粒或物质,回答下列问题:(1)互为同位素的是
(2)互为同素异形体的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】2020年,嫦娘五号带回1731克月壤样本,完成我国首次地外天体采样,并首次发现新矿石——嫦娥石 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。
(1)有关 说法正确的是_______。
说法正确的是_______。
(2)写出P原子的电子式_______ 。
(3) 属于_______。
属于_______。
(4)已知 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,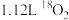 中所含的中子数为_______。
中所含的中子数为_______。
(5)同温同压下,氮气与氧气的体积不同,主要原因是_______。
(6) 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
(7)人造空气(氧气和氮气的混合气)可用于宇航员登月使用。在标准状况下, “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为_______ ,氧气和氦气的分子数之比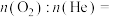
_______ 。
 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。(1)有关
 说法正确的是_______。
说法正确的是_______。| A.质子数为3 | B.与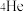 互为同素异形体 互为同素异形体 |
C.与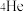 的化学性质相同 的化学性质相同 | D.与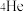 具有相同的电子数 具有相同的电子数 |
(3)
 属于_______。
属于_______。| A.磷酸盐 | B.钙盐 | C.混合物 | D.有机物 |
 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,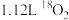 中所含的中子数为_______。
中所含的中子数为_______。A. | B. | C.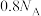 | D. |
| A.气体的分子大小不同 | B.气体的性质不同 |
| C.气体的分子数不同 | D.气体的分子间距不同 |
 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。| A.核外电子的质量太小,忽略不计 |
| B.质子和中子的相对原子质量都很接近1 |
| C.氧的其它同位素的丰度太低,忽略不计 |
| D.元素的近似相对原子质量约等于质量数 |
 “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为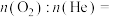
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将下列物质按要求填空
①131 I 与132I ②C60 与石墨 ③CH3Cl 与CH3CH2Cl ④硫酸氢钠 ⑤ 氯化镁 ⑥氩
⑦过氧化氢 ⑧
⑨CS2 ⑩过氧化钠
(1)互为同位素的是_______________________
(2)互为同素异形体的是__________________________
(3)互为同系物的是________________________________
(4)⑧中两种物质的关系是______________ (同系物,同素异形体,同一种物质)
(5)含共价键的离子化合物__________________________________
(6)仅含共价键的物质______________________________________
(7)用电子式表示⑨的形成过程______________________________
①131 I 与132I ②C60 与石墨 ③CH3Cl 与CH3CH2Cl ④硫酸氢钠 ⑤ 氯化镁 ⑥氩
⑦过氧化氢 ⑧

⑨CS2 ⑩过氧化钠
(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同系物的是
(4)⑧中两种物质的关系是
(5)含共价键的离子化合物
(6)仅含共价键的物质
(7)用电子式表示⑨的形成过程
您最近一年使用:0次

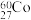 放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。
放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。 ,其中,
,其中,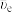 是反中微子,它的电荷数为0,静止质量可认为是0。
是反中微子,它的电荷数为0,静止质量可认为是0。

