2020年,嫦娘五号带回1731克月壤样本,完成我国首次地外天体采样,并首次发现新矿石——嫦娥石 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。
(1)有关 说法正确的是_______。
说法正确的是_______。
(2)写出P原子的电子式_______ 。
(3) 属于_______。
属于_______。
(4)已知 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,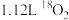 中所含的中子数为_______。
中所含的中子数为_______。
(5)同温同压下,氮气与氧气的体积不同,主要原因是_______。
(6) 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
(7)人造空气(氧气和氮气的混合气)可用于宇航员登月使用。在标准状况下, “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为_______ ,氧气和氦气的分子数之比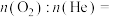
_______ 。
 。月壤中存在着大量的
。月壤中存在着大量的 ,
, 有望成为未来的清洁能源。
有望成为未来的清洁能源。(1)有关
 说法正确的是_______。
说法正确的是_______。| A.质子数为3 | B.与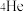 互为同素异形体 互为同素异形体 |
C.与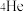 的化学性质相同 的化学性质相同 | D.与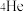 具有相同的电子数 具有相同的电子数 |
(3)
 属于_______。
属于_______。| A.磷酸盐 | B.钙盐 | C.混合物 | D.有机物 |
 为阿伏加德罗常数的值。标准状况下,
为阿伏加德罗常数的值。标准状况下,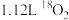 中所含的中子数为_______。
中所含的中子数为_______。A. | B. | C.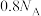 | D. |
| A.气体的分子大小不同 | B.气体的性质不同 |
| C.气体的分子数不同 | D.气体的分子间距不同 |
 的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。
的质量数常被当作氧元素的近似相对原子质量。“近似”的含义不包括_______。| A.核外电子的质量太小,忽略不计 |
| B.质子和中子的相对原子质量都很接近1 |
| C.氧的其它同位素的丰度太低,忽略不计 |
| D.元素的近似相对原子质量约等于质量数 |
 “人造空气”的质量是
“人造空气”的质量是 。该混合气体的平均相对分子质量为
。该混合气体的平均相对分子质量为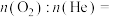
更新时间:2024-01-12 23:15:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g·cm-3的溶液。请计算:
①混合后的溶液中NaCl的质量分数为__________________ 。
②混合后的溶液的物质的量浓度为___________ 。
③在1 000g水中需加入__________ mol氯化钠,才能使其浓度恰好与上述混合后的溶液的浓度相等(计算结果保留1位小数)。
(2)相同条件下,某Cl2与O2混合气体100 mL恰好与150 mL H2化合生成HCl和H2O,则混合气体中Cl2与O2的体积比为__________ ,混合气体的平均相对分子质量为____________ 。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为____________ 。
(4)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为____________ (计算结果保留1位小数) 。若其中CO和N2的物质的量之比为1∶1,则混合气体中氧元素的质量分数为_______________ (计算结果保留1位小数)。
①混合后的溶液中NaCl的质量分数为
②混合后的溶液的物质的量浓度为
③在1 000g水中需加入
(2)相同条件下,某Cl2与O2混合气体100 mL恰好与150 mL H2化合生成HCl和H2O,则混合气体中Cl2与O2的体积比为
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
(4)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:
(1)现有标准状况下CO和 混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为
混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为_______ ,质量之比为_______ ;
(2)40.5g某金属氯化物 中含有
中含有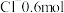 ,则M的相对原子质量为
,则M的相对原子质量为_______ ;
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为_______ ;
(4)将4gNaOH溶于_______ g水中,可使溶液中 和
和 的物质的量之比为
的物质的量之比为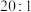 ,若测得该溶液的密度为
,若测得该溶液的密度为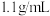 ,溶液中
,溶液中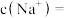
_______ ;
(5)已知阴离子 的原子核内有n个中子,R原子的质量数为m,则
的原子核内有n个中子,R原子的质量数为m,则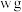 该离子所含电子的物质的量为
该离子所含电子的物质的量为_______ ;
(6)明矾溶于水的电离方程式_______ ;
(7)工业上电解饱和食盐水制备氯气的方程式_______ 。
(1)现有标准状况下CO和
 混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为
混合气体8.96L,其质量为16g,则此混合气体中,CO气体的体积分数为(2)40.5g某金属氯化物
 中含有
中含有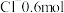 ,则M的相对原子质量为
,则M的相对原子质量为(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)将4gNaOH溶于
 和
和 的物质的量之比为
的物质的量之比为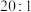 ,若测得该溶液的密度为
,若测得该溶液的密度为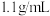 ,溶液中
,溶液中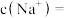
(5)已知阴离子
 的原子核内有n个中子,R原子的质量数为m,则
的原子核内有n个中子,R原子的质量数为m,则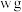 该离子所含电子的物质的量为
该离子所含电子的物质的量为(6)明矾溶于水的电离方程式
(7)工业上电解饱和食盐水制备氯气的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)2molO3和3molO2的质量之比为________ ,分子数之比为________ ,同温同压下的密度之比为________ 。
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2物质的量之比是____ ,混合气体的平均相对分子质量是_____ ,对氢气的相对密度是____ 。
(3)19 gACl2中含有0.4 mol Cl-,则该氯化物的摩尔质量是_____ ;A的相对原子质量是______ 。
(1)2molO3和3molO2的质量之比为
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2物质的量之比是
(3)19 gACl2中含有0.4 mol Cl-,则该氯化物的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)与16 gO2所含原子总数相同的NH3标准状况下体积是___________ L;
(2)100 mL硫酸铝溶液中,c(A13+)=0.2mol/L,则c( )=
)=___________ ;将该溶液稀释至150 mL,稀释后溶液中的Al2(SO4)3的物质的量为___________ 。
(3)同温同压下,同体积的NH3和H2S气体的质量比为___________ ;同质量的NH3和H2S气体的体积比为___________ ,其中含有的氢的原子个数比为___________ ;若二者氢原子数相等,它们的体积比为___________ 。
(4)在标准状况下,8.96 L的CH4和CO的混合气体,二者对氢气相对密度是9.5,混合气体平均摩尔质量为___________ ,混合气体中CH4的体积为___________ ,一氧化碳的质量分数为___________ ,二者原子个数比为___________ 。
(5)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入H2和O2的混合气体,向B室中充入3 mol空气,此时活塞的位置如图所示:

已知A室混合气体的质量为102 g,若将A室中H2与O2的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在___________ (填数字)刻度,反应后容器内气体压强与反应前气体压强之比为___________ 。
(1)与16 gO2所含原子总数相同的NH3标准状况下体积是
(2)100 mL硫酸铝溶液中,c(A13+)=0.2mol/L,则c(
 )=
)=(3)同温同压下,同体积的NH3和H2S气体的质量比为
(4)在标准状况下,8.96 L的CH4和CO的混合气体,二者对氢气相对密度是9.5,混合气体平均摩尔质量为
(5)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入H2和O2的混合气体,向B室中充入3 mol空气,此时活塞的位置如图所示:

已知A室混合气体的质量为102 g,若将A室中H2与O2的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】填空
(1) 中含有的阴离子个数约为
中含有的阴离子个数约为_______ 。
(2)等物质的量的 和
和 ,其质量之比为
,其质量之比为_______ ,所含氧原子数之比为_______ 。
(3)将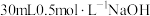 溶液加水稀释到
溶液加水稀释到 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4) 某二价金属的氯化物
某二价金属的氯化物 中含有
中含有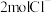 ,则
,则 的摩尔质量为
的摩尔质量为_______ 。
(1)
 中含有的阴离子个数约为
中含有的阴离子个数约为(2)等物质的量的
 和
和 ,其质量之比为
,其质量之比为(3)将
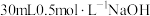 溶液加水稀释到
溶液加水稀释到 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度为
的物质的量浓度为(4)
 某二价金属的氯化物
某二价金属的氯化物 中含有
中含有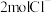 ,则
,则 的摩尔质量为
的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题:
(1)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为_________ ,碳原子和氧原子的个数比为________ ,该混合气体的摩尔质量为__________ 。
(2)12.4g含Na2X中含Na+0.4mol,则Na2X的摩尔质量是________ ,X的相对原子质量是____________ 。
(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是_____________ ,氧气的质量是____________ 。
(1)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为
(2)12.4g含Na2X中含Na+0.4mol,则Na2X的摩尔质量是
(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水。该核废水中含有以目前技术手段无法去除的放射性物质“氚”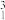 H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
(1)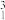 H与
H与 H互为
H互为___ 。
(2)数字3表示___ 。
(3)氢元素的相对原子质量计算表达式___ 。(氕、氘、氚原子的质量用m1,m2,m3表示,C—12原子质量用m0表示)。
(4)碳也有一种放射性核素14C,举出一种该核素的应用___ 。
(5)该两种核素形成的化合物14C3H4中化学键为__ ;空间构型__ ;用电子式表示该化合物的形成过程___ 。
(6)6.5g该两种核素形成的化合物14C3H4,在标况下的体积为___ L;其中所含的质子为___ mol,中子为___ 个。
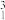 H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)(1)
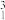 H与
H与 H互为
H互为(2)数字3表示
(3)氢元素的相对原子质量计算表达式
(4)碳也有一种放射性核素14C,举出一种该核素的应用
(5)该两种核素形成的化合物14C3H4中化学键为
(6)6.5g该两种核素形成的化合物14C3H4,在标况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。请回答下列问题:
(1)砷只有一种稳定的同位素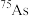 ,其原子核内中子数比核外电子数多
,其原子核内中子数比核外电子数多_______ 个。
(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(复选)。
(3)Marsh试砷法和Gutzeit试砷法是法医学上鉴定砷的重要方法。其原理是先将 (剧毒)转化为
(剧毒)转化为 ,前者让
,前者让 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。
① 的电子式为
的电子式为_______ 。
②Gutzeit试砷法中 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(1)砷只有一种稳定的同位素
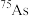 ,其原子核内中子数比核外电子数多
,其原子核内中子数比核外电子数多(2)下列事实中,能说明As元素的非金属性弱于N元素的是_______(复选)。
A.沸点: | B.酸性: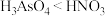 |
C.分解温度: | D.相对分子质量: |
 (剧毒)转化为
(剧毒)转化为 ,前者让
,前者让 分解产生黑亮的砷镜(As),后者让
分解产生黑亮的砷镜(As),后者让 被
被 溶液氧化为
溶液氧化为 ,同时还生成Ag单质。
,同时还生成Ag单质。①
 的电子式为
的电子式为②Gutzeit试砷法中
 被氧化的离子方程式为
被氧化的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图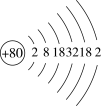 汞在第
汞在第___________ 周期。
(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷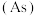 也是氮族元素。
也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是___________ (填序号)。
a、含有离子键和共价键
b、能与 溶液反应
溶液反应
c、与 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样
③砷酸 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:___________ 。
 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)据汞的原子结构示意图
 汞在第
汞在第(2)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷
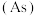 也是氮族元素。
也是氮族元素。①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测不正确的是
性质的推测不正确的是a、含有离子键和共价键
b、能与
 溶液反应
溶液反应c、与
 加热充分分解产物的种类完全一样
加热充分分解产物的种类完全一样③砷酸
 可用于制造杀虫剂、药物。
可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方程式:
溶于稀硝酸中可得砷酸,此反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种核素的比例确定“北京人”生存年代的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)26Al和27Al_______(选填编号)。
(2)碳元素的一种核素也可以考古断代,其原子符号为_______ ;
(3)10 g10Be所含的中子数与质子数之差为_______ 个。
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的_______ 。硅原子的结构示意图为 _______ ,核外能量最高的电子位于_______ (填电子层符号)层。
(1)26Al和27Al_______(选填编号)。
| A.是同一种元素 | B.是同一种核素 | C.具有相同的中子数 | D.具有相同的化学性质 |
(3)10 g10Be所含的中子数与质子数之差为
(4)自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.现有5种有机物:①乙烯 ②乙醇 ③苯 ④乙酸 ⑤乙酸乙酯 ⑥乙醛。
(1)请分别写出其中含有下列官能团的有机物的结构简式:
①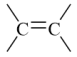
_______ , ②-CHO_______ 。
(2)在上述5种有机物中(填写序号):能发生水解反应的是_______ ;具有酸性且能发生酯化反应的是_______ ;写出乙烯加聚生成聚乙烯的化学方程式:_______ 。
II.有下列各组物质:① 和
和 ;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3 ④正丁烷和异庚烷; ⑤
;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3 ④正丁烷和异庚烷; ⑤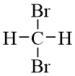 和
和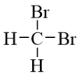 。用序号填空:
。用序号填空:
(3)_______ 组两者互为同位素。
(4)_______ 组两者互为同素异形体。
(5)_______ 组两者属于同系物。
(6)_______ 组两者互为同分异构体。
(7)_______ 组两者是同一物质。
(1)请分别写出其中含有下列官能团的有机物的结构简式:
①

(2)在上述5种有机物中(填写序号):能发生水解反应的是
II.有下列各组物质:①
 和
和 ;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3 ④正丁烷和异庚烷; ⑤
;②石墨和足球烯;③CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3 ④正丁烷和异庚烷; ⑤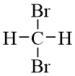 和
和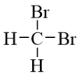 。用序号填空:
。用序号填空:(3)
(4)
(5)
(6)
(7)
您最近一年使用:0次

 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等。已知N2H5+的形成过程类似于NH
等。已知N2H5+的形成过程类似于NH

